Топохимические реакции – гетерогенные реакции, у которых химическое взаимодействие не усложнено диффузионными процессами.
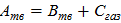
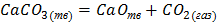
Скорость топохимических реакций характеризуется степенью превращения вещества в единицу времени:
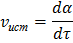
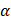 - степень превращения исходного вещества;
- степень превращения исходного вещества;
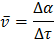
Особенностью топохимических реакций является то, что скорость реакции изменяется по мере разложения исходного вещества:
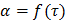
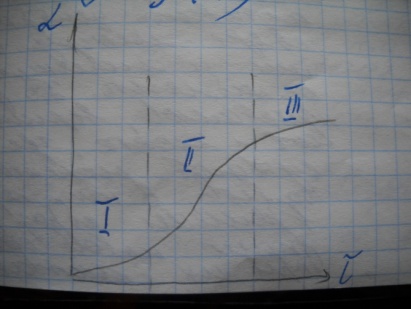
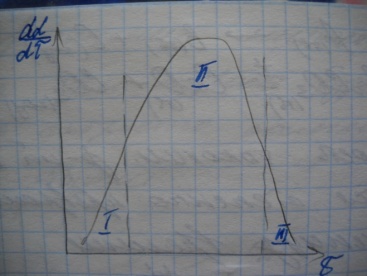
Скорость топохимической реакции зависит от величины реакционной поверхности, которая изменяется в процессе реакции. При протекании топохимической реакции, можно выделить три периода:
а. Индукционный – характеризуется низкой скоростью реакции, т.к. реакция начинается только на активных центрах, где связи между атомами и молекулами ослаблены. Это рёбра кристаллов, вершины углов и места, где присутствуют дефекты кристаллов. В начальный период времени образуются зародыши новой фазы при их контакте с исходным веществом, и начинает протекать реакция, т.к. вначале поверхность раствора мала, следовательно, скорость реакции тоже мала.
б. Основной – характеризуется резким ростом скорости реакции (для гомогенных реакций скорость падает). Такое увеличение скорости реакции, называется автокаталитическим процессом. Причина в том, что по мере развития процесса происходит рост зародышей новой фазы, вследствие этого резко увеличивается поверхность раздела фаз, следовательно, следовательно, увеличивается скорость химического взаимодействия. Максимальная скорость будет соответствовать максимальной величине поверхности фаз. Это произойдёт тогда, когда поверхности отдельных реакционных зон пересекаются друг с другом.
в. Заключительный – резкое снижение скорости реакции, обусловлено тем, что после перекрывания отдельных зон резко сокращается суммарная поверхность раздела фаз.
Уравнение Ерофеева.
Данное уравнение описывает кинетику топохимической реакции. Особенностью уравнения Ерофеева, является то, что оно описывает кинетику реакции только в основном периоде (прямолинейный участок на S-образной кинетически интегральной кривой).
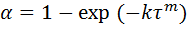
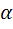 - степень превращения исходного вещества;
- степень превращения исходного вещества;
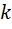 - константа скорости топохимической реакции;
- константа скорости топохимической реакции;
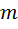 - эмпирический коэффициент.
- эмпирический коэффициент.
Уравнение описывается кривой. Для определения 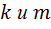 существует два способа:
существует два способа:
- Графическая;
- Аналитическая;
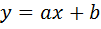
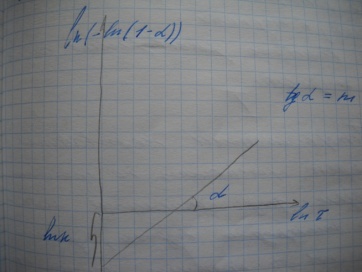
Уравнение логарифмируем:
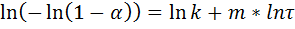
Статистика значений берётся только на прямолинейном участке:
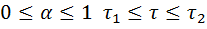
Для аналитического метода выбирают любые два значения 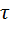 :
: 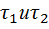 и решают систему уравнений:
и решают систему уравнений:
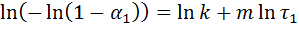
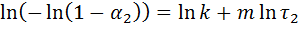
 2018-01-21
2018-01-21 4106
4106