Диссоциация комплексного соединения проходит по двум ступеням: а) диссоциация на комплексный и простой ионы с сохранением внутренней сферы комплекса и б) диссоциация внутренней сферы, приводящая к разрушению комплекса. Диссоциация по первой ступени проходит по типу диссоциации сильных электролитов, а диссоциация комплексного иона - по типу диссоциации слабых электролитов. Диссоциация комплексного соединения будет тем полнее, чем сильнее сдвинуто вправо это равновесие. Диссоциация комплексного соединения - сильного электролита на составляющие его ионы имеет особенности, свойственные диссоциации любого сильного электролита.
Комплексные соединения, имеющие ионную внешнюю сферу, в растворе подвергаются диссоциации на комплексный ион и ионы внешней сферы. Они ведут себя в разбавленных растворах как сильные электролиты: диссоциация протекает моментально и практически нацело. Примеры такого рода:
[Cu(NH3)4]SO4 = [Cu(NH3)4]2+ + SO42-
K3[Fe(CN)6] = 3 K+ + [Fe(CN)6]3-
Однако на отщеплении внешнесферных ионов процесс электролитической диссоциации не заканчивается. Комплексные ионы, в свою очередь, подвергаются обратимой электролитической диссоциации, уже как слабые электролиты, по схеме:
[ML n ]  M + n L
M + n L
Такая диссоциация, разумеется, протекает ступенчато: лиганды удаляются из внутренней сферы постепенно, один за другим (точнее, происходит реакция замещения лиганды на молекулы растворителя - воды).
Для упрощения записи в качестве примера взят незаряженный комплекс, а продукт диссоциации представлен в негидратированном виде.
Аналогичным образом происходит и обратный процесс - образование комплекса. Сначала во внутренней сфере появляется один лиганд, затем второй, третий и так далее:
M + L  [ML]
[ML]
[ML] + L  [ML2]
[ML2]
[ML2] + L  [ML3]
[ML3]
…….
[ML(n -1)] + L  [ML n ]
[ML n ]
Процесс комплексообразования завершается, когда число присоединившихся монодентатных лигандов L станет равным координационному числу комплексообразователя M. При этом устанавливается динамическое равновесие, поскольку наряду с образованием комплексов идет и их диссоциация.
Химические свойства комплексного иона с известной электронной конфигурацией и геометрическим строением определяются двумя факторами: а) способностью равновесной системы при определенных условиях к превращениям; б) скоростью, с которой могут происходить превращения, ведущие к достижению равновесного состояния системы.
Первый определяет термодинамическую, а второй – кинетическую устойчивость комплексного соединения. Кинетическая устойчивость зависит от многих факторов, поэтому обычно поддается лишь качественной оценке.
В противоположность ей термодинамическая устойчивость может быть легко охарактеризована количественно с помощью констант равновесия.
В растворе ион металла M и монодентатный лиганд L взаимодействуют ступенчато с образованием комплексного иона [MLn] по схеме:

|

где Ki – ступенчатые константы образования (устойчивости) отдельных комплексов [MLi].
Поскольку в этой системе существует лишь n независимых равновесий, полная константа процесса M + nL = MLn – общая константа образования:
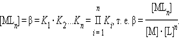

Чем больше константа устойчивости, тем более прочным является данный комплекс, поскольку ΔG° = –RT lnβ.
Образование прочных комплексных ионов может быть использовано для растворения труднорастворимых электролитов. Концентрация ионов в растворе определяется величиной произведения растворимости такого электролита. Добавляя в раствор вещества, образующие с одним из его ионов комплексное соединение, можно во многих случаях достичь растворения осадка за счет комплексообразования. Добиться этого тем легче, чем больше величина произведения растворимости и чем больше константа устойчивости комплексного иона. Например, хлорид серебра AgCl растворяется в избытке аммиака, образуя [Ag(NH3)2]Cl. Менее растворимый AgI в аммиаке практически не растворим, но растворяется в тиосульфате натрия Na2S2O3 по реакции

|
поскольку β[Ag(S2O3)2]3– на несколько порядков больше β[Ag(NH3)2]+.
Комплексные ионы участвуют в реакциях обмена с образованием более прочного или менее растворимого соединения:
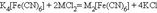
Здесь M = Ni2+, Cu2+, Fe2+.
(ИЗ УЧЕБНИКА ГЛИНКА): Константа нестойкости – константа равновесия реакции распада. Они могут относиться к отдельным стадиям распада (ступенчатые константы нестойкости Ki) и к суммарной реакции (полная константа нестойкости Kн).
Чем больше константа нестойкости, тем устойчивее комплексное соединение.
Kобр=1/Kн
Для суммарной реакции константу образования принято обозначать β.
Чем больше константа образования, тем устойчивее комплексное соединение.
 2018-01-21
2018-01-21 1902
1902
