А служат для накопления энергии, чтобы в нужный момент расходовать её. Накопление энергии осуществляется при пропускании постоянного электрического тока через А. При этом происходит преврщение электрической энергии в химическую (электролиз). Под влиянием эл.тока идёт окислит-восстановит реакция (ОВР) и А заряжается. При разрядке идёт та же реакция, но в обратонм направлении: химическая энергия превращается в эектрическую.
Существует два вида А: кислотный(синцовый) и щелочной(никель-кадмиевый и никель-железный)
Анод заряженного свинцового аккумулятора состоит из свинца, катод – из диоксида свинца. Металлический тип проводимости PbO2 делает его пригодным для работы в качестве электрода. Электролитом служит раствор H2SO4 (32–39 %), в котором PbSO4 и PbO2 малорастворимы.
Схему аккумулятора можно изобразить так:

Анодный процесс работающего аккумулятора

катодный процесс –

Таким образом, в свинцовом аккумуляторе осуществляется реакция
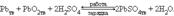
При зарядке протекает обратная реакция и электроды меняют свои функции: катод становится анодом, а анод – катодом. ЭДС свинцового аккумулятора зависит от отношения активности кислоты и воды:

В процессе работы аккумулятора концентрация кислоты падает, а следовательно, падает и ЭДС. Когда ЭДС достигает 1,85 В, аккумулятор считается разрядившимся. При более низкой ЭДС пластины покрываются тонким слоем PbSO4 и и аккумулятор разряжается необратимо. Во избежание этого аккумулятор периодически подзаряжают.
Показателем того, что зарядка закончена является кипение А. Он даёт напряжение 2В. Позволительный разряд 1,7В. При более сильной разрядке происходит сульфатация и А выходит из строя. Свинцовые А нельзя долго хранить в заряженном виде, т.к. на пластинах происходит саморазряд. Свинцовый А даёт более высокое напряжение, чем щелочной, у него высокий КПД, большая ёмкость, но большие габориты. Таке недостатком является то, что электролит и серная кислота должны быть очень чистыми (без примесей). Свинцовые А применяются для питания радио- и телефонной аппаратуры, для питания оборудования на автотранспорте.
42. Никель-кадмиевый и никель железный аккумуляторы. Герметичный никель кадмиевый аккумулятор.
Щелочные А бывают железно-никелевые, кадмиев-никелевые, серебренно-цинковые. При разрядке первого образуется гидроксид железа (II) и гидроксид никеля (II). Зарядка идёт в обратном направлении и образуется железо и гидроксид никеля (III). Даёт напряжение 1.45-1.48В, Позволительный разряд 1В. Саморазряд возможен, но в меньшей степени, чем у свинцового. Он меньше по габоритам и лучше выдерживает толчки вибрации, но у него меньше КПД и ёмкость. Применяется для освещения вагонов на ж/д транспорте, для питания ламп шахтёров.
Рассмотрим процесс работы. В заряженном щелочном железо-никелевом аккумуляторе анодом служит железо, катодом – гидроксид никеля (III), электролит – 20%-й раствор KOH:
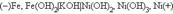
При работе аккумулятора на аноде происходит окисление железа:

на катоде – восстановление гидроксида никеля (III): 
Суммарная активность процесса:

ЭДС щелочного аккумулятора не зависит от концентрации щелочи.
Аналогично работают щелочные кадмий-никелевый 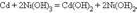
и серебряно-цинковый аккумуляторы:

В потребительской электронике, большинство аккумуляторов - никель-кадмиевые. Это самый популярный тип подзаряжаемых батареек. Обычно их обозначают NiCad. Катоды в таких элементах сделаны из никеля, а аноды - кадмиевые
Особую группу никель-кадмиевых аккумуляторов составляют герметичныеаккумуляторы
Как и в свинцовых аккумуляторах, в никель-кадмиевых батарейках возможен электролиз - распад воды в электролите на потенциально взрывоопасные водород и кислород.
Производители батареек предпринимают различные меры для предотвращения этого эффекта. Обычно элементы для предотвращения утечки герметично упаковывают. Кроме того, батарейки устроены так, чтобы сначала вырабатывался не водород, а кислород, который предотвращает реакцию электролиза.
Для того чтобы герметичные аккумуляторы не взрывались, и чтобы в них не скапливался газ, обычно в батарейках предусматривают клапаны. Если закрыть эти вентиляционные отверстия, то возникнет опасность взрыва. Обычно эти отверстия настолько малы, что остаются незамеченными. Работают они автоматически. Это предостережение (не закрывать вентиляционные отверстия) относятся в основном к производителям устройств. Стандартные отсеки для батареек предполагают возможность вентиляции, но вот если залить батарейку в эпоксидной смоле, то вентиляции не будет.
 2018-01-21
2018-01-21 1180
1180
