Каждый из идеальных газов ведет себя в смеси автономно, т. е. так, будто других газов нет. Отсутствие межмолекулярного взаимодействия у идеальных газов обусловливает независимость их свойств от других газов, составляющих смесь. Следствием этой независимости свойств идеальных газов в смеси является строгая аддитивность таких термодинамических величин смеси как давление, внутренняя энергия, энтальпия и т. д.
(Термин «аддитивный» происходит от латинского additivus - полученный путем сложения)
Т. о. вышеперечисленные термодинамические величины для всей смеси получаются путем арифметического сложения соответствующих величин всех компонентов смеси.
Примеры аддитивных величин:масса смеси газов, внутренняя энергия смеси, энтальпия смеси, все термодинамические функции состояния смеси газов, включая характеристические функции ( ) и энтропию
) и энтропию  (термодинамический параметр состояния).
(термодинамический параметр состояния).
Масса смеси:
 .
.
Внутренняя энергия  смеси nгазов массой
смеси nгазов массой  , занимающих объем
, занимающих объем  , равна:
, равна:
 ,
,
где:  - внутренняя энергия
- внутренняя энергия  килограммов i -го газа в составе
килограммов i -го газа в составе
смеси, Дж
Обозначим: uсм - удельная внутренняя энергия смеси газов (внутренняя энергия одного кг смеси), Дж / кг; ui- удельная внутренняя энергия i -го газа смеси, Дж / кг
 ,
,
 .
.
Тогда:

Окончательно:

 .
.
Энтальпия смеси  газов
газов  , Дж:
, Дж:
 ,
,
где:  - энтальпия
- энтальпия  килограммов i - го газа в составе смеси;
килограммов i - го газа в составе смеси;  = 1, 2,..........,
= 1, 2,..........,  .
.
(В формулах для вычисления энтальпии индекс «i» для газа заменен на « » во избежание совпадения обозначений удельной энтальпии (i) и индекса i -го газа)
» во избежание совпадения обозначений удельной энтальпии (i) и индекса i -го газа)
По аналогии с внутренней энергией можно получить формулу для удельной энтальпии смеси газов iсм, Дж / кг:

где: 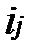 - удельная энтальпия i -го газа в составе смеси.
- удельная энтальпия i -го газа в составе смеси.
Все термодинамические функции состояния смеси газов также обладают свойством аддитивности.К функциям состояния помимо всех характеристических функций ( ) относится также энтропия
) относится также энтропия  - термодинамический параметр состояния.
- термодинамический параметр состояния.
Здесь:  - свободная энергия (энергия Гельмгольца, изохорно-изотермический потенциал);
- свободная энергия (энергия Гельмгольца, изохорно-изотермический потенциал);
 - свободная энтальпия (энтальпия Гиббса, изобарный потенциал, изобарно-изотермический потенциал).
- свободная энтальпия (энтальпия Гиббса, изобарный потенциал, изобарно-изотермический потенциал).
Для свободной энергии по аналогии с внутренней энергией и энтальпией смеси можно окончательно записать:
У дельная свободная энергия  -компонентной смеси газов массой
-компонентной смеси газов массой  , Дж / кг:
, Дж / кг:
 ,
,
где:  - удельная свободная энергия i -го газа смеси, Дж / кг.
- удельная свободная энергия i -го газа смеси, Дж / кг.
Удельная свободная энергия смеси газов, Дж / кг:
 ,
,
где: 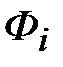 - удельная свободная энергия i -го газа смеси, Дж / кг
- удельная свободная энергия i -го газа смеси, Дж / кг
Удельная энтропия смеси газов, Дж / (кг К)
 ,
,
где:  - удельная энтропия i -го газа смеси, Дж / (кг К)
- удельная энтропия i -го газа смеси, Дж / (кг К)
 2018-01-21
2018-01-21 815
815








