МОСКОВСКИЙ ТЕХНОЛОГИЧЕСКИЙ УНИВЕРСИТЕТ
Институт тонких химических технологий
| Кафедра общей химической технологии |
Курсовая работа
по теме: «Производство этилового спирта»
Вариант № 3
| Выполнил: студент группыХЕБО-13-14 Першина А.В. |
| Преподаватель: Устюгов А.В. |
МОСКВА 2017
Содержание
этиловый спирт синтез гидратация
1. Введение
2. Сырьевая база
3. Характеристика целевого продукта
4. Сернокислотная гидратация этилена
5. Прямая гидратация этилена
6. Технологическая схема синтеза производства этилового спирта
7. Структурная блок-схема
8. Балансовая математическая модель
9. Материальный баланс ХТС
10. Список литературы
Введение
В мировой химической промышленности производство этилового спирта занимает одно из первых мест. Так, в 2009 году в мире было произведено почти 59 миллионов тонн. Такие объемы производства позволяют отнести производство этанола к разряду крупнотоннажных.
Этиловый спирт широко применяется в различных отраслях промышленности. Его используют в медицине в качестве растворителя для лекарственных средств, для обеззараживания, как пеногаситель в системах подачи кислорода, для лечения отравления метиловым спиртом. Этанол широко применяется в пищевой промышленности для производства различных видов спиртных напитков, в парфюмерии в качестве основного компонента для духов, одеколонов.
В последнее время в мире широко развивается производство биотоплива на основе этилового спирта. Так же этанол используют как компонент ракетного топлива. Этиловый спирт широко применяется в химической промышленности в качестве полупродукта в основном органическом синтезе.
Исходное сырье
В промышленности для получения этилового спирта в качестве исходного сырья используютрастительные продукты, в составе которых есть крахмал или сахар, и этилен. Отдается предпочтение методу прямой гидратации этилена.
Основными источниками этилена являются промышленные газы нефтеперерабатывающего производства, которые образуются при переработке нефтяного сырья, газы, получаемые дегидрированием газообразных парафинов, коксовый газ.
Из газовых смесей этилен необходимо сконцентрировать и выделить. Для этого применяют сорбцию, хемосорбцию и конденсационную ректификацию. В промышленности наиболее распространен последний способ, так как позволяет из сложной смеси водорода, предельных и непредельных углеводородов, получать этиленовую фракцию с концентрацией 96-99% этилена.
Характеристика целевого продукта
Физические свойства
Этиловый спирт представляет собой бесцветную прозрачную легкоподвижную жидкость с характерным запахом. Значения физических свойств:
| Свойство | Значение |


| 
|

| 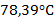
|

| 
|

| 
|

| 
|

| 
|

| 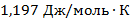
|
Этиловый спирт смешивается во всех соотношениях с водой, спиртами, диэтиловым эфиром, глицерином, хлороформом, ацетальдегидом, бензином и др. С воздухом образует взрывоопасные смеси в пределах концентраций 3–20% (об.). Образует азеотропные смеси: с водой дает азеотропную смесь, содержащую 95,6% спирта и кипящую при 78,1°С (в виде такого ректификата этанол обычно употребляют в технике); с бензолом (32,4%; 68,24°С); с гексаном (21%; 58,7°С); с этилацетатом (30,8%; 71,8°С).
Химические свойства
Этанол – одноатомный алифатический спирт. Горит светлым голубоватым пламенем, образуя диоксид углерода и воду.
Является слабой ОН-кислотой, по кислотности мало отличаясь от воды. Взаимодействует со щелочными металлами, образуя при этом этоксиды:

Реагирует с кислотами. Будучи первичным спиртом, реагирует без осложнения с неорганическими кислотами, образуя сложные эфиры:

С галогенводородами вступает в обратимые реакции нуклеофильного замещения, реагирует с тионилхлоридом:


При нагреве до 170-200°Сдегидратируется в присутствии серной кислоты:

Реагирует с  , образуя моно-, ди- и триэтиламины:
, образуя моно-, ди- и триэтиламины:

 2018-01-21
2018-01-21 1491
1491







