Глава 13. Абсорбция
Абсорбцией называется избирательное поглощение компонентов паровых или газовых смесей жидким поглотителем. Десорбция  процесс обратный абсорбции, т.е. переход отдельных компонентов жидкой смеси в газовую фазу. Абсорбтив
процесс обратный абсорбции, т.е. переход отдельных компонентов жидкой смеси в газовую фазу. Абсорбтив  распределяемый компонент газовой фазы, переходящий в жидкую. Абсорбент
распределяемый компонент газовой фазы, переходящий в жидкую. Абсорбент  жидкий поглотитель. Инертный газ
жидкий поглотитель. Инертный газ  компонент газовой смеси не переходящий границу раздела фаз. Необходимо иметь в виду, что инертный газ может состоять из нескольких компонентов, например, воздух, абсорбент также может быть многокомпонентным и поглощаться в общем случае могут несколько компонентов. Рассмотрим вначале простейший случай бинарной абсорбции, когда в каждой фазе содержится не более двух компонентов: в газовой – абсорбтив и инертный газ, в жидкой – абсорбтив и абсорбент. Более общий случай многокомпонентной абсорбции рассматривается в разделе 13.4.
компонент газовой смеси не переходящий границу раздела фаз. Необходимо иметь в виду, что инертный газ может состоять из нескольких компонентов, например, воздух, абсорбент также может быть многокомпонентным и поглощаться в общем случае могут несколько компонентов. Рассмотрим вначале простейший случай бинарной абсорбции, когда в каждой фазе содержится не более двух компонентов: в газовой – абсорбтив и инертный газ, в жидкой – абсорбтив и абсорбент. Более общий случай многокомпонентной абсорбции рассматривается в разделе 13.4.
Различают физическую абсорбцию, не сопровождающуюся химическими реакциями, и хемосорбцию, при которой абсорбтив образует с абсорбентом химическое соединение.
Абсорбция широко применяется в промышленности для извлечения ценных компонентов газовых смесей (бензола из коксового газа) или очистки их от вредных примесей (коксового газа от сероводорода), а также с целью получения готового продукта (серной кислоты за счет поглощения 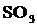 водой).
водой).
Особенности равновесия и массопередачи в процессе абсорбции
Как отмечалось в разделе 12.2.1, при записи уравнений материального баланса и рабочих линий целесообразно выбирать единицы измерения расходов таковыми, чтобы эти величины не менялись по высоте аппарата. Это сделает рабочие линии прямыми и упростит процедуру расчета. В случае абсорбции по высоте колонны не изменяются массовые и мольные расходы инертного газа и абсорбента, что позволяет использовать их в уравнениях материального баланса и рабочих линий в совокупности с относительными массовыми и относительными мольными концентрациями распределяемых компонентов. Выберем, например, массовые расходы и концентрации, тогда
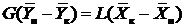 , (13.1)
, (13.1)
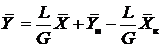 , (противоток) (13.2)
, (противоток) (13.2)
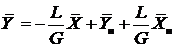 , (прямоток) (13.3)
, (прямоток) (13.3)
где 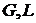 массовые расходы инертного газа и абсорбента (кг/с);
массовые расходы инертного газа и абсорбента (кг/с); 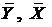
 относительные массовые концентрации абсорбтива в инертном газе (кг абсорбтива/ кг инертного газа) и в абсорбенте (кг абсорбтива / кг абсорбента). С использованием этих же концентраций запишем уравнение линии равновесия.
относительные массовые концентрации абсорбтива в инертном газе (кг абсорбтива/ кг инертного газа) и в абсорбенте (кг абсорбтива / кг абсорбента). С использованием этих же концентраций запишем уравнение линии равновесия.
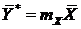 ;
; 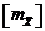 =кг абсорбента/ кг инертного газа. (13.4)
=кг абсорбента/ кг инертного газа. (13.4)
В связи с этим коэффициенты распределения 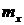 , способы определения которых подробно рассмотрены, как для равновесия в системах пар
, способы определения которых подробно рассмотрены, как для равновесия в системах пар  жидкость, так и газ
жидкость, так и газ  жидкость в разделе 12.1, необходимо перевести в соответствующие единицы измерения
жидкость в разделе 12.1, необходимо перевести в соответствующие единицы измерения 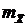 [9, 49]. В соответствии с правилом фаз Гиббса (12.3) для трехкомпонентной двухфазной системы число степеней свободы равно трем, т.е.
[9, 49]. В соответствии с правилом фаз Гиббса (12.3) для трехкомпонентной двухфазной системы число степеней свободы равно трем, т.е. 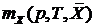 . Если процесс абсорбции проводится при постоянных давлении и температуре, то их можно считать фиксированными и коэффициент распределения будет являться функцией только одной переменной
. Если процесс абсорбции проводится при постоянных давлении и температуре, то их можно считать фиксированными и коэффициент распределения будет являться функцией только одной переменной 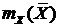 .
.
Рассмотрим выбор схемы относительного направления движения фаз. Пусть заданы: расход инертного газа G, начальная и конечная концентрация абсорбтива в нем 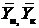 , а также начальная концентрация абсорбтива в абсорбенте
, а также начальная концентрация абсорбтива в абсорбенте 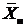 . Допустим, что коэффициент распределения
. Допустим, что коэффициент распределения 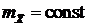 , то есть линия равновесия
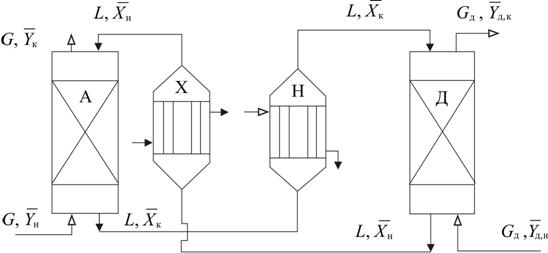
, то есть линия равновесия  прямая. Это допущение справедливо для идеальных смесей, подчиняющихся законам Генри (12.59) или Рауля (12.53), при постоянных температуре и давлении. Проведение процесса абсорбции требует выполнение условия
прямая. Это допущение справедливо для идеальных смесей, подчиняющихся законам Генри (12.59) или Рауля (12.53), при постоянных температуре и давлении. Проведение процесса абсорбции требует выполнение условия 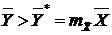 . Определим минимальные расходы абсорбента
. Определим минимальные расходы абсорбента 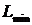 и максимальные конечные концентрации абсорбтива в абсорбенте
и максимальные конечные концентрации абсорбтива в абсорбенте 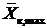 для прямотока и противотока. Проведем на
для прямотока и противотока. Проведем на 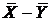 диаграмме равновесную линию, а также из точек с известными координатами
диаграмме равновесную линию, а также из точек с известными координатами 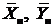 (прямоток) и
(прямоток) и 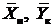 (противоток) рабочие линии, соответствующие
(противоток) рабочие линии, соответствующие 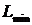 (рис.13.1), то есть соприкаса-ющиеся с линией равновесия.
(рис.13.1), то есть соприкаса-ющиеся с линией равновесия.
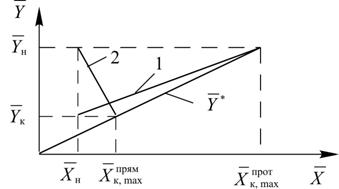
Рис. 13.1. Расположение рабочих линий при минимальном расходе абсор-бента для противоточного 1 и прямоточного 2 движения фаз
Нетрудно видеть, что использование противотока позволяет достигать больших конечных концентраций абсорбтива в абсорбенте и, как следует из уравнения материального баланса (13.1), применять меньшие значения расхода абсорбента L. Этот же результат можно получить аналитически
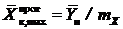 , (13.5)
, (13.5)
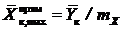 , (13.6)
, (13.6)
т.к. 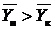 , то
, то
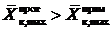 , (13.7)
, (13.7)
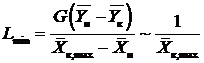 ,
, 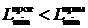 . (13.8)
. (13.8)
Эффективность работы массообменного аппарата может быть охарактеризована степенью извлечения распределяемого компонента из отдающей его фазы. Вводится понятие коэффициента извлечения j, являющегося отношением количества компонента перешедшего в другую фазу к максимально возможному. Наибольшее количество абсорбтива может поглотиться абсорбентом при достижении равновесия уходящего газа с поступающей жидкостью, т.е. 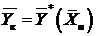 . Тогда
. Тогда
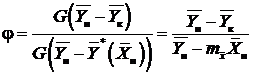 . (13.9)
. (13.9)
Можно показать [49], что в случае идеального вытеснения и 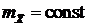 для одинаковых L и
для одинаковых L и 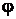 средняя движущая сила массопередачи
средняя движущая сила массопередачи 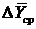 больше, а высота аппарата, следовательно, меньше при противотоке по сравнению с прямотоком, или для одинаковых L и
больше, а высота аппарата, следовательно, меньше при противотоке по сравнению с прямотоком, или для одинаковых L и 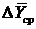 при противотоке
при противотоке 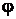 больше, чем при прямотоке. Этим объясняется преимущественное применение противоточного движения фаз в процессе абсорбции.
больше, чем при прямотоке. Этим объясняется преимущественное применение противоточного движения фаз в процессе абсорбции.
Увеличение движущей силы массопередачи при проведении процесса абсорбции можно достичь также уменьшением коэффициентов распределения 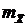 . При абсорбции паровых компонентов, как это следует из (12.52), для этого необходимо увеличивать давление в системе p или уменьшать температуру T так как давление насыщенного пара
. При абсорбции паровых компонентов, как это следует из (12.52), для этого необходимо увеличивать давление в системе p или уменьшать температуру T так как давление насыщенного пара 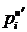 прямо пропорционально температуре. Такой же вывод можно сделать и для газовых компонентов, анализируя (12.59), так как коэффициенты Генри
прямо пропорционально температуре. Такой же вывод можно сделать и для газовых компонентов, анализируя (12.59), так как коэффициенты Генри 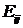 также, как правило, прямо пропорциональны температуре.
также, как правило, прямо пропорциональны температуре.
В том случае, когда при растворении абсорбтива в абсорбенте выделяется значительное количество теплоты и не предусмотрен ее отвод из аппарата, происходит повышение температуры жидкой фазы и, следовательно, коэффициента распределения и уменьшение движущей силы процесса. Для учета этого эффекта необходимо использовать уравнение теплового баланса
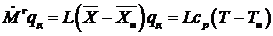 , (13.10)
, (13.10)
где 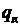
 дифференциальная теплота растворения абсорбтива в абсорбенте, кДж/кг;
дифференциальная теплота растворения абсорбтива в абсорбенте, кДж/кг; 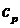
 удельная теплоемкость жидкой фазы, кДж/(кг×К).
удельная теплоемкость жидкой фазы, кДж/(кг×К).
Решив (13.10) относительно T, можно определить температуру, в каждом сечении аппарата, а затем коэффициент распределения 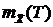 и равновесную концентрацию
и равновесную концентрацию 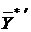 (рис 13.2).
(рис 13.2).
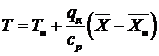 . (13.11)
. (13.11)
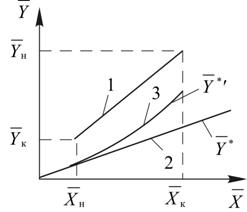
Рис. 13.2. Относительное расположение рабочей линии 1 процесса абсорбции для противотока и равновесных линий при выделении тепла без его отвода 3 и при изотермическом процессе 2
Как видно из рисунка 13.2, выделение теплоты при растворении абсорбтива приводит к уменьшению движущей силы процесса. Чтобы этого избежать, в аппаратах для проведения таких процессов предусматривается отвод тепла с помощью охлаждающего агента.
В процессе хемосорбции абсорбтив вступает в химическое соединение с абсорбентом, образуя новое вещество, следовательно, концентрация распределяемого компонента в жидкой фазе 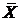 уменьшается. Это приводит к уменьшению равновесной концентрации
уменьшается. Это приводит к уменьшению равновесной концентрации 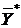 и увеличению движущей силы процесса абсорбции.
и увеличению движущей силы процесса абсорбции.
В зависимости от величины коэффициентов распределения 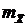 , компоненты газовой смеси условно можно подразделить на хорошо растворимые в абсорбенте (
, компоненты газовой смеси условно можно подразделить на хорошо растворимые в абсорбенте (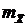
 мал, порядка единицы) и плохо растворимые (
мал, порядка единицы) и плохо растворимые (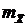
 велик, порядка ста). Очевидно, что для поглощения данного компонента следует подбирать абсорбент, обеспечивающий по возможности лучшее его растворение (меньшее значение
велик, порядка ста). Очевидно, что для поглощения данного компонента следует подбирать абсорбент, обеспечивающий по возможности лучшее его растворение (меньшее значение 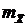 ) и, соответственно большую движущую силу.
) и, соответственно большую движущую силу.
Таким образом, на движущую силу абсорбции влияют вид и расход абсорбента, давление и температура. Они могут служить параметрами оптимизации при проектировании абсорберов.
Анализ соотношения (12.83) позволяет сделать вывод, что для хорошо растворимых компонентов, как правило, 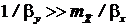 и
и 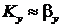 т.е. основное сопротивление массопередачи сосредоточенно в газовой фазе, а для плохо растворимых
т.е. основное сопротивление массопередачи сосредоточенно в газовой фазе, а для плохо растворимых 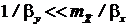 ,
, 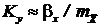
 в жидкой. Разумеется, при этом необходимо учитывать и соотношение коэффициентов массоотдачи в газовой и жидкой фазах.
в жидкой. Разумеется, при этом необходимо учитывать и соотношение коэффициентов массоотдачи в газовой и жидкой фазах.
Десорбция
Десорбция применяется преимущественно для выделения абсорбтива из абсорбента в целях получения его в чистом виде, а также повторного использования абсорбента. Можно выделить два вида десорбции: с применением десорбирующего агента и без него.
Десорбция с применением десорбирующего агента. Этот вид десорбции описывается соотношениями, аналогичными рассмотренными в предыдущем разделе. Отличие заключается лишь в обратном по сравнению с абсорбцией направлении проведении процесса, что обеспечивается в случае бинарной смеси условием 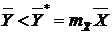 . Обозначим расход десорбирующего агента, не поглощающегося абсорбентом,
. Обозначим расход десорбирующего агента, не поглощающегося абсорбентом, 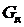 , а начальную и конечную концентрации абсорбтива в нем
, а начальную и конечную концентрации абсорбтива в нем 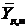 и
и 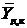 (рис. 13.4).
(рис. 13.4).
Тогда уравнения материального баланса и рабочей линии процесса десорбции примут вид.
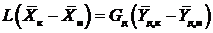 , (13.12)
, (13.12)
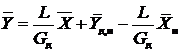 . (противоток) (13.13)
. (противоток) (13.13)
В отличие от абсорбции, при десорбции рабочая линия (13.13) должна располагаться ниже линии равновесия (рис. 13.3). В этом случае находится минимальный расход десорбирующего агента 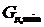 , обеспечивающий процесс десорбции и соответствующее ему значение
, обеспечивающий процесс десорбции и соответствующее ему значение 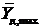 . Для увеличения движущей силы процесса десорбции следует увеличивать коэффициент распределения, т.е. повышать температуру или понижать давление. Поэтому в схеме, изображенной на рис. 13.4 предусмотрен нагреватель Н.
. Для увеличения движущей силы процесса десорбции следует увеличивать коэффициент распределения, т.е. повышать температуру или понижать давление. Поэтому в схеме, изображенной на рис. 13.4 предусмотрен нагреватель Н.
Рис. 13.3. Расположение равновесной 1 и рабочих линий в процессе десорбции при минимальном расходе десорбирующего агента  2 и
2 и 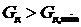
 3
3
Сочетание абсорбции с десорбцией или перегонкой позволяет многократно использовать поглотитель, выделяя из него абсорбтив.
Рис. 13.4. Схема абсорбционной установки с регенерацией абсорбента путем десорбции с десорбирующим агентом: А  абсорбер; Н
абсорбер; Н  нагреватель; Д
нагреватель; Д  десорбер; Х
десорбер; Х  холодильник.
холодильник.
В том случае, когда распределяемый компонент не представляет ни ценности, ни опасности для окружающей среды в качестве десорбирующего агента может использоваться воздух (инертный газ), отводимый вместе с распределяемым компонентом в атмосферу. Если же абсорбтив требуется выделить в чистом виде, то в качестве десорбирующего агента часто применяют водяной пар, при условии возможности достаточно простого последующего отделения его от абсорбтива за счет конденсации. Абсорбтив должен не конденсироваться, либо не смешиваться с водой в жидком состоянии.
Десорбция без применения десорбирующего агента. Этот способ осуществляется за счет снижения давления в аппарате и применим для отделения абсорбтива от практически нелетучего абсорбента. Особо часто его используют, если абсорбция проходит при повышенных давлениях.
Снижениe давления смещает равновесие и распределяемый компонент переходит из жидкой фазы в газовую. При условии нелетучести абсорбента газовая фаза будет состоять только из распределяемого компонента, его мольная доля 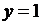 , и применение относительной массовой концентрации
, и применение относительной массовой концентрации 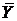 теряет смысл. В этом случае удобнее описывать процесс массопередачи с использованием объемных мольных концентраций c (кмоль/м3) распределяемого компонента в газовой
теряет смысл. В этом случае удобнее описывать процесс массопередачи с использованием объемных мольных концентраций c (кмоль/м3) распределяемого компонента в газовой 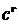 и жидкой
и жидкой 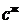 фазах. При фиксированном давлении в десорбере
фазах. При фиксированном давлении в десорбере 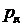 (МИС по газовой фазе) величина
(МИС по газовой фазе) величина 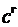 также будет постоянной, как это следует из уравнения состояния при
также будет постоянной, как это следует из уравнения состояния при 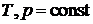 . Уравнение равновесия примет вид
. Уравнение равновесия примет вид
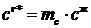 . (13.14)
. (13.14)
Концентрации абсорбтива в жидкой фазе в процессе десорбции будет изменяться от 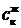 до
до 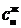 (рис.13.5).
(рис.13.5).
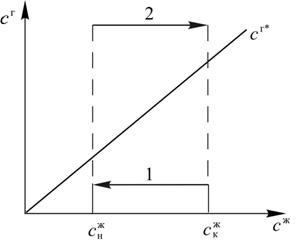
Рис. 13.5. Растворение чистого газа в жидкости  2 и десорбции без применения десорбирующего агента за счет снижения давления
2 и десорбции без применения десорбирующего агента за счет снижения давления  1
1
Таким образом, рабочая линия процесса десорбции будет изображаться на 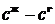 диаграмме горизонтальной прямой 1. Все сопротивление массопередачи в данном случае будет сосредоточенно в жидкой фазе.
диаграмме горизонтальной прямой 1. Все сопротивление массопередачи в данном случае будет сосредоточенно в жидкой фазе.
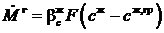 ,
, 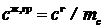 . (13.15)
. (13.15)
Десорбцию в данном случае можно рассматривать как процесс обратный растворению чистого газа в жидкости (частный случай абсорбции из однокомпонентной газовой фазы). Рабочая линия процесса растворения также будет изображаться горизонтальной прямой, но располагаться выше линии равновесия. Давление в процессе растворения должно быть больше, чем при десорбции 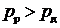 . Необходимо отметить, что коэффициент
. Необходимо отметить, что коэффициент 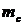 в отличие от
в отличие от 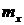 практически не зависит от давления.
практически не зависит от давления.
Кроме рассмотренных способов десорбции отделение абсорбтива от абсорбента может осуществляться простой перегонкой или ректификацией, речь о которых пойдет в следующей главе.
 2018-01-21
2018-01-21 1843
1843