Полимер – высокомолекулярное соединение, состоящее из повторяющихся звеньев, элементарных единиц – мономеров.
Белки – биополимеры, мономерами которых являются аминокислоты.
Аминокислоты – низкомолекулярные соединения
Аминокислоты
Из аминокислот построены молекулы белков. В тканях и клетках встречается свыше 170 различных аминокислот, но обычными компонентами белков можно считать лишь 20 аминокислот.
Растения синтезируют все необходимые им аминокислоты из более простых веществ. В отличие от них животные не способны синтезировать все аминокислоты, в которых они нуждаются; часть аминокислот они должны получать в готовом виде, т. е. с пищей. Эти последние принято называть незаменимыми аминокислотами; другие необходимые организму животных аминокислоты могут быть синтезированы из них. Следует, однако, подчеркнуть: название «незаменимые» вовсе не означает, что эти аминокислоты в качестве компонентов животных клеток в чем-то важнее остальных. «Незаменимы» они лишь в том смысле, что организм животного не способен их синтезировать.
Аминокислоты:
· заменимые – те, что организм может синтезировать самостоятельно
· незаменимые – необходимо получать вместе с пищей.
Строение аминокислот. Классификация аминокислот.
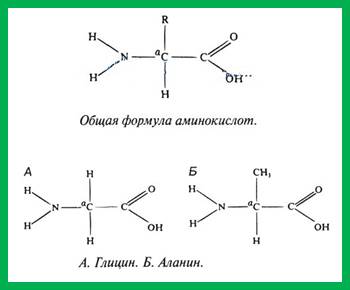
Общая формула аминокислот приведена на рисунке. В молекуле аминокислоты к центральному атому углерода всегда присоединена одна кислотная группа, — СООН (карбоксильная), одна основная —NH2 (аминогруппа) и один атом водорода. Варьирует только остальная часть молекулы — R-гpynna. Ее строение у разных аминокислот различается весьма сильно, и именно она определяет уникальные свойства каждой отдельной аминокислоты.
В простейшей аминокислоте глицине роль R играет атом водорода Н. У аланина эту роль выполняет группа — СН3.
Физические свойства аминокислот: бесцветные, кристаллические, растворимы в воде, нерастворимы в органических растворителях.
Амфотерность аминокислот.
Соединения, которые подобно аминокислотам содержат в своей молекуле как основную, так и кислотную группы, называют амфотерными. Они существуют главным образом в виде ионов, у которых основная часть несет положительный заряд, а кислотная — отрицательный. Это так называемые биполярные ионы. Амфотерность объясняет способность аминокислот и белков перемещаться в электрическом поле, что используется, например, для их разделения методов электрофореза. Заряд аминокислоты может изменяться под влиянием среды. Так, при подкислении раствора, с возрастанием концентрации ионов водорода, растет и положительный заряд аминокислоты, отрицательный же соответственно нейтрализуется.
 2017-11-01
2017-11-01 2147
2147