Окислительная способность оксокислот хлора связана с возможностью понижения степени окисления в анионе кислоты HXOn, n = 1,2,3,4. С термодинамической точки зрения закономерности изменения окислительной способности, как и стабильности, оксокислот хлора удобно проанализировать с помощью диаграммы окислительных состояний (рис.6).
1.Все oксокислоты являются сильными окислителями, о чем свидетельствует положительный наклон линий, соединяющих вольт-эквиваленты (энергии Гиббса) окисленных и восстановленных форм на рис.6.
2. Их окислительная способность соответствует следующей последовательности: Cl2 < HClO 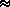 HClO2 >HClO3 > HClO4, что отвечает наклонам линий для пар 1/2
HClO2 >HClO3 > HClO4, что отвечает наклонам линий для пар 1/2 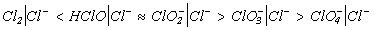 . Например, раствор соли NaClO окисляет
. Например, раствор соли NaClO окисляет 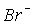 до Br2 в кислой, нейтральной и щелочной средах:
до Br2 в кислой, нейтральной и щелочной средах:
NaClO + 2KBr + H2O = NaCl +Br2 +2KOH ( в щелочной среде происходит дальнейшее окисление Br2 до 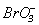 ).
).
C помощью NaClO3 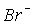 окисляется только в кислой среде:
окисляется только в кислой среде:
NaClO3+ 6KBr +3H2SO4 = 3Br2 + NaCl + 3K2SO4 + 3Н2О.
3. С увеличением рН = -lg[H+] окислительная способность уменьшается. Например, для реакции
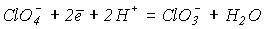

в соответствии с уравнением Нернста
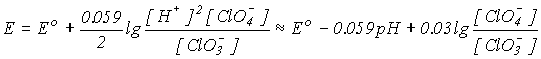 .
.
величина потенциала уменьшается от Ео = 1.02 В при рН = 0 до Ео = +0.37 при рН=14. Таким образом, окислительная способность солей ниже, чем соответствующих кислот.
С точки зрения кинетики для сопоставления окислительной способности кислот и оксоанионов хлора необходимо рассмотреть особенности механизма реакций. Изменение степени окисления может происходить двумя способами:
- путем прямого переноса электронов между молекулярными орбиталями окислителя и восстановителя без изменений в строении анионов;
- путем переноса отдельных атомов или групп атомов.
Оба варианта описания равноправны. С точки зрения метода молекулярных орбиталей (ММО) при этом важен факт перехода электронов с несвязывающих орбиталей на связывающие и наоборот (В случае комплексных соединений переходных металлов возможен переход электронов между несвязывающими орбиталями). В любом случае для осуществления окислительно-восстановительной реакции сначала должен быть установлен контакт между частицами - канал, по которому может произойти переход электронов от восстановителя на свободные молекулярные орбитали окислителя.
В качестве примера присоединения атомной группировки, сопровождающегося переносом электронов (способ 2), рассмотрим механизм окисления сульфит-иона 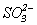 хлорноватистой кислотой HClO. Результаты ( K.D.Fogelman, D.M.Walker, D.W.Margerum. Inorg.Chem, 1989, V.28, P.986-993) изучения скорости реакции показывают, что первый медленный этап - нуклеофильное (Нуклеофильные (от латинского слова "нуклеус" - ядро) частицы - частицы со свободной электронной парой, стремящиеся к остову (ядру) другой частицы, имеющей пустую орбиталь) присоединение к атому хлора иона
хлорноватистой кислотой HClO. Результаты ( K.D.Fogelman, D.M.Walker, D.W.Margerum. Inorg.Chem, 1989, V.28, P.986-993) изучения скорости реакции показывают, что первый медленный этап - нуклеофильное (Нуклеофильные (от латинского слова "нуклеус" - ядро) частицы - частицы со свободной электронной парой, стремящиеся к остову (ядру) другой частицы, имеющей пустую орбиталь) присоединение к атому хлора иона 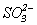 , в котором имеются два электрона на разрыхляющей орбитали. При этом образуется хлоросульфат-ион
, в котором имеются два электрона на разрыхляющей орбитали. При этом образуется хлоросульфат-ион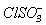 :
:
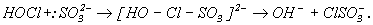 (1)
(1)
В промежуточном комплексе (интермедиате) хлор выступает как мостик между HO-- и 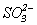 . Вторая стадия - гидролиз хлоросульфата - протекает быстро:
. Вторая стадия - гидролиз хлоросульфата - протекает быстро:
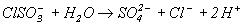 (2).
(2).
Скорость реакции (1) определяется доступностью атома хлора для нуклеофильной атаки. В ряду Cl2 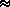 HClO < HClO2 < HClO3 < HClO4 увеличивается экранирование хлора атомами кислорода, а значит, и уменьшается скорость реакции, где указанные молекулы или ионы выступают как окислители. Это интересный факт, поскольку в рассматриваемом ряду окислительная способность уменьшается как с точки зрения термодинамики, так и с позиций кинетики.
HClO < HClO2 < HClO3 < HClO4 увеличивается экранирование хлора атомами кислорода, а значит, и уменьшается скорость реакции, где указанные молекулы или ионы выступают как окислители. Это интересный факт, поскольку в рассматриваемом ряду окислительная способность уменьшается как с точки зрения термодинамики, так и с позиций кинетики.
Следует также отметить, что скорость реакций, в которых оксоанионы действуют как окислители, ускоряется ионами водорода. Это связано с протонированием атомов кислорода в оксоанионе и ослаблением связи Cl-O, а также с увеличением электрофильности (электрофильная частица - частица с пустой орбиталью, которая стремится к остову другой частицы, имеющей свободную электронную пару) хлора по отношению к восстановителю, несущему электроны. Действительно, концентрированная HClO4, особенно в смеси с H2SO4, действует как сильный окислитель и взрывается в присутствии следов органических соединений (например, при попадании пыли).
 2014-01-31
2014-01-31 942
942








