Что такое ядерные реакции и чем они отличаются от химических, чем определяются химические и ядерно-физические свойства вещества?
Химические реакции связаны с перестройкой электронных оболочек атомов и приводят к образованию новых молекул (объединений атомов), но не новых элементов. А вот в результате ядерных реакций могут появляться новые виды ядер и атомов, т.е. новые химические элементы, так как в таких реакциях происходит взаимодействие ядер с элементарными частицами или с другими ядрами.
Следовательно,химические свойства элемента зависят от заполнения электронных оболочек атома, а именно – от количества электронов внешней оболочки. Оно, в свою очередь, определяется общим количеством электронов в атоме, и, следовательно, порядковым номером в таблице Д.И. Менделеева. Отсюда следует, что изотопы одного и того же элемента имеют одинаковые химические свойства. При этом их ядерно-физические свойства, определяемые строением ядра (стало быть, количеством нейтронов), могут быть совершенно непохожими. Например, весьма по-разному проявляют себя в активной зоне реактора обычная легкая вода H2O и тяжелая вода D2O. Легководный реактор на природном уране неосуществим, а тяжеловодный не только возможен, но и экономически целесообразен, так как поглощение нейтронов дейтерием намного меньше, чем легким водородом.
Рассмотрим возможные виды ядерных реакций. Для этого вернемся к дефекту массы и энергии связи нуклонов в ядре.
Возьмем конкретный пример. Атом углерода-12 состоит из 6 протонов, 6 нейтронов и 6 электронов. Это записывается следующим образом: 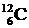 (6 p, 6 n, 6 e).
(6 p, 6 n, 6 e).
Масса природного атома углерода-12 составляет ровно 12 а.е.м., поскольку он является эталонным. Суммарная же масса составляющих его 18 частиц равна 12,098940 а.е.м., что можно определить с помощью данных, приведенных в таблице 1.1. Таким образом, дефект массы данного атома составляет 0,098940 а.е.м. Это говорит о том, что энергетически выгодно было бы «собирать» атомы углерода-12 из протонов, нейтронов и электронов – если бы, конечно, у нас был «склад» этих частиц.
Разумеется, его нет. Но вполне возможны реакции, в которых происходит превращение одних ядер в другие с выделением энергии. Такие ядерные реакции называются экзотермическими (или экзоэнергетическими). Они возможны, если сумма дефектов масс продуктов реакции превышает сумму дефектов масс исходных компонентов. В противном случае реакция будет эндотермической (эндоэнергетической), и для ее осуществления необходим подвод энергии извне.
Необходимо подчеркнуть, что средняя энергия связи нуклонов в ядре составляет несколько МэВ. Это намного больше энергии связи электронов в атоме, которая колеблется от 1 до 10 эВ.
Отсюда следуют два вывода:
- величины дефекта массы для атома и для ядра этого же атома практически совпадают;
- ядерные источники энергии в миллионы раз более энергоемки, чем горючие ископаемые.
Если проанализировать приведенную на рис. 2.1 кривую зависимости средней энергии связи нуклонов от массового числа, то можно выделить два вида экзотермических ядерных реакций. При массовом числе не более 50-60 энергетически выгодна реакция синтеза, т.е. слияния исходных ядер с образованием новых, например:
 +
+  = 2
= 2 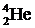 + Q,
+ Q,
где Q – теплота, выделяемая в реакции.
Наоборот, для ядер с массовым числом более 60 выделение энергии будет происходить в реакции деления, а не синтеза, например:
 +
+ 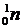 =
=  * =
* =  +
+  + 2
+ 2 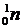 + Q.
+ Q.
Здесь приведен один из вариантов деления урана-235 при поглощении им нейтрона – с образованием двух осколков деления (лантан и бром) и испусканием двух новых нейтронов, называемых нейтронами деления. При других каналах данной реакции возможно появление иных осколков и какого-либо числа нейтронов деления (необязательно двух). Верхний индекс (*) у урана-236 означает неустойчивость (радиоактивность) данного нуклида.
Если деление ядра происходит самопроизвольно, без бомбардировки его какими-либо другими частицами, то такой процесс считается одним из видов радиоактивного распада вещества.
Энергия, выделяемая в результате синтеза, деления ядер или радиоактивного распада, называется ядерной или атомной энергией.
Сравним удельную (на единицу массы реагирующих веществ) энергетическую эффективность химических и ядерных реакций.
Выделение энергии в какой-либо реакции связано с преобразованием некоторой части энергии покоя частиц в кинетическую энергию их движения.
При химическом взаимодействии веществ происходит перестройка внешних электронных оболочек атомов, и за счет этого в экзотермической химической реакции возможно преобразование в кинетическую энергию примерно одной десятимиллиардной доли (10-10) энергии покоя молекул или атомов.
В ядерных реакциях освобождается энергия, составляющая 10-4÷10-3 энергии покоя ядра, причем удельная энергетическая эффективность реакций синтеза легких ядер в несколько раз больше, чем реакций деления тяжелых ядер (таблица 2.2). По этой причине реакции синтеза стали называть термоядерными, а реакции деления – просто ядерными.
Для ясности еще раз подчеркнем, что термоядерные реакции – это одна из разновидностей ядерных реакций («ядерных» в широком смысле слова), а ядерные реакции деления именуются таковыми в узком смысле слова «ядерные».
Таблица 2.2
Удельная энергетическая эффективность
химических, ядерных и термоядерных реакций
| Вид реакции | Уравнение реакции (левая часть) | Удельное энерговыделение, ккал/г |
| Химическая реакция | C + O2 | 7 |
| Ядерная реакция деления |  + + 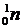
| 19700000 |
| Термоядерная реакция синтеза |  + + 
| 65000000 |
3. РАДИОАКТИВНОСТЬ, ЗАКОН РАДИОАКТИВНОГО РАСПАДА
Все известные ядра можно разделить на две группы – стабильные (устойчивые) и нестабильные (неустойчивые), называемые также радиоактивными.
Одной из причин неустойчивости ядер, т.е. их радиоактивности, является отклонение соотношения числа протонов и нейтронов от равновесного значения, необходимого для стабильности ядра. Следовательно, в таких радиоактивных ядрах имеется излишек одного из видов нуклонов - нейтронов или протонов - по сравнению с устойчивыми ядрами того же химического элемента.
Причиной такого отклонения может быть, в частности, повышение относительной доли нейтронов (в суммарном числе нуклонов ядра) с увеличением порядкового номера элемента в таблице Д.И. Менделеева. Большее число нейтронов необходимо для компенсации кулоновских сил отталкивания протонов, нарастающих с увеличением заряда ядра.
Действительно, в легких стабильных ядрах наблюдается примерное равенство количества протонов и нейтронов (например, 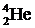 ,
,  ,
, 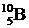 ,
, 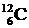 и др.), но с возрастанием массового числа положение начинает изменяться – нейтронов в ядрах становится все больше по сравнению с числом протонов. В ядре последнего (т.е. самого тяжелого) стабильного изотопа, а это
и др.), но с возрастанием массового числа положение начинает изменяться – нейтронов в ядрах становится все больше по сравнению с числом протонов. В ядре последнего (т.е. самого тяжелого) стабильного изотопа, а это  (висмут), количество нейтронов более чем в полтора раза превышает количество протонов. Заметим, кстати, что число нейтронов в этом ядре является магическим – 126, благодаря чему оно и стабильно.
(висмут), количество нейтронов более чем в полтора раза превышает количество протонов. Заметим, кстати, что число нейтронов в этом ядре является магическим – 126, благодаря чему оно и стабильно.
Изотопы всех химических элементов с порядковым номером больше 83 неустойчивы, поскольку при таком количестве протонов ядерные силы уже не могут компенсировать кулоновское отталкивание.
Другой причиной нестабильности нуклида может быть его энергетическое состояние, требующее сброса излишней энергии путем испускания излучения.
Радиоактивность
Под радиоактивностью понимается свойство вещества претерпевать радиоактивный распад, т.е. любые самопроизвольные (спонтанные) превращения атомного ядра, связанные с изменением его заряда, массы или энергетического состояния. Радиоактивностью называют также само явление спонтанного испускания веществом потока какого-либо излучения, имеющего ядерное происхождение.
При радиоактивном распаде исходное ядро называют материнским, а конечное – дочерним. В результате распада получается новый нуклид, который по своим свойствам отличается от начального.
Очевидно, что самопроизвольный распад ядра возможен только в том случае, когда масса материнского ядра превышает суммарную массу дочернего ядра и всех частиц, испускаемых в результате распада. Это необходимо для энергетической возможности процесса, исходя из формулы Эйнштейна. Отсюда следует, что спонтанный радиоактивный распад ядер необратим.
При радиоактивном распаде выполняются законы сохранения энергии, электрического заряда, числа нуклонов, импульса. Закон сохранения энергии здесь означает равенство энергии исходного ядра и энергии продуктов распада. В процессе распада часть энергии покоя материнского ядра преобразуется в кинетическую энергию дочернего ядра и энергию испускаемого излучения.
Радиоктивные ядра могут быть естественными (природными) и искусственными.
Сначала и более подробно поговорим об естественной радиоактивности.
Естественные радиоактивные изотопы (всего их известно около 50-ти) содержатся в природных минералах, почве, воде, воздухе, в растениях и животных, в теле человека - другими словами, повсюду.
Радиоактивный распад естественных изотопов происходит и во всей толще Земли. Именно этот процесс является первопричиной очень высокой температуры (порядка 4000 оС) в ее центре. Отвод к поверхности нашей планеты (и далее в космическое пространство) энергии, выделяющейся в результате ядерных превращений, весьма затруднен из-за очень низкой скорости передачи теплоты на огромные расстояния от центра Земли к ее верхним слоям.
Радиоактивный распад естественного нуклида необязательно приводит сразу к образованию стабильного ядра. Возможно последовательное превращение одних ядер в другие, прежде чем появится устойчивый изотоп, и, тем самым, цепочка радиоактивного распада закончится.
При радиоактивном распаде естественные радионуклиды испускают α- и β-частицы, а также γ-излучение. Поскольку изменение массового числа возможно при этом лишь в результате альфа-распада и только в сторону уменьшения на 4 единицы, должно существовать четыре природных цепочки ядер, получающихся при радиоактивном распаде. Их называют естественными радиоактивными семействами (рядами), каждое из них содержит от 11 до 15 элементов. Свои названия семейства получили по начальному изотопу в цепочке распада (таблица 3.1). Все четыре таких изотопа принадлежат к группе актиноидов в таблице Д.И. Менделеева и являются альфа-радиоактивными.
Таблица 3.1
Естественные радиоактивные семейства
| Название радиоактивного семейства | Первый изотоп в цепочке радиоактивного распада | Конечное стабильное ядро | |
| Нуклид | Т 1/2, лет | ||
| Семейство тория | 
| 13,9 млрд | 
|
| Семейство актиния | 
| 0,713 млрд | 
|
| Семейство урана | 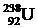
| 4,51 млрд | 
|
| Семейство нептуния (вымершее) | 
| 0,0022 млрд | 
|
Радиоактивное семейство нептуния было получено искусственным путем, а семейства тория, актиния и урана сохранились в природе до настоящего времени, так как периоды полураспада Т 1/2 титульных элементов этих трех радиоактивных рядов сопоставимы с временем существования нашей планеты, составляющим по оценкам ученых примерно 4,5 млрд лет.
Из сравнения периодов полураспада естественных нуклидов урана и тория с временем жизни Земли становится понятным, почему в природном уране содержание столь нужного нам изотопа  (~ 0,71%) сейчас намного меньше, чем
(~ 0,71%) сейчас намного меньше, чем 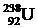 (~ 99,29%), а запасы тория, в свою очередь, значительно превышают имеющиеся на планете ресурсы всего урана.
(~ 99,29%), а запасы тория, в свою очередь, значительно превышают имеющиеся на планете ресурсы всего урана.
Некоторые наиболее тяжелые природные изотопы способны не только претерпевать распад с испусканием каких-либо частиц, но и спонтанно делиться на два новых ядра, однако вероятность деления весьма невелика по сравнению с первым исходом. Например, на каждые два миллиона случаев альфа-распада ядра урана-238 приходится только одно деление. С учетом известного периода полураспада это означает, что в 1 кг данного изотопа происходит примерно 7 делений за одну секунду.
Искусственные радиоактивные изотопы (их получено уже около 1500) можно создать двумя основными способами – путем бомбардировки (облучения) ядер какими-либо частицами (например, в ускорителях элементарных частиц) или в результате переработки использованного ядерного топлива после его выгрузки из активной зоны реактора.
Впервые в мире искусственный радиозотоп получили Ирен и Фредерик Жолио-Кюри во Франции в 1934 г. – это был радиоактивный фосфор, появившийся при облучении ядер алюминия альфа-частицами.
Еще раз подчеркнем, что в настоящее время подавляющее большинство известных радиоактивных изотопов составляют радионуклиды, полученные искусственным путем. В таблице 3.2 приведены сведения о некоторых естественных и искусственных радиоизотопах, которые наиболее интересны с практической точки зрения.
Таблица 3.2
Характеристики радиоактивного распада некоторых изотопов
| Изотоп | Вид распада | Т 1/2 | Энергия распада, МэВ |
 (тритий) (тритий)
| β | 12,3 лет | 0,019 |
 (углерод-14) (углерод-14)
| β | 5730 лет | 0,156 |
 (кобальт-60) (кобальт-60)
| β γ | 5,3 лет | 0,314 1,173; 1,332 |
 (стронций-90) (стронций-90)
| β | 27,7 лет | 0,546 |
 (иод-131) (иод-131)
| β | 8,05 суток | 0,606 |
 (радий-226) (радий-226)
| α | 1602 года | 4,78 |
 (уран-234) (уран-234)
| α | 248 тыс. лет | 4,75 |
 (уран-235) (уран-235)
| α | 713 млн лет | 4,40 |
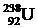 (уран-238) (уран-238)
| α | 4,51 млрд лет | 4,20 |
 (плутоний-239) (плутоний-239)
| α | 24390 лет | 5,16 |
Из данных этой таблицы видно, что плутония-239 в земной коре практически не осталось, но если его получить искусственным путем сейчас, то он может храниться многие сотни лет без какого-либо заметного уменьшения (вследствие радиоактивного распада) своего количества во время хранения.
 2018-03-09
2018-03-09 1141
1141
