При выборе материалов для изготовления различного рода изделий, использующихся в широком диапазоне условий эксплуатации, необходима оценка их физико-химических, механических и технологических свойств и возможностей изменения последних. Рациональный подход к такой оценке дают знание диаграмм фазового равновесия и умение их анализировать.
К настоящему времени изучено около 10 тыс. диаграмм состояния двойных систем, и число их продолжает расти.
Цель практической работы — изучение основных типов диаграмм фазового равновесия реальных двойных систем, приобретение практических навыков их использования для изучения превращений, происходящих в сплавах, анализа и расчета фазового состава и состава твердых растворов системы при заданной температуре.
Термины и определения
Диаграмма фазового равновесия (диаграмма состояния) — графическое изображение соотношения между параметрами состояния (температурой, давлением, составом) термодинамически равновесной системы, т.е. фазового состояния любого сплава изучаемой системы компонент в зависимости от его концентрации.
Компонент — составная часть, в данном случае химический элемент, образующий сплав.
Конода — горизонтальный отрезок, концы которого ограничены равновесными сосуществующими фазами и содержанием в них компонентов; характеризует состав фаз, находящихся в равновесии.
Ликвидус — геометрическое место точек начала затвердевания бинарных сплавов с различным содержанием компонентов на диаграмме состояния.
Линии фигуративных точек — вертикальные линии на диаграмме состояния, соответствующие определенному химическому составу сплава.
Линия предельной растворимости — линия на диаграмме состояния бинарных сплавов, характеризующая изменение растворимости компонента с
изменением температуры.
Перитектика — структурная составляющая сплава, представляющая собой механическую смесь фаз, образующуюся за счет ранее выделившейся твердой фазы и закристаллизовавшейся жидкой части сплава определенного состава.
Раствор твердый — однофазный в твердом состоянии сплав, в котором соотношение компонент может быть переменным и один из компонентов (растворитель) сохраняет свою кристаллическую решетку, а атомы другого (или других) компонента располагаются в решетке этого компонента, изменяя ее размеры (периоды решетки).
Система (гетерогенная) — макроскопически неоднородная термодинамическая система, состоящая из различных по физическим свойствам или химическому составу частей (фаз).
Соединение химическое — фаза, кристаллическая решетка которой отличается от решеток компонентов, ее образующих. Вхимическом соединении всегда сохраняется простое кратное соотношение компонентов А m В n, где т и n — простые числа.
Солидус — на диаграмме состояния геометрическое место точек конца затвердевания бинарных сплавов с различным содержанием компонентов.
Составляющая структурная — часть сплава (однофазная или многофазная), имеющая характерную (однообразную) структуру и отделенная от остальных частей сплава поверхностями раздела.
Состав фазовый — количественная характеристика содержания в материале различных фаз.
Состав химический — количественная характеристика содержания в материале химических элементов.
Строение — совокупность устойчивых связей вещества, обеспечивающих его целостность и тождественность самому себе, т.е. сохранение основных свойств.
Микроструктура — форма, размеры, количество и характер взаимного распределения фаз гетерогенной системы, наблюдаемые с помощью оптического или электронного микроскопа.
Точки фигуративные — точки на диаграмме состояния, определяющие фазовый и химический состав системы при заданной температуре.
Фаза — термодинамически равновесное состояние вещества, характеризующееся агрегатным состоянием, атомным (молекулярным) составом и строением, а также отделенное пространственными границами от других возможных равновесных состояний (фаз) того же вещества.
Эвтектика — структурная составляющая сплава, представляющая собой механическую смесь фаз, образующуюся при одновременной кристаллизации двух (или более) фаз из расплава.
Эвтектоид — структурная составляющая сплава, представляющая собой механическую смесь фаз, образующуюся при одновременной вторичной кристаллизации двух (или более) фаз из твердого раствора.
Основы теории
1.1 Способ и условия построения диаграмм фазового равновесия
Для построения диаграмм фазового равновесия используют термический анализ. Для этой цели экспериментально получают кривые охлаждения отдельных сплавов и по их перегибам или остановкам, связанным с тепловыми эффектами превращений, определяют температуры соответствующих превращений. Эти температуры называют критическими точками. для количественного и качественного изучения этих превращений в твердом состоянии используют различные методы физико-химического анализа: микроанализ, рентгеноструктурный, магнитный и др.
Как правило, диаграммы фазового равновесия строят в координатах температура — концентрация в процентах по массе или атомных процентах компонента. диаграммы фазового равновесия в удобной графической форме показывают фазовый состав сплава в зависимости от температуры и концентрации компонентов и дают наглядное представление о процессах, происходящих в сплавах системы при нагреве и охлаждении.
Пример построения диаграммы фазового равновесия приводится в разделе “Эвтектическая диаграмма состояния непрерывных твердых растворов”, а для системы “олово — цинк” — в приложении.
1.2 Основные типы диаграмм фазового равновесия
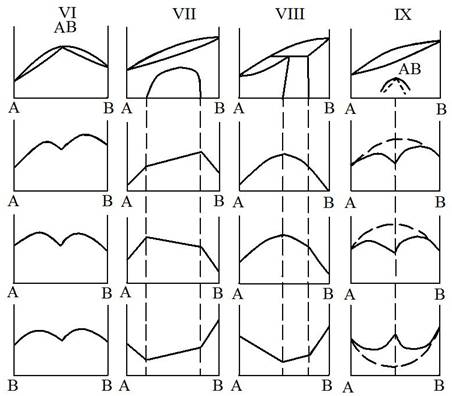
Рассмотрим наиболее распространенные типы диаграмм фазового равновесия (в дальнейшем — диаграмм состояния) бинарных систем, построенных на основе термографического и микроскопического анализов (рис. 1).
диаграммы состояния
непрерывных твердых растворов
Если компоненты А и В по строению электронных оболочек атомов, их радиусам и энергиям химических связей достаточно близки между собой и их замена друг другом не связана с затруднениями структурного и энергетического характера, то обычно возникают непрерывные твердые растворы (рис. 2). Над линией ликвидуса l лежит область расплава L, под линией солидуса s — область твердого раствора S, между ними — область кристаллизации. Рассмотрим особенности кристаллизации систем этого типа (рис. 2, а).
При составе, соответствующем фигуративной точке Ф1, охлаждаем расплав до точки l’. Начинают выпадать кристаллы состава s’. При охлаждении до точки К” выпадут кристаллы s ”, состав расплава отвечает точке l”. По мере охлаждения состав кристаллов изменяется по кривой s’ - s” - s”’, состав расплава — по кривой l’— l“— l’”. Соотношение количества выпавших кристаллов и доли расплава равно отношению отрезков Кl:К s коноды ls. В точке s”’ расплав окончательно кристаллизуется.
В качестве примера диаграмм состояния непрерывных твердых растворов на рис. 2b приведена реальная диаграмма состояния системы
Ag —Аu. Диаграммы состояния непрерывных твердых растворов могут иметь максимум или минимум (рис. 3)
| Температура |
|
| Твердость | |
| Электро-сопротивл. | |
| Температурный коэф. эл.сопротивления |
| Температура |
|
| Твердость | |
| Электро-сопротивл. | |
| Температурный коэф. эл.сопротивления |

| Отожженные сплавы | 
| Закалённые сплавы |
Рис.1. Важнейшие типы диаграмм состояния в бинарных системах (по В.А.Немилову)
|
| |

|
Рис. 2. Диаграммы состояния непрерывных твердых растворов: а – ход кристаллизации в таких системах; б – диаграмма состояния системы Ag —Аu.
|
| ||
|
| ||
Рис.3. Диаграммы состояния непрерывных твердых растворов с максимум или минимумом. Примером первого случая является система Рб – Ti,
примером второго – система Сu – Mn
 2018-03-09
2018-03-09 890
890