При температурах до 2000 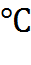 различают три вида состояния вещества: твёрдое, жидкое, газообразное. Состояние вещества можно определить по фазовой диаграмме
различают три вида состояния вещества: твёрдое, жидкое, газообразное. Состояние вещества можно определить по фазовой диаграмме 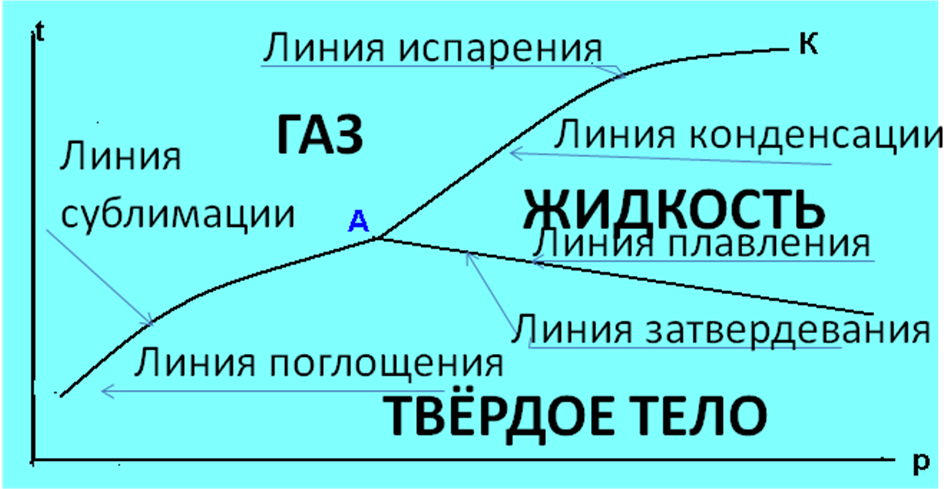
Точка А – тройная точка, в ней вещество находится одновременно в трёх фазах.
Переход вещества из одной фазы в другую происходит при постоянной температуре, при этом в зависимости от направления перехода, происходит или выделение или поглощение тепла. Это тепло называют скрытой теплотой фазового перехода, её значения зависят от температуры и давления.
Если двигаться по линии испарения (конденсации) в сторону увеличения давления, то величина теплоты фазового перехода будет уменьшаться и в точке К станет равной нулю. Эта точка (к) называется критической, а параметры в ней критическими, которые для каждого вещества строго определены и неизменны.
Наличие точки (К) показывает, что между жидкостью и паром нет принципиальных различий.
 2018-02-13
2018-02-13 453
453








