Мы приступаем к изучению основных законов термодинамики, которые принято называть началами.
Эти начала исторически были открыты в одно время. Если первая трактовка 1-го начала дана в 1842году, то 2-е начало было сформулировано в 1850году. С точки зрения физики 1-е начало это закон сохранения энергии в термодинамической форме, а 2-е начало описывает ограничения, накладываемые на закон сохранения термодинамикой.
1-е начало можно сформулировать так: «вечный тепловой двигатель 1-го рода создать нельзя». 2-е начало – «вечный тепловой двигатель 2-го рода создать нельзя» Как видим, формулировки очень похожи.
Таким образом, эти начала неразрывны между собой и, я считаю, что они обязательно должны изучаться совместно.
Кроме того за годы разработки начал произошло наслоение различных определений и выводов.
При изучении этой темы мы сначала рассмотрим качественные аспекты, а к количественной оценке начал перейдём в следующих вопросах. При качественном рассмотрении темы мы почти не будем касаться математических выводов, а ограничимся только историческими и физическими рассуждениями.
В первой половине 19 века наблюдается бурное развитие паровых машин, в то же время теоретические исследования в области термодинамики находились в зачаточном состоянии. Это связано с тем, что не было ответов на следующие вопросы: - что такое теплота; - как в тепловой машине тепло превращается в механическую работу; -куда девается часть подведённого к машине тепла и почему она не участвует в создании работы; -каким образом осуществлять анализ работы тепловых машин, что брать при этом за основу; -какой параметр контролирует теплообмен в тепловой машине.
Первые попытки ответить на поставленные вопросы сделал французский инженер Сади Карно в 1824 году. В своём единственном труде «Размышления о движущей силе огня и о машинах способных развивать эту силу» он сделал следующие выводы: -полезная работа производится при переходе тепла от нагретого тела к более холодному, она обусловлена разностью температур нагревателя и холодильника и не зависит от природы вещества; -любая работа может полностью переходить в тепло, а для получения работы из тепла необходима машина-преобразователь (пример). Карно ввёл понятия: -идеальная тепловая машина; -идеальный цикл тепловой машины; -необратимые термодинамические процессы; -КПД тепловой машины.
Карно считал, что тепловая машина сравнима с гидравлической и отличается от неё только тем, что в ней вместо падения жидкости с высоты, падает температура от высокого значения до низкого. Он предложил схему тепловой машины
| Горячий источник теплоты |
| Рабочее тело |
| Холодный источник теплоты |
Этой схемой пользуются до настоящего времени. Карно доказал, что КПД зависит только от начальной и конечной температуры рабочего тела  . Карно стоит у истоков термодинамики, но после него в течение 20 лет подвижек в теории термодинамики не было, т.к. будущие великие учёные (Джоуль, Ленц, Томсон, Майер, Клаузиус, Геймгольц и др.) ещё не вышли из детского возраста.
. Карно стоит у истоков термодинамики, но после него в течение 20 лет подвижек в теории термодинамики не было, т.к. будущие великие учёные (Джоуль, Ленц, Томсон, Майер, Клаузиус, Геймгольц и др.) ещё не вышли из детского возраста.
Большой вклад в разработку всей термодинамики сделал Джоуль (1818-1889г). Он совместно с Томсоном занялся разработкой теории теплоты. До начала 19-го века учёные считали, что тепло появляется за счёт существования теплорода – тепловой материи в виде невесомой, несжимаемой жидкости, находящейся в телах. Это такое же заблуждение как флогистон – вещество создающее горение или эфир – среда распространения электромагнитных волн. В своей работе Джоуль установил, что теплота связана с мельчайшими частицами вещества и их движением, т.е. теплота – это тепловое движение молекул и атомов. Джоуль и Томсон предположили, что тепловое движение и взаимодействие молекул и атомов составляют внутреннюю энергию тела.
1.5.1. Внутренняя энергия тела.
В технической термодинамике рассматривают преобразование только тепловой энергии и поэтому, внутренняя энергия тела является суммой внутренней кинетической и внутренней потенциальной энергий. 
Кинетическая энергия определяется хаотическим движением частиц тела. С увеличением скорости их движения она увеличивается. Но температура тела тоже определяется скоростью движения частиц этого тела, поэтому изменение температуры тела в процессе означает изменение внутренней кинетической энергии.
Потенциальная энергия определяется силами взаимодействия между частицами тела.
Абсолютное значение внутренней энергии тела определить невозможно (отсутствует начальная точка отсчёта). Всю внутреннюю энергию в термодинамическом процессе использовать невозможно, поэтому достаточно знать, как изменилась энергия в данном процессе.
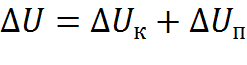 [Дж] изменение удельной внутренней энергии
[Дж] изменение удельной внутренней энергии
 [
[  (5.1)
(5.1)
В 1843 году Джоуль сформулировал весьма важный закон идеальных газов «внутренняя энергия идеального газа зависит лишь от температуры этого газа», т.к.  T–параметр состояния, то U идеального газа тоже будет параметром состояния.
T–параметр состояния, то U идеального газа тоже будет параметром состояния.
1.1.5. Принцип эквивалентности
Джоуль экспериментально доказал, что между теплом и механической энергией есть взаимосвязь. Проделанные опыты показали наглядно эту связь. Они проводились в период с 1843г. по 1850г. и позволили сформулировать принцип эквивалентности.

Установление этого принципа–наиболее трудный этап в формировании первого начала (закона) термодинамики. Им занимались: академик Гесс (1840г.), Джоуль(1843г.), Майер(1842г.), Геймгольц(1847г.)
Джоуль определил, что между затраченной работой и полученным теплом существует зависимость  , (5.2)
, (5.2)
где А – коэффициент пропорциональности, он сохраняет постоянное значение независимо от вида работы, пути получения тепла, температуры тела и т.д. Этот коэффициент получил название теплового эквивалента работы. Величина, обратная коэффициенту А, называется механическим эквивалентом теплоты.
Таким образом, если разные виды энергии взяты в таких количествах, что каждый из них вызывает одно и то же изменение системы, то указанные количества разных видов энергии будут являться эквивалентными.
Первое начало термодинамик и было сформулировано Майером в 1842году «невозможно создать вечный тепловой двигатель 1-го рода». В более ясной форме оно сформулировано Геймгольцем в 1847году «Невозможно построить такую машину, с помощью которой можно было бы получить полезную работу без затрат энергии из вне, т.е. черпая энергию из ничего.
Подобное устройство называется вечным двигателем первого рода, построение и работа которого в соответствии с законом сохранения энергии невозможно.»
Первый закон (первое начало) термодинамики в общем виде представляет собой закон сохранения и превращения энергии. Этот закон налагает строгое условие на все процессы природы, которые при всём их многообразии ограничены условием сохранения энергии.
Дадим несколько формулировок закона.
 2018-02-13
2018-02-13 314
314








