Т.к. единицами количества вещества для газов являются: килограмм, кубический метр, киломоль, то различают три вида удельных теплоёмкостей: массовую теплоёмкость, объёмную и молярную.
Массовой удельной теплоёмкостью с[Дж/кг∙К] называется количество тепла, необходимого для нагрева 1кг вещества на 1градус в данном процессе
 (4.1).
(4.1).
Объёмной удельной теплоёмкостью с’[Дж/м³∙К] называется количество тепла, необходимого для нагрева 1м³ на 1градус в данном процессе
с’=сρн, где (4.2)
ρн – плотность вещества при стандартных условиях.
Молярной удельной теплоёмкостью с[Дж/кмоль∙К] называется количество тепла, необходимого для нагрева 1киломоля вещества на 1градус в данном процессе
с=μс (4.3)
Наиболее часто в расчётах пользуются массовой удельной теплоёмкостью, которую в дальнейшем будем называть просто теплоёмкостью.
В уравнении (4.1) величина подведённого тепла(q) зависит не только от интервала температур(t₂–t₁), но и от вида процесса подвода (отвода) тепла, поэтому величина q снабжается индексом z, характеризующим вид процесса. Индекс обозначает тот параметр, который сохраняет постоянное своё значение в данном процессе. Наиболее часто на практике используют изобарную – 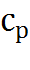 и изохорную –
и изохорную –  теплоёмкости.
теплоёмкости.
1.4.2. Истинная и средняя теплоёмкость.
Теплоёмкость вещества – величина переменная, зависящая от температуры. У газов теплоёмкость зависит от температуры, давления и атомности газа. Идеальные и одноатомные газы меняют теплоёмкость только при изменении температуры.
Теплоёмкость меняет свои значения в ряде случаев весьма значительно. Поэтому в уравнении (4.1) теплоёмкость, определённая в интервале температур (t₂–t₁) называют средней теплоёмкостью и обозначают  .
.
Теплоёмкость, определённая для заданной температуры t, называется истинной теплоёмкостью и обозначается  и
и 
Истинные и средние теплоёмкости можно определять двумя путями:
– графически по с–t диаграмме;
– по таблицам теплоёмкостей.
Зависимость теплоёмкости от температуры выражается нелинейным уравнением c=a+bt+еt², где а, b, е – постоянные величины, зависящие от природы газа. Графиком этого уравнения является парабола в системе
с–t. Если площадь четырёхугольника 1-2-t₂-t₁ заменить площадью равновеликого прямоугольника 3-4-t₂-t₁, то ордината 3-t1 в масштабе определяет среднюю теплоёмкость в интервале температур (t₂-t₁).

 На практике параболический закон изменения теплоёмкости заменяют линейным. При этом средняя теплоёмкость определяется по среднеарифметической температуре процесса
На практике параболический закон изменения теплоёмкости заменяют линейным. При этом средняя теплоёмкость определяется по среднеарифметической температуре процесса

Найденная Сm будет средней для процесса в интервале температур (t₂–t₁) и истинной для температуры tm. При пользовании таблицами, как правило, в интервале температур предусматривается только линейная зависимость.
 2018-02-13
2018-02-13 662
662








