Переход вещества из твердого состояния в жидкое называется плавлением, наоборот – кристаллизацией.
При плавлении происходит увеличение расстояния между молекулами и происходит разрушение кристаллической решетки, увеличивается молекулярно-кинетическая энергия. При кристаллизации всё происходит наоборот.
Область, в которой вещество однородно по всем физическим и химическим свойствам, называется фазой состояния этого вещества.
Удельная теплота плавления. Плавление и кристаллизация определённого вещества происходит при одинаковой температуре, не изменяющейся, пока совместно существуют твердая и жидкая фазы вещества.
 ,
,
где Q – теплота плавления;
l – удельная теплота плавления;
m – масса вещества.
Q зависит от рода вещества и внешних условий.
l характеризует зависимость изменения внутренней энергии вещества в процессе его плавления или кристаллизации от рода вещества и внешних условий.
 [Дж/кг].
[Дж/кг].
Теплоту Qж, нужную для нагревания жидкости до точки кипения, находят по формуле:
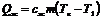
где m – масса жидкости, сж – её удельная теплоемкость.
Теплоту Qп, необходимую для превращения жидкости в пар без изменения температуры рассчитывают по формуле: Qп = rm.
Следовательно, общее количество теплоты при парообразовании:
Qпар=Qж+Qп=cжm(Tк-T1)+rm
Количество теплоты при кристаллизации:
Qкр=λm+cm(T-Tпл)
 2018-02-14
2018-02-14 1223
1223
