Второе начало термодинамики можно сформулировать как закон возрастания энтропии замкнутой системы при необратимых процессах: любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает.
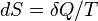

Можно дать более короткую формулировку второго начала термодинамики: в процессах, происходящих в замкнутой системе, энтропия не убывает. Существенен момент, что речь идет о замкнутых системах, так как в незамкнутых системах энтропия может вести себя произвольным образом (возрастать, убывать, оставаться постоянной). Кроме того, повторим еще раз, что энтропия остается постоянной в замкнутой системе только при обратимых процессах. При необратимых процессах и в замкнутой системе энтропия всегда возрастает.
Формула Больцмана S=k•lnW дает объяснение, постулируемое вторым началом термодинамики возрастанию энтропии в замкнутой системе при необратимых процессах: возрастание энтропии означает переход системы из менее вероятных в более вероятные состояния. Значит, формула Больцмана дает статистическое толкование второго начала термодинамики. Являясь статистическим законом, оно описывает закономерности хаотического движения огромного числа частиц, которые составляют замкнутую систему.
Дадим еще две формулировки второго начала термодинамики:
1) по Кельвину: невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу;
2) по Клаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
Цикл Карно. К.П.Д.
Основываясь на втором начале термодинамики,Карно вывелтеорему, носящую теперь его имя: из всех периодически действующих тепловых машин, имеющих одинаковые
Рис. 87 
температуры нагревателей ( ) холодильников (
) холодильников ( ), наибольшим к. п. д. обладают обратимые машины; при этом к. п. д. обратимых машин, работающих при одинаковых температурах нагревателей (
), наибольшим к. п. д. обладают обратимые машины; при этом к. п. д. обратимых машин, работающих при одинаковых температурах нагревателей ( ) и холодильников (
) и холодильников ( ), равны друг другу и не зависят от природы рабочего тела (тела, совершающего круговой процесс и обменивающегося энергией с другими телами).
), равны друг другу и не зависят от природы рабочего тела (тела, совершающего круговой процесс и обменивающегося энергией с другими телами).
Карно теоретически проанализировал обратимый наиболее экономичный цикл, состоящий из двух изотерм и двух адиабат, называемый циклом Карно. Рассмотрим прямой цикл Карно, в котором в качестве рабочего тела используется идеальный газ, заключенный в сосуд с подвижным поршнем.
Цикл Карно изображен на рис. 87, где изотермические расширения и сжатия заданы соответственно кривыми 1—2 и 3—4,а адиабатические расширение и сжатие — кривыми 2—3 и 4—1. При изотермическом процессе U =constколичество теплоты  , полученное газом от нагревателя, равно работе расширения
, полученное газом от нагревателя, равно работе расширения  , совершаемой газом при переходе из состояния 1 в состояние 2:
, совершаемой газом при переходе из состояния 1 в состояние 2:

 (59.1)
(59.1)
При адиабатическом расширении 2—3 теплообмен с окружающей средой отсутствует, и работа расширения  совершается за счет изменения внутренней энергии:
совершается за счет изменения внутренней энергии: 
Количество теплоты  , отданное газом холодильнику при изотермическом сжатии, равно работе сжатия
, отданное газом холодильнику при изотермическом сжатии, равно работе сжатия 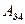 :
:
 (59.2)
(59.2)
Работа адиабатического сжатия

Работа, совершаемая в результате кругового процесса,

и, как можно показать, определяется площадью, выполненной в цвете на рис. 87.
Термический к.п.д. цикла Карно:

Применив уравнение для адиабат 2—3 и 4—1, получим

откуда
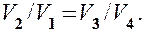 (59.3)
(59.3)
Подставляя (59.1) и (59.2) в формулу (56.2) и учитывая (59.3), получим
 (59.4)
(59.4)
т. е. для цикла Карно к. п. д. действительно определяется только температурами нагревателя и холодильника. Для его повышения необходимо увеличивать разность температур нагревателя и холодильника. Например, при  = 400 K и
= 400 K и  = 300 К
= 300 К  =0,25. Если же температуру нагревателя повысить на 100 К, а температуру холодильника понизить на 50 К, то
=0,25. Если же температуру нагревателя повысить на 100 К, а температуру холодильника понизить на 50 К, то  = 0,5. К. п. д. всякого реального теплового двигателя из-за трения и неизбежных тепловых потерь гораздо меньше вычисленного для цикла Карно.
= 0,5. К. п. д. всякого реального теплового двигателя из-за трения и неизбежных тепловых потерь гораздо меньше вычисленного для цикла Карно.
 2018-02-14
2018-02-14 1461
1461
