Классификация дисперсных систем. Коллоидное состояние.
Колоидная химия, занимается дисперсными системами и поверх.явл.
Дисперсная система - это такое состояние материи,где одно вещество(дисперсионная фаза), распред. в другом (дисперсионная среда).(масло в H2O)
Классификация дисперсных систем:
1)г/ж-(пена, газовые эмульсии)-мыльная пена
2)ж/ж-(эмульсия)-молоко, смазки, сырая нефть(бензол-вода)
3)тв/ж-золи, суспензия(золи металлов в воде),бактерии
4)г/тв-твердая пена (пемза,пенопласт,силикагель,угли активные)
5)ж/тв-(пористые тела,капилярные системы)-встреч. редко (адсорбенты,почвы)
6)тв/тв-сплавы,композиты,минералы
7)ж/г-аэрозоли(туманы)-тучи,облака
8)тв/г-аэрозоли(пыль,дым)
9)г/г-атмочфера Земли
Грубодисперсные системы(суспензии,эмульсии,порошки)-более 1мкн(10-4-10-2 см), так и высокодисперсные меньше 1мкн(<10-6)/(10-4-10-7 см)
Область коллоидного состояния- 1нм-1мкн
Переходное состояние от молек.диспергированного состояния к микро фаз. Важный параметр-устойчивость.Любое дисперсионное состояние-энергоперенасыщенно.(явлповерх.раздела фаз –частица на поверх.-бол. энергия,чем в толщевещества. Дисперсионная система-характеризуется, дисперсионным размером частиц и удельной поверхностью.
Понятие о поверхностном слое. Геометрические параметры поверхности. Термодинамич. Функции поверхностного слоя.
На границе между дисперсионной фазой и дисперсионной средой расположен слой отличающийся от свойств дисперсной фазы и дисперсионной среды- поверхностный слой.
Между молекулами любого вещества действуют Ван-дер-Ваальсовы силы. Существует набор и полярных сил:диполи, легко поляризуемые и плохо поляризуемые.
1)равнодействующая сила межмолякулярного взаимодействия для частиц, на поверхности направленна в глубь вещества, а для частиц в объеме равна 0.
2)частицы на поверх. обладают бол. энергией,чем частицы в объеме.
3) Требуется совершить работу, чтобы вытащить частицу из объема на поверхность. (ув. свободной пов. энергии)
Толщина поверхностного слоя зависит от свойств дисперсной фазы и дисперсионной среды.Доля поверхностного слоя в общем объеме вещества тем больше, чем меньше размер частиц дисперсионной фазы. Степень раздробленности дисперсионной фазы оценивается величиной частиц и величиной удельной поверхности Sуд.(отношюпов раздела фаз S к объему или массе дисперсной фазы) Явления протекающие на границе раздела фаз, называются поверхностными явлениями (адсорбция).-перераспределение компонентов гетерогенной системы между фазами и поверхностным слоем.
Поверхностное и межфазное натяжение. Влияние природы фаз на натяжение. Методы определения поверхностного натяжения.
Поверхностное натяжение- это сила действующая на единицу поверхности и направленная перпендикулярно опоясывающему его контур.
Кроме силовой используется и энергетическая трактовка. В этом случае под силой понимают работу которую требуется совершить при квазиравновесном изменении площади межфазной поверхности на 1м2. Поверхностное натяжение жидкостей обусловлено взаимодействием молекул поверхностного слоя. Межмолекулярное взаимодействие складывается из 3 составляющих: ориентационной, индукционной и дисперсионной.
Ориентационной называется взаимодействие молекул полярных веществ.
Индукционное взаимодействие полярной и неполярной молекулы.
Дисперсионной взаимодействие неполярных молекул, взаимодействие мгновенных диполей
Поверхностное натяжение полярных жидкостей больше,чем неполярных.
Методы определения поверхностного натяжения.
Статические методы:
Метод вращающейся капли
Сущностью метода является измерение диаметра капли жидкости, вращающейся в более тяжелой жидкости. Этот способ измерения годится для измерения низких или сверхнизких значений межфазного натяжения. Он широко применяется для микроэмульсий, измерения эффективности ПАВ в нефтедобыче, а также для определения адсорбционных свойств.
Динамические методы:
МетодДюНуи (метод отрыва кольца)
Метод является классическим. Сущность метода вытекает из названия. Платиновое кольцо поднимают из жидкости, смачивающей его, усилие отрыва и есть сила поверхностного натяжения и может быть пересчитано в поверхностную энергию. Метод подходит для измерения ПАВ, трансформаторных масел и т. д.
4..Адсорбция на границе раствор – газ. Поверхностное натяжение растворов. Уравнение изотермы адсорбции Гиббса, его анализ.
В жидких растворах поверхностное натяжение σ является функцией от концентрации растворенного вещества. На рис. 4.1 представлены три возможных зависимости поверхностного натяжения от концентрации раствора (т.н. изотермы поверхностного натяжения). Вещества, добавление которых к растворителю уменьшает поверхностное натяжение, называют поверхностно-активными (ПАВ), вещества, добавление которых увеличивает или не изменяет поверхностное натяжение – поверхностно-инактивными (ПИАВ).

Рис. 4.1 Изотермы поверхностного Рис. 4.2 Изотерма адсорбции
натяжения растворов ПИАВ (1, 2) и ПАВ на границе раствор – пар
ПАВ (3)
Уменьшение поверхностного натяжения и, следовательно, поверхностной энергии происходит в результате адсорбции ПАВ на поверхности раздела жидкость – пар, т.е. того, что концентрация поверхностно-активного вещества в поверхностном слое раствора оказывается больше, чем в глубине раствора.
Количественной мерой адсорбции на границе раствор-пар является поверхностный избыток Г (гамма), равный числу молей растворенного вещества в поверхностном слое. Количественное соотношение между адсорбцией (поверхностным избытком) растворенного вещества и изменением поверхностного натяжения раствора с ростом концентрации раствора определяет изотерма адсорбции Гиббса:
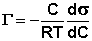
График изотермы адсорбции ПАВ представлен на рис. 4.2. Из уравнения следует, что направление процесса – концентрирование вещества в поверхностном слое или, наоборот, нахождение его в объеме жидкой фазы – определяется знаком производной dσ/dС. Отрицательная величина данной производной соответствует накоплению вещества в поверхностном слое (Г > 0), положительная – меньшей концентрации вещества в поверхностном слое по сравнению с его концентрацией в объеме раствора. С ростом концентрации поверхностная активность ПАВ уменьшается.
 2018-02-13
2018-02-13 1225
1225