Електрохімічне одержання металів з водних розчинів електролізом займає значне місце в технічній електрохімії.
Цим способом одержують і рафінують багато металів (мідь, цинк, нікель, хром та ін.).
Електроліз ведуть як з розчинним так і з не розчинним анодом. На катоді виділяється чистий метал, а на аноді галоген або кисень і регенерується відповідна кислота.
Гідроелектрометалургійний процес одержання металів із руд складається з слідуючих стадій:
- Підготовка руди з метою переводу її в розчинну форму.
- Розчинення руди.
- Очищення одержаного розчину від шкідливих для електролізу домішок.
- Корегування електроліту – добавка кислот та інших речовин.
- Електроліз для одержання чи рафінування металу.
Прикладом гідрометалургічного процесу одержання кольорових металів може бути одержання цинку.
Електролітом при цьому служить розчин сірчанокислого цинку, одержаний розчиненням цинку з цинкових руд сірчаною кислотою.
Для покращення розчинності сульфідів цинку піддають випалювання при цьому одержують легкорозчинний оксид цинку в сірчаній кислоті.

Одержавши розчин сірчанокислого цинку
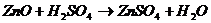
його піддають очищенню від домішок і направляють на електроліз. Для кращої єлектропроводності розчин підкислюють сірчаною кислотою. Концентрація цинку в електроліті, звичайно, 50-60 г/л., а сірчаної кислоти не більше 100-120 г/л, температура електроліту - 35-40°С.
При електролізі на катодах з алюмінію осідає цинк, а на свинцевих анодах виділяється кисень. Чистота одержаного цинку 99,7-99,9%. Катодний цинк переплавляється і розливається в чушки.
Подібними способами одержують і інші кольорові метали.
 2018-02-20
2018-02-20 258
258








