Идеальными газами (ИГ) называют такие, которые полностью подчиняются законам Бойля-Мариотта и Гей-Люссака. В идеальных газах отсутствуют силы взаимного притяжения и отталкивания между молекулами, а объем самих молекул пренебрежимо мал по сравнению с объемом газа. Состояние идеального газа – это предельное состояние реального газа, когда давление стремится к нулю ( ).
).
Введение понятия об идеальном газе позволило составить простые математические зависимости между величинами, характеризующими состояние тела, и на основе законов для ИГ создать стройную теорию ТДП.
Закон Бойля – Мариотта (английский физик 1664 г. – французский химик 1676 г.) гласит: при постоянной температуре объем, занимаемый идеальным газом, изменяется обратно пропорционально его давлению:
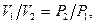 (10)
(10)
или при постоянной температуре 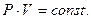
Закон Гей-Люссака (французский физик 1803 г.) устанавливает зависимость между удельным объемом 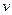 и абсолютной температурой T. Закон гласит: при постоянном давлении объемы одного и того же количества идеального газа изменяются прямо пропорционально абсолютным температурам:
и абсолютной температурой T. Закон гласит: при постоянном давлении объемы одного и того же количества идеального газа изменяются прямо пропорционально абсолютным температурам:
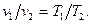 (11)
(11)
Совместное применение этих законов к произвольному процессу дает уравнение состояния идеального газа:
 . (12)
. (12)
При умножении обеих частей уравнения (12) на массу газа (М, кг) получаем:
PV=MRT (13)
где R – удельная газовая постоянная, 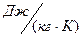 .
.
Уравнения (12) и (13) называются уравнениями Клапейрона. С достаточной для практики точностью их можно применять и для реальных газов, имеющих низкое давление и высокую температуру.
Умножив обе части уравнения (13) на молярную массу газа (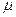 ,
, 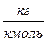 ) получим уравнение Клапейрона – Менделеева:
) получим уравнение Клапейрона – Менделеева:
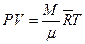 . (14)
. (14)
Величина 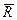 носит название универсальной газовой постоянной:
носит название универсальной газовой постоянной:
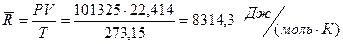 .
.
Газовые смеси
В качестве рабочего тела тепловых двигателей и установок часто используются смеси различных газов.
Под газовой смесью понимается смесь отдельных газов, не вступающих между собой ни в какие химические реакции. Каждый компонент газовой смеси полностью сохраняет все свои свойства и ведет себя так, как если бы он один занимал весь объем смеси.
Газовая смесь ИГ подчиняется закону Дальтона – общее давление смеси газов равно сумме парциальных давлений отдельных газов, составляющих смесь:
 (15)
(15)
 2020-01-15
2020-01-15 144
144








