В теорию газовых смесей введено понятие о средней (кажущейся) молекулярной массе смеси mсм, т.е. о молекулярной массе такого воображаемого однородного газа, который по своим свойствам аналогичен рассматриваемой смеси.
Находится кажущаяся молекулярная масса следующим образом. Из определения киломоля вытекает равенство, справедливое для любого однородного газа:
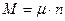 , (24)
, (24)
где n - количество вещества компонента, моль.
Для смеси по аналогии можно записать:
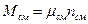 . (25)
. (25)
Отсюда, из равенства:
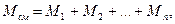 (26)
(26)
следует, что:
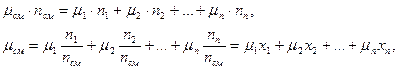 (27)
(27)
где 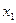 ;
; 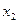 ; …;
; …; 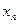 – мольные доли компонентов смеси, моль.
– мольные доли компонентов смеси, моль.
Поскольку 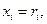 то среднюю молекулярную массу можно выразить:
то среднюю молекулярную массу можно выразить:
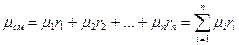 . (28)
. (28)
Если известен массовый состав смеси, то кажущуюся молекулярную массу смеси вычисляют по уравнению:
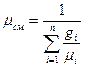 . (29)
. (29)
Если известен объемный состав смеси (объемная доля компонентов), то плотность смеси газов можно вычислить из соотношений:
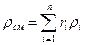 . (30)
. (30)
Если газовая смесь задана массовыми долями, то плотность смеси можно определить из соотношения:
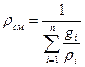 . (31)
. (31)
Удельный объем смеси представляет величину, обратную плотности смеси:
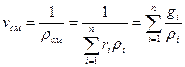 . (32)
. (32)
Объемные доли компонентов смеси удобно использовать для вычисления парциальных давлений ее составных частей. Из уравнения:
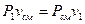 , (33)
, (33)
следует, что:
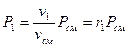 , (34)
, (34)
т.е. для любого компонента смеси можно записать:
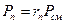 . (35)
. (35)
ТЕПЛОЕМКОСТЬ
Теплоемкостью называется количество теплоты, которое необходимо подвести к какой-либо количественной единице рабочего тела, чтобы нагреть ее на
1 градус (1 °С или 1 К).
Истинная теплоемкость – производная количества теплоты по температуре, она определяется в виде отношения:
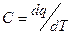 , (36)
, (36)
откуда:
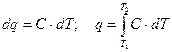 . (37)
. (37)
Теплоемкость зависит от характера процесса, при котором подводится или отводится теплота, поэтому при экспериментальном определении ее значения обычно используют два термодинамических процесса, протекающих при постоянном объеме 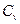 и давлении
и давлении 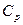 . Значения теплоемкостей
. Значения теплоемкостей 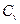 и
и 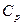 для различных веществ сведены в таблицы.
для различных веществ сведены в таблицы.
Подведенная при постоянном объеме теплота, когда dl=0, расходуется только на изменение внутренней энергии. При постоянном давлении некоторое количество теплоты идет также на совершение работы, поэтому для изменения температуры рабочего тела на 1 градус при P = const требуется большее количество теплоты, чем при v = const и, следовательно 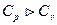 .
.
В зависимости от способа определения количества рабочего тела (т.е. от количественной единицы измерения рабочего тела, которую необходимо нагреть) теплоемкости делят на:
- удельные массовые:
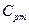 и
и 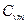 ,
, 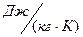 ;
; - удельные объемные:
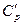 и
и 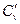 ,
, 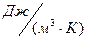 ;
; - удельные молярные:
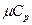 и
и 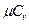 ,
, 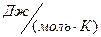 .
.
Все они связаны м/у собой соотношениями:
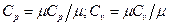 ; (38)
; (38)
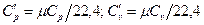 ; (39)
; (39)
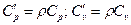 . (40)
. (40)
Теплоемкости 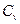 и
и 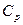 газа не зависят ни от объема, ни от давления, и являются однозначными функциями температуры. Иногда, в приближенных расчетах, зависимостью от температуры пренебрегают и значения теплоемкости принимают постоянными. Тогда в соответствии с выражением (37):
газа не зависят ни от объема, ни от давления, и являются однозначными функциями температуры. Иногда, в приближенных расчетах, зависимостью от температуры пренебрегают и значения теплоемкости принимают постоянными. Тогда в соответствии с выражением (37):
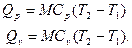 (41)
(41)
В большинстве случаев функцию С=f(Т) (см. рисунок 3) приходится учитывать и использовать для определения количества подведенной или отведенной теплоты, которая численно равна площади под характеристикой 1-2 процесса. Количество теплоты можно найти, если использовать средние значения теплоемкости Сср, при V = const или Р = const определяются отношением:
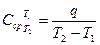 . (42)
. (42)
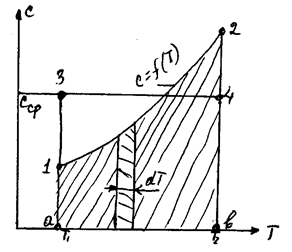
Рисунок 3 – Зависимость теплоемкости от температуры
В этом случае площадь а34в, равна площади а12в. С помощью Сср, можно рассчитать количество теплоты по формуле аналогичной выражению (42).
Если необходимо получить количество подведенной теплоты в интервале температур T1 – T2 , то поступают следующим образом: сначала определяют количество теплоты
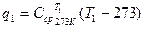 ,
,
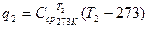 ,
,
а затем:
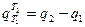 . (43)
. (43)
Для многих теплотехнических расчетов зависимость С=f(Т) принимают линейной, тогда:
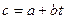 . (44)
. (44)
где а – теплоемкость при 0 ºС;
b – тангенс угла наклона прямой (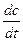 ).
).
В этом случ ае
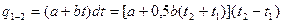 , (45)
, (45)
тогда:
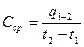 . (46)
. (46)
Если рабочим телом является смесь газов, то ее теплоемкость зависит от состава смеси:
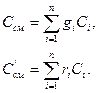 (47)
(47)
 2020-01-15
2020-01-15 1553
1553
