Из фототрофных организмов способность к выделению Н2 проявляют многие пурпурные бактерии, цианобактерии и ряд водорослей. Среди последних есть не только микро-, но и макроформы. Есть данные о выделении в небольшом количестве Н2 и высшими растениями.
Пурпурные бактерии осуществляют так называемый аноксигенный фотосинтез (фотосинтез без выделения молекулярного кислорода). Объясняется это тем, что они не могут использовать воду при фотоассимиляции СО2 и в других конструктивных процессах в качестве исходного донора электронов; такую функцию у них выполняют сульфид, сера, тиосульфат, органические вещества или Н2.
Анаэробное окисление многими пурпурными бактериями органических веществ и неорганических соединений серы в определенных условиях ведет к образованию ими Н2. Особенно в большом количестве эти микроорганизмы выделяют молекулярный водород в присутствии света. Поэтому данный процесс часто называют фотовыделением водорода. В отличие от образования Н2 при брожении фотовыделение Н2 пурпурными бактериями катализирует обычно не гидрогеназа, а нитрогеназа — фермент, главная функция которого заключается в превращении N2 в аммиак. Но даже при наличии N2 часть электронов, поступающих к нитрогеназе, расходуется на восстановление протонов, что ведет к выделению H2:
N2 + 8е  + 8Н+
+ 8Н+  2NH3 + Н2
2NH3 + Н2
К фотовыделению Н2 способны растущие культуры, суспензии клеток, а также иммобилизованные клетки пурпурных бактерий. Некоторые субстраты, например ацетат, лактат, малат, глюкоза, могут полностью разлагаться клетками этих микроорганизмов до СО2 и Н2.
К числу наиболее активных продуцентов Н2 относятся некоторые штаммы Rhodobacter capsulatus. Растущие культуры этой бактерии, используя лактат, выделяют в некоторых условиях Н2 со скоростью 300—500 мл ч  ∙г
∙г  сухой биомассы. При использовании клетками пурпурных бактерий 1 кг лактата можно получить до 1350 л Н2. КПД конверсии энергии света при образовании пурпурными бактериями Н2 достигает 2,0—2,8 %.
сухой биомассы. При использовании клетками пурпурных бактерий 1 кг лактата можно получить до 1350 л Н2. КПД конверсии энергии света при образовании пурпурными бактериями Н2 достигает 2,0—2,8 %.
Среди цианобактерий также обнаружены штаммы, выделяющие при наличии света Н2 в довольно большом количестве и со значительной скоростью (30—40 мл ч  ∙г
∙г  сухой биомассы). К таким организмам относятся в основном нитчатые формы, образующие особые клетки — гетероцисты (например, Anabaena cylindrica, A. varidbilis, Mastlgocladus thermophilus, M. laminosus).
сухой биомассы). К таким организмам относятся в основном нитчатые формы, образующие особые клетки — гетероцисты (например, Anabaena cylindrica, A. varidbilis, Mastlgocladus thermophilus, M. laminosus).
Выделение Н2 чаще всего отмечается у суспензий клеток, причем может продолжаться 30 сут и более. Такую же способность проявляют иммобилизованные клетки микроорганизмов. В отличие от пурпурных бактерий для образования Н2 цианобактериями не требуется каких-либо экзогенных доноров электронов, кроме воды. Важно также, что нитчатые формы бактерий, образующие гетероцисты, и некоторые одноклеточные виды способны выделять Н2 не только в анаэробных, но и в аэробных условиях.
Фотообразование цианобактериями Н2, как и у пурпурных бактерий (за редким исключением) катализирует нитрогеназа. Этот фермент очень чувствителен к молекулярному кислороду, но у цианобактерий, выделяющих Н2 в аэробных условиях, он защищен от инактивирующего действия О2 разными способами. У нитчатых форм, образующих гетероцисты, нитрогеназа локализуется в основном в этих специализированных клетках, которые в процессе фотосинтеза молекулярный кислород не выделяют.
КПД преобразования энергии света в Н2 у цианобактерий по имеющимся расчетам может достигать около 10 %.
Выделение молекулярного водорода водорослями обнаружено лишь у суспензий клеток и в небольшом количестве, кроме того, процесс не стабилен. Одной из главных причин этого является инактивация гидрогеназы, катализирующей образование водорослями Н2, под действием молекулярного кислорода, который они выделяют при фотосинтезе.
Из вышесказанного следует, что из разных фототрофов наиболее просто использовать в качестве продуцентов водорода пурпурные бактерии. Но масштабность процесса получения с их помощью Н2 ограничивается запасами и ценой тех субстратов (органических веществ или неорганических соединений серы), которые могут разлагаться с выделением молекулярного водорода.
Более перспективны в данном отношении цианобактерии, поскольку выделение ими Н2связано с биофотолизом воды, которая пока остается наиболее дешевым и доступным субстратом. Не прекращаются работы и с водорослями, так как они также способны выделять Н2 при разложении воды. Предлагается, кроме того, использовать комплексные системы, образующие Н2, в которые входят разные фототрофы или фототрофы и хемотрофы. Известно, что хлоропласты (например, из шпината) в присутствии искусственного донора электронов и бактериального экстракта, содержащего фермент гидрогеназу, способны продуцировать водород:
донор электронов  фотосистема I
фотосистема I  переносчик e
переносчик e 
 гидрогеназа
гидрогеназа  Н2
Н2
Гидрогеназа получает электроны от ферредоксина. В качестве доноров электронов используются различные органические соединения. Процесс сопровождается облучением видимым светом. Эта форма получения энергии имеет ряд достоинств: избыток субстрата фотолиза (воды); нелимитированный источник энергии (солнечный свет); не загрязняющий атмосферу водород. Водород обладает более высокой теплотворной способностью по сравнению с углеводородами, кроме того, процесс получения водорода — возобновляемый процесс, зависящий в основном от стабильности выделенных хлоропластов. Водород можно получать в присутствии искусственного донора e  (вместо воды) и поглощающих свет пигментов, а не мембран хлоропластов. Его способны выделять и некоторые микроорганизмы, например цианобактерии (аэробные фототрофы) и др. При этом микробиологическое образование водорода может идти из соединений углеводного характера, включая крахмал и целлюлозу, а также из амино- и кетокислот.
(вместо воды) и поглощающих свет пигментов, а не мембран хлоропластов. Его способны выделять и некоторые микроорганизмы, например цианобактерии (аэробные фототрофы) и др. При этом микробиологическое образование водорода может идти из соединений углеводного характера, включая крахмал и целлюлозу, а также из амино- и кетокислот.
Основная проблема создания систем конверсии энергии биомассы в водород связана с превращением этих метаболитов в топливную форму. Для биотехнологии можно было бы воспользоваться и другими механизмами превращения энергии, выявленными у микроорганизмов. Например, галофильная бактерия Halobacterium halobium способна использовать световую энергию, улавливаемую пурпурным пигментом (бактериородопсином), вмонтированным в мембрану клетки. Молекула пигмента состоит из одной полипептидной цепи, к которой прикреплена молекула ретиналя, являющегося светочувствительной частью пигмента. Под влиянием солнечного света изменяется конформация пигмента, приводящая к переносу ионов водорода(H  ) через мембрану. Пигмент является как бы протонным насосом. Молекулы бактериородопсина располагаются в мембране триадами, и перекачивание протонов через мембрану обеспечивает градиент концентрации H
) через мембрану. Пигмент является как бы протонным насосом. Молекулы бактериородопсина располагаются в мембране триадами, и перекачивание протонов через мембрану обеспечивает градиент концентрации H  (Δ H
(Δ H 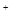 ), вследствие чего они движутся к наружной cтенке, у которой пространство подкисляется и возникает электрохимический градиент (Δ
), вследствие чего они движутся к наружной cтенке, у которой пространство подкисляется и возникает электрохимический градиент (Δ  ). Предприняты попытки
). Предприняты попытки  встраивания молекул пигмента в искусственные системы повышения эффективности их использования. В частности, растущие бактерии H. halobium переносят в мелкие водоемы с высокой концентрацией NaCl и других минеральных солей, в которых исключается загрязнение. У некоторых штаммов половина клеточной мембраны покрыта пурпурным пигментом, и из 10 л бактериальной культуры можно получить 0,5 г пурпурных мембран. В таких биомембранах содержится до 100 000 молекул родопсина. Биомембраны фиксируют на особой подложке, которая должна обладать всеми свойствами, необходимыми для обеспечения тока протонов, а не других ионов. В частности, для этих целей вполне пригодны пористые подложки, пропитанные липидами, которые, сливаясь с мембраной, сплошным слоем покрывают поверхность фильтра. Мембранные фрагменты можно смешивать и с акриламидом с образованием геля. Вместо создания плотных слоев молекул бактериородопсин и липиды могут создавать протеолипосомы, которые встраивают в структуры, обеспечивающие эффективное перекачивание протонов.
встраивания молекул пигмента в искусственные системы повышения эффективности их использования. В частности, растущие бактерии H. halobium переносят в мелкие водоемы с высокой концентрацией NaCl и других минеральных солей, в которых исключается загрязнение. У некоторых штаммов половина клеточной мембраны покрыта пурпурным пигментом, и из 10 л бактериальной культуры можно получить 0,5 г пурпурных мембран. В таких биомембранах содержится до 100 000 молекул родопсина. Биомембраны фиксируют на особой подложке, которая должна обладать всеми свойствами, необходимыми для обеспечения тока протонов, а не других ионов. В частности, для этих целей вполне пригодны пористые подложки, пропитанные липидами, которые, сливаясь с мембраной, сплошным слоем покрывают поверхность фильтра. Мембранные фрагменты можно смешивать и с акриламидом с образованием геля. Вместо создания плотных слоев молекул бактериородопсин и липиды могут создавать протеолипосомы, которые встраивают в структуры, обеспечивающие эффективное перекачивание протонов.
У H. Halobium имеется и другой тип насоса, который обеспечивает галородопсин, использующий световую энергию непосредственно для перекачивания ионов. Изучение систем энергоконверсии чрезвычайно перспективно с точки зрения разработки искусственных устройств, более эффективных, чем естественные.
Наконец, следует отметить интерес к некоторым ферментам, образуемым фототрофами и хемотрофами, выделяющими Н2, прежде всего к гидрогеназам. Помимо использования для получения Н2, гидрогеназы могут быть применены в других практически важных целях, включая восстановление кофакторов, например НАД, требующихся в некоторых производственных процессах, при синтезе соединений, меченных дейтерием и тритием, а также в топливных элементах.
Таким образом, хотя микробиологический способ получения молекулярного водорода еще не реализован, но работы в данном направлении развиваются и аспекты исследований водородобразующих видов микроорганизмов достаточно широки.
Заключение
Круг вопросов, к решению которых привлекают биотехнологические методы и достижения, достаточно широк. Большинство из них прямо или косвенно связано с глобальными проблемами, стоящими перед современной цивилизацией, такими, как загрязнение окружающей среды, угроза экологического кризиса, истощение запасов полезных ископаемых, опасность мирового энергетического кризиса, нехватка продовольствия, борьба с болезнями.
Повышение цен на традиционные источники энергии(природный газ, нефть, уголь) и угроза их исчерпания побудили ученых обратиться к альтернативным путям получения энергии. Роль биотехнологии в создании экономичных возобновляемых энергетических источников (спиртов, биогенных углеводородов, водорода) чрезвычайно велика. Эти экологически чистые виды топлива можно получать путем биоконверсии отходов промышленного и сельскохозяйственного производства. Перспективно продолжение исследований по усовершествованию и внедрению процессов производства метана, этанола, созданию на основе микроорганизмов (и ферментов) элементов, эффективно производящих электричество, а также по организации искусственного фотосинтеза, в частности, биофотолиза воды, при котором можно получать богатые энергией водород и кислород.
Список литературы
1. Промышленная микробиология. Под ред. Н.С.Егорова. М.: Высшая школа, 1989 – 688 с.
2. Т.А. Егорова, С.М. Клунова. Основы биотехнологии. М.: Академия, 2003 – 207с.
 2020-01-14
2020-01-14 366
366







