Атомно-абсорбционный спектральный анализ — метод количественного анализа, основанный на поглощении электромагнитного излучения атомами анализируемого вещества [6].
В результате неупругого взаимодействия внешнего (диагностирующего) излучения с атомами определенная доля этого излучения поглощается. Таким образом, интенсивность падающего излучения при прохождении через слой вещества уменьшается [6].
В результате поглощения излучения атомы переходят в возбужденные энергетические состояния. Таким переходам в атомных спектрах поглощения соответствуют так называемые резонансные линии. Энергия резонансных переходов и соответствующие частоты поглощения являются строго специфичными для атомов каждого химического элемента. В соответствии с величиной энергии диагностирующего излучения, используемой в атомно-абсорбционной спектрометрии, в атомах анализируемого вещества происходит возбуждение внешних электронов [6].
Для изучения поглощения используются оптические приборы - спектрофотометры. Применение атомно-абсорбционной спектроскопии в количественном химическом анализе основано на существовании взаимно однозначного соответствия между величиной поглощения и концентрацией атомов анализируемого вещества. Это соотношение определяется следующими законами светопоглощения:
Закон Бера: каждая частица (атом или молекула) поглощает одну и ту же долю энергии излучения. Тогда коэффициент поглощения k пропорционален количеству поглощающих частиц, которое, в свою очередь, определяет концентрацию анализируемого вещества:
k(λ) = α(λ)С (9)
Размерность коэффициента α(λ), как следует из (9), обратна размерности концентрации С. Эта величина зависит от длины волны падающего излучения, которая определяет энергию электронного возбуждения и вероятности переходов между электронными уровнями. В свою очередь, совокупность переходов между энергетическими уровнями создает спектр поглощения I(ν) или I(λ), зависящий от длины волны [6].
Закон Бера (9) справедлив для идентичных частиц поглощающей среды. Если, например, при взаимодействии атомов А образуется димеры А2, происходит или ионизация атомов, или образование молекул при взаимодействии с молекулами или атомами среды, то количество поглощающих частиц уменьшается. Это приводит к кажущемуся отклонению от закона Бера [6].
Закон Бугера—Ламберта: если среда однородна и слой вещества перпендикулярен падающему параллельному (коллимированному) световому потоку, то интенсивность I(λ) уменьшается с увеличением толщины поглощающего слоя по экспоненциальному закону:
I = I0ехр(-kl),(10)
где I0 и I — интенсивности падающего и прошедшего излучения; l — толщина слоя вещества.
Отклонения от закона Бугера—Ламберта известны только для световых потоков очень большой интенсивности, например, мощного лазерного излучения. Для источников света, используемых в аналитических приборах атомно-абсорбционной спектрометрии, данный закон выполняется с достаточной точностью [6]. Объединяя уравнения (9) и (10), получим формулу для основного закона поглощения света — закона Бугера—Ламберта—Бера:
I = I0ехр(-αCl) (11)
В спектральном анализе используется величина относительного пропускания света:
T = 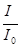 = ехр(-αCl) (12)
= ехр(-αCl) (12)
Эту безразмерную величину часто выражают в процентах. Линейное соотношение между концентрацией и поглощением получаем, если ввести
A = -lgT = lg 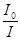 (13)
(13)
Безразмерную величину
A = lg 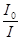 = ехр(αCl) = αCllge ≈ 0,4343αCl = εCl (14)
= ехр(αCl) = αCllge ≈ 0,4343αCl = εCl (14)
называют абсорбцией поглощающего слоя, где ε = 0,4343α.
Если величина концентрации выражена в молях на литр, то ε называют коэффициентом молярного поглощения. Часто используемая размерность ε, моль-1 · л ∙ см-1.
Градуировочный график, построенный в координатах (A,C), представляет прямую, проходящую через начало координат [6].
Чувствительность метода не зависит от концентрации и определяется величиной молярного поглощения ε(λ):
S = 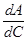 = ε(λ)l (15)
= ε(λ)l (15)
Таким образом, анализ следует проводить на длине волны λmax излучения, соответствующей максимуму ε(λ).
Так же, как и в методе атомно-эмиссионной спектроскопии, в атомно-абсорбционной спектрометрии анализируемое вещество должно находиться в атомизированном состоянии. Однако в отличие от атомно-эмиссионной спектроскопии здесь не требуются высокие температуры, приводящие к электронному возбуждении атомов анализируемого вещества с последующей спонтанной эмиссией излучения. Напротив, в атомно-абсорбционной спектрометрии диагностирующее излучение вызывает резонансное электронное возбуждение свободных атомов, находящихся в основном состоянии. Доля атомов, находящихся в основном состоянии, является преобладающей. При неизменных условиях атомизации исследуемого вещества концентрация атомов в атомизаторе пропорциональна истинной концентрации определяемого элемента в пробе. Тогда для поглощающего слоя можно записать:
A = KlC (16)
где коэффициент K включает коэффициенты молярного поглощения ε(λ) [см. формулу (14)] и перехода от истинной концентрации определяемого элемента в пробе к его концентрации в атомизаторе, l - толщина светопоглощающего слоя (пламени); C – концентрация [6].
Таким образом, так же как и в атомно-эмиссионной спектроскопии, коэффициент K в формуле (16) находится опытным путем при проведении серии измерений для стандартных образцов исследуемого вещества [6].
В практике анализа обычно применяют метод градуировочного графика и метод добавок.
В методе градуировочного графика измеряют оптическую плотность нескольких стандартных растворов и строят график в координатах оптическая плотность - концентрация. Затем в тех же условиях определяют оптическую плотность анализируемого раствора и по градуировочному графику находят его концентрацию [4].
При работе по методу добавок сначала измеряют оптическую плотность анализируемого раствора (Ах), затем вводят в анализируемый раствор определенный объем стандартного раствора и снова измеряют оптическую плотность (Ах+ст), Если Cх - концентрация анализируемого раствора, а Cст - стандартного, то
Ах = KlCx; (17)
Ах+ст = Kl (Cx + Cст) (18)
Учитывая, что K и l одинаковы, получаем:
Ах
|
Ах+ст - Ах
Метод применим для систем, подчиняющихся в исследуемой области концентраций уравнению:
A = lg 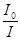 = KlC [4].
= KlC [4].
 2020-01-14
2020-01-14 296
296








