2. Лабораторные и промышленные методы получения диенов с сопряжёнными π-связями
3. Физические и химические свойства
Краткое содержание:
Эти два класса органических веществ — альдегиды и кетоны — характеризуются присутствием в молекуле карбонильной
группы, или радикала карбонила, >С=О. В альдегидах атом углерода этого радикала связан не менее чем с одним атомом водорода, так что получается одновалентный радикал
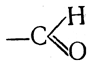
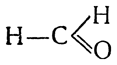 альдегид, называемый муравьиным альдегидом или формальдегидом, содержит альдегидную группу, связанную с атомом водорода, и имеет строение
альдегид, называемый муравьиным альдегидом или формальдегидом, содержит альдегидную группу, связанную с атомом водорода, и имеет строение
, или сокращенно
называемый также альдегидной группой. В кетонах карбонильная группа связана с двумя углеводородными радикалами и называется также кетогруппой или оксо-группой.
Гомологический ряд альдегидов и их номенклатура
Простейший
Н—СНО. В остальных альдегидах предельного ряда место одного атома водорода занимает алкил: С n С2 n +1—СНО.
Альдегиды можно также рассматривать как вещества, происшедшие от замещения в парафиновых углеводородах атома водорода на альдегидную группу, т. е. как однозамещенные производные углеводородов гомологического ряда метана. Следовательно, здесь гомология и изомерия те же, что и для других однозамещенных производных предельных углеводородов.
Названия альдегидов производятся от тривиальных названий кислот с тем же числом атомов углерода в молекуле. Так, альдегид СН3—СНО называется уксусным альдегидом или ацетальдегидом, СН3СН2—СНО — пропионовым альдегидом, СН3СН2СН2—СНО — нормальным масляным альдегидом или бутиральдегидом, (СН3)2СН—СНО — изомасляным альдегидом, альдегиды С4Н9—СНО — валериановыми альдегидами и т. д.
По женевской номенклатуре, названия альдегидов производятся от названий углеводородов, имеющих то же число углеродных атомов, с присоединением к окончанию ан слога аль, например метаналь Н—СНО, этаналь СН3—СНО, 2 -метилпропаналь СН3СН(СН3)—СНО и т. д.
Гомологический ряд кетонов и их номенклатура
Простейший из кетонов имеет строение СН3—СО—СН3 и называется диметилкетоном или ацетоном. От ацетона можно произвести гомологический ряд последовательным замещением атомов водорода на метил. Таким образом, следующий гомолог ацетона — метилэтилкетон имеет строение СН3—СО—СН2—СН3. Третий гомолог может существовать в трех изомерных формах:
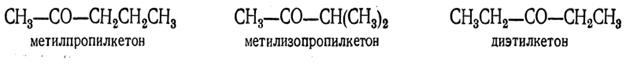
Названия кетонов, так же как и названия альдегидов, по женевской номенклатуре, производятся от названий углеводородов с тем же числом атомов углерода, с присоединением к окончанию ан слога он и прибавлением цифры, обозначающей место атома углерода карбонильной группы, считая от начала нормальной углеродной цепи; ацетон, таким образом, носит название пропанон, диэтилкетон — пентанон- 3, метилизопропилкетон — 2 -метилбутанон и т. д
Альдегиды и кетоны с одинаковым числом атомов углерода в молекуле изомерны друг другу. Общая формула для гомологических рядов предельных альдегидов и кетонов: С n Н2 n О.
Альдегиды и кетоны содержат в молекуле одну и ту же карбонильную группу, обусловливающую много общих типических свойств. Поэтому имеется очень много общего и в способах получения и в химических реакциях обоих этих родственных классов веществ. Присутствие в альдегидах атома водорода, связанного с карбонильной группой, обусловливает ряд отличий этого класса веществ от кетонов.
Способы получения
1. Окисление спиртов
Альдегиды и кетоны могут быть получены окислением спиртов, причем при окислении первичных спиртов получаются альдегиды, а при окислении вторичных — кетоны.
Окислителем, обычно применяемым для этой цели в лабораториях, является хромовая кислота, употребляемая чаще всего в виде «хромовой смеси» (смесь бихромата калия или натрия с серной кислотой). Иногда применяются также перманганаты различных металлов или перекись марганца и серная кислота. Наиболее важным практическим способом получения альдегидов является окисление спиртов кислородом воздуха в присутствии металлических катализаторов. Такими катализаторами, действующими уже при обыкновенной температуре, могут служить платина и другие металлы группы платины, а при повышенной температуре — металлическая медь.
2. Дегидрогенизация (дегидрирование) спиртов При пропускании паров спирта через нагретые трубки с мелко раздробленной, восстановленной водородом металлической медью первичные спирты распадаются на альдегид и водород, а вторичные — на кетон и водород. Несколько хуже эта реакция проходит в присутствии никеля, железа или цинка.
3. Получение из одноосновных карбонов ых к и с л о т Альдегиды можно получать восстановлением кислот:
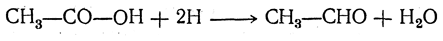
Для этой цели применяют частично отравленную сернистыми соединениями платиновую чернь (восстановление хлорангидридов по Розенмунду).
Кетоны и альдегиды могут быть получены также сухой перегонкой кальциевых и бариевых солей одноосновных кислот. Для всех кислот, кроме муравьиной, реакция идет следующим образом:
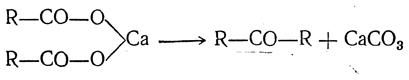
Чаще восстанавливают не самые кислоты, а их производные, например хлорангидриды:
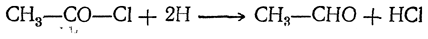
т. е. образуется кетон с двумя одинаковыми радикалами и карбонат кальция.
Если взять смесь солей двух кислот или смешанную соль, то наряду с предыдущей реакцией происходит также реакция между молекулами разных солей:
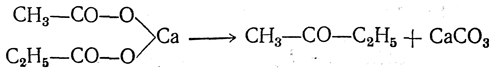
Если же взять смесь солей, из которых одна — соль муравьиной кислоты, то получается альдегид:
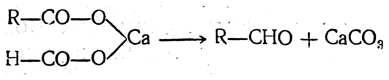
Вместо сухой перегонки готовых солей используют также контактный способ, так называемую реакцию кетонизации кислот, состоящую в том, что пары кислот пропускают при повышенной температуре над катализаторами, в качестве которых применяют углекислые соли кальция или бария, закись марганца, окись тория, окись алюминия и др. Для получения этим путем альдегидов лучшими катализаторами являются закись марганца и окись титана.
Несомненно, здесь сначала образуются соли органических кислот, которые затем разлагаются, регенерируя вещества, являющиеся катализаторами. В результате реакция идет, например, для уксусной кислоты по следующему уравнению:
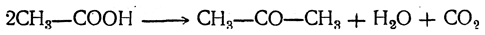
4. Действие воды на дигалоидные соединения Альдегиды и кетоны могут получаться при взаимодействии с водой дигалоидных соединений, содержащих оба атома галоида при одном и том же атоме углерода. При этом можно было бы ожидать обмена атомов галоида на гидроксилы и получения двухатомных спиртов, у которых обе гидроксильные группы находятся при одном и том же атоме углерода, например:
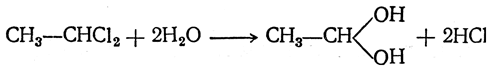
Но такие двухатомные спирты в обычных условиях не существуют, они отщепляют молекулу воды, образуя альдегиды или кетоны:
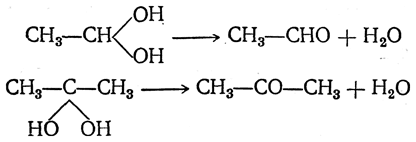
Таким образом, альдегиды и кетоны можно рассматривать как ангидриды двухатомных спиртов этого рода.
5. Действие воды на ацетиленовые углеводороды (реакция Кучеров а) При действии воды на ацетилен в присутствии солей окиси ртути получается уксусный альдегид:
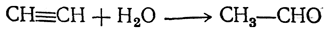
При действии воды в тех же условиях на гомологи ацетилена получаются кетоны:
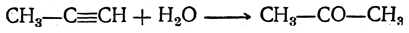
Эта реакция, открытая М. Г. Кучеровым в 1881—1884 гг., долгое время очень широко применялась и до сих пор не утратила своего значения для промышленного получения ацетальдегида, являющегося важным промежуточным продуктом в крупнотоннажных органических синтезах (уксусной кислоты, синтетических каучуков и т. п.).
6. Получение с помощью магний- и цинкорганических соединений Как было показано., при взаимодействии производных карбоновых кислот с некоторыми металлоорганическими соединениями присоединение одной молекулы металлоорганического соединения по карбонильной группе протекает по схеме
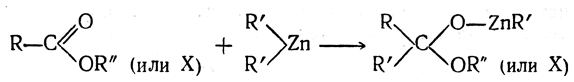
В случае производных муравьиной кислоты, например ее сложного эфира, реакция протекает следующим образом:
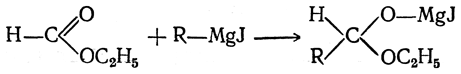
Если на полученные соединения подействовать водой, то они реагируют с ней с образованием в первом случае кетонов, а во втором — альдегидов:
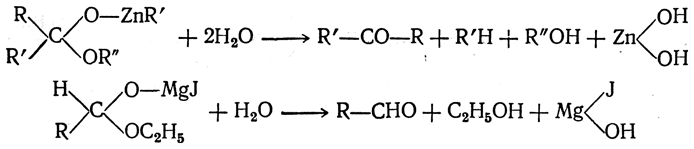
При указанных реакциях магнийорганических соединений приходится принимать различные меры, чтобы реакция не пошла дальше, вплоть до образования третичных спиртов.
И все же это удается лишь в ограниченном числе случаев. При действии магнийорганического соединения на сложный эфир чаще всего в реакцию вступает половина всего количества сложного эфира с образованием третичного спирта, а кетон вовсе не получается.
Практически наиболее удобным синтезом альдегидов при помощи металлоорганических соединений является получение их через посредство ацеталей из ортомуравьиного эфира СН(ОС2Н5)3, а также из амидов или нитрилов кислот.
При действии магнийорганических соединений на ортомуравьиный эфир происходит обмен радикала магнийорганического соединения на один из радикалов ОС2Н5 (этоксил), причем получается ацеталь альдегида (А. Е. Чичибабин, Бодру):
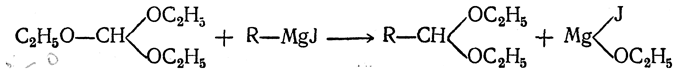
Ацеталь в присутствии кислоты омыляется, образуя альдегид:
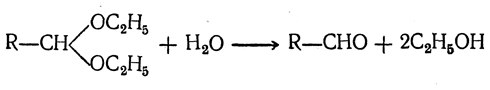
При действии на амид кислоты двух молекул магнийорганического соединения, а затем воды также получаются кетоны без образования третичных спиртов:
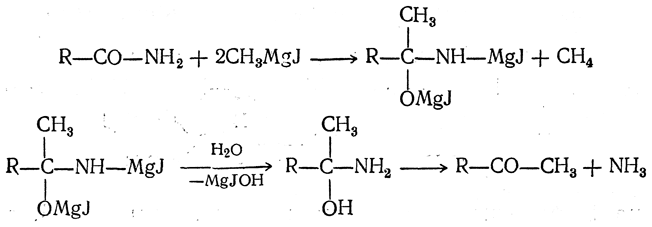
С формамидом по этой реакции получаются альдегиды. Сходно с амидами реагируют нитрилы кислот:
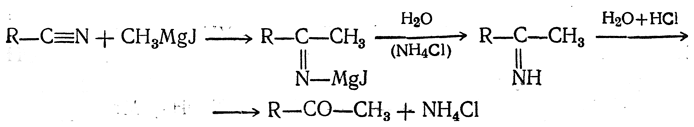
7. Действие кадмийорганических соединений на хлорангидриды кислот Кадмийорганические соединения взаимодействуют с хлорангидридами кислот иначе, чем магний- или цинкорганические:
R—СО—Cl + C2H5CdBr → R—СО—С2Н5 + CdClBr
Поскольку кадмийорганические соединения не вступают в реакцию с кетонами, здесь не могут получаться третичные спирты.
8. Гидролиз виниловых эфиров Альдегиды получаются при действии воды в присутствии минеральных кислот на простые виниловые эфиры (А. Е. Фаворский и М. Ф. Шостаковский):
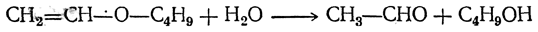
9. Взаимодействие олефинов с окисью углерода и водородом (оксосинтез) В присутствии кобальтового катализатора олефины реагируют в жидкой фазе при 150—250 ат и 100—200° С с окисью углерода и водородом. При этом получаются альдегиды, например:
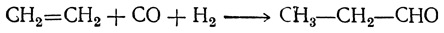
или
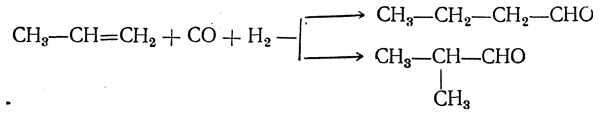
Фактически катализатором этой реакции являются карбонилы кобальта, образующиеся при взаимодействии кобальта с окисью углерода и действующие как гомогенный катализатор. Одновременно происходит частичное гидрирование альдегидов с образованием первичных спиртов. Этот процесс, называемый оксосинтезом, позволяет в промышленном масштабе получать различные первичные спирты из непредельных углеводородов.
 2020-04-12
2020-04-12 408
408








