Третичные амины присоединяют галоидные алкилы, особенно легко иодистые, а также средние эфиры сильных минеральных кислот, образуя соединения, имеющие строение солей четырехзамещенного аммония (соли четвертичных аммониевых оснований), например:
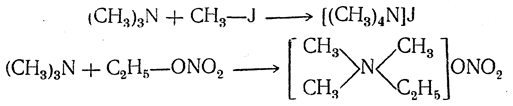
Эти соли растворимы в воде, на лакмус нейтральны, сильно диссоциированы электролитически в водных растворах и легко вступают в реакции обменного разложения с другими солями, например:
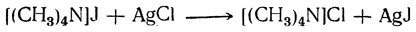
При нагревании эти соли распадаются на третичный амин и галоидный алкил (или эфир минеральной кислоты).
Прибавлением к растворам этих солей едкой щелочи нельзя выделить соответствующего основания вследствие обратимости реакции:

Наоборот, при действии водной окиси серебра на иодистую соль оседает нерастворимое иодистое серебро, а в водном растворе остается свободное четырехзамещенное аммониевое основание.
Гидроокись тетраметиламмония осторожным выпариванием в вакууме может быть получена в виде белого твердого вещества, похожего на едкие щелочи. Кристаллогидрат ((CH3)4N]OH · 5H2O плавится при 62—63°С.
В противоположность одно-, двух- и трехзамещенным аммониевым основаниям четырехзамещенные аммониевые основания обладают чрезвычайно сильными основными свойствами, приближаясь в этом отношении к едким щелочам. Эти основания нестойки к нагреванию. Гидроокись тетраметиламмония при нагревании распадается на триметиламин и метиловый спирт:
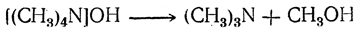
При нагревании всех четвертичных оснований, содержащих высшие алкилы, образуется не спирт, а соответствующий этиленовый углеводород и вода, например:
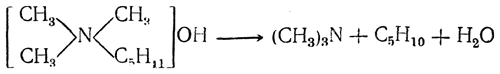
Эта реакция оказалась очень полезной при исследовании сложных циклических аминов, какими являются, например, многие природные алкалоиды.
Вопросы для самоконтроля:
1. Номенклатура нитросоединений алифатического ряда
2. Изомерия
3. Способы получения
4. Физические свойства
5. Химические свойства
Рекомендуемая литература:
1. Перекалин В.В., Зонис С.А. Органическая химия. М.,1982
2. Терней А. Современная органическая химия. М.,1979
3. Петров Е.Е., Бальян Х.В., Трощенко А.Т. Органическая химия. М, 1974
4. Ю. А. Жданова «Очерки методологии органической химии», Изд. «Высшая школа»., М., 1960.
Лекция № 20-21. Альдегиды и кетоны
Цель: ознакомиться с номенклатурой, методами получения, физическими и химическими свойствами, механизмом реакций альдегидов и кетонов.
Основные вопросы:
 2020-04-12
2020-04-12 212
212








