Сложные эфиры жирных кислот и предельных спиртов — жидкости, обладающие приятным фруктовым запахом. Лишь простейшие из них несколько растворимы в воде. Метиловые и этиловые сложные эфиры кипят при более низких температурах, чем соответствующие кислоты.
Химические свойства
Наиболее важной реакцией сложных эфиров язляется реакция омыления, обратная реакции этерификации. Кроме кислот, омыление могут вызывать также и щелочи, с которыми омыление происходит даже лучше, чем с кислотами, причем в данном случае реакция необратима, так как происходит нейтрализация образовавшейся кислоты. В растительном мире весьма распространены энзимы (так называемые эстеразы),обладающие способностью каталитически расщеплять сложные эфиры. Один из таких энзимов — рициназа содержится в семенах клещевины,
Подобно хлорангидридам и ангидридам кислот сложные эфиры являются ацилирующими средствами, хотя еще менее энергичными, чем ангидриды. Так, например, к числу реакций ацилирования можно отнести следующие реакции, идущие с вытеснением спирта из сложного эфира:
1. Переэтерификация
1. Переэтерификация (протекает в присутствии следов кислот, щелочей или алкоголятов):

2. Образование амидов

Сложные эфиры применяются для получения альдегидов, кетонов и спиртов с помощью металлоорганических соединений, а также для получения первичных спиртов восстановлением натрием в спиртовом растворе или литий-алюминийгидридом. Уксусноэтиловый эфир, или этилацетат, и уксусноизоамиловый эфир, или изоамилацетат, находят применение в технике как растворители и для других целей. Этилацетат приготовляется, кроме реакции этерификации, также из уксусного альдегида по реакции В. Е. Тищенко.
Синтетически получаются также некоторые сложные эфиры, имитирующие природные эфирные масла, например искусственные фруктовые эссенции (грушевая эссенция — изоамилацетат, ананасная эссенция — этил- н -бутират, яблочная эссенция — изоамилизовалерат).
Амиды кислот
Амиды кислот могут быть получены нагреванием аммонийных солей кислот, а также действием аммиака на галоидангидриды, ангидриды и сложные эфиры.
Кроме того, амид можно получить присоединением одной молекулы воды к нитрилу:
Физические и химические свойства
За исключением жидкого амида муравьиной кислоты (формамида), остальные амиды — кристаллические вещества. Чистые амиды почти не имеют запаха. Низшие амиды растворимы в воде.
Химические свойства
1. Образование солеобразных соединений Амиды представляют собой нейтральные вещества, так как основные свойства аммиака ослаблены замещением в нем атома водорода кислотным остатком. Поэтому группа NH2 в амидах в отличие от аминов лишь с трудом образует ониевый катион. Все же с сильными кислотами амиды дают соли, например [CH3CONH3]Cl, легко разлагающиеся водой. С другой стороны, водород группы NH2 в амидах легче, чем в аммиаке и в аминах, замещается на металлы. Ацетамид, например, легко растворяет окись ртути, образуя соединение (CH3CONH)2Hg.
Возможно, однако, что при образовании металлических производных происходит изомеризация амида и получающееся соединение имеет изомерное (таутомерное) строение соли имидокислоты

т. е. здесь имеет место аналогия с солями синильной кислоты.
2. Действие азотистой кислоты С азотистой кислотой амиды реагируют, подобно первичным аминам, с образованием карбоновых кислот и выделением азота:

3. Омыление При кипячении с минеральными кислотами и щелочами амиды присоединяют воду, образуя карбоновую кислоту и аммиак:

4. Действие галоидных алкилов. При действии галоидных алкилов на амиды или их металлические производные получаются N-замещенные амиды:

5. Действие пятихлористого фосфора. При действии пятихлористого фосфора на амиды получаются хлорамиды

легко распадающиеся на соляную кислоту и имидхлориды
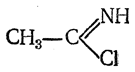
Последние с аммиаком могут давать соли амидинов;

6. Превращение в амины. Энергичным восстановлением амидов могут быть получены первичные амины с тем же числом атомов углерода:

7. Реакция Гофмана. При действии на амиды гипогалогенита или брома и щелочи образуются амины, а углеродный атом карбонильной группы отщепляется в виде СО2 (А. Гофман). Ход реакции можно представить так:

В учебных руководствах до сих пор еще часто встречается другое толкование механизма этой реакции:

Однако такой ход реакции менее правдоподобен, так как образование осколка
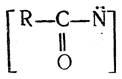
с атомом азота, несущим две свободные электронные пары, мало вероятно.
Против этого механизма говорит, в частности, тот факт, что если радикал R оптически деятельный, то он не рацемизуется в результате реакции. Между тем даже мимолетное существование свободного радикала R–: привело бы к потере оптической деятельности.
Следует подчеркнуть, что в реакциях Гофмана, Курциуса и Лоссена происходят совершенно аналогичные перегруппировки:

Вероятно, все эти перегруппировки имеют сходный механизм.
Вопросы для самоконтроля:
1. Номенклатура производных карбоновых кислот
2. Изомерия
3. Способы получения
4. Физические свойства
5. Химические свойства
Рекомендуемая литература:
1. Перекалин В.В., Зонис С.А. Органическая химия. М.,1982
2. Терней А. Современная органическая химия. М.,1979
3. Петров Е.Е., Бальян Х.В., Трощенко А.Т. Органическая химия. М, 1974
4. Ю. А. Жданова «Очерки методологии органической химии», Изд. «Высшая школа»., М., 1960.
Лекция № 26. Соединения с двумя или несколькими функциями.
Цель: ознакомиться с номенклатурой, методами получения, физическими и химическими свойствами, механизмом реакций соединений с несколькими функциями
Основные вопросы:
1. Непредельные алкилгалогениды.
2. Непредельные кислоты жирного ряда
3. Жиры, строение триглицеридов
4. Мыла, СМС
Краткое содержание.
 2020-04-12
2020-04-12 149
149








