Разряд - сохраняются общие закономерности для цинкового электрода в щелочных растворах. Анодная реакция многоступенчата и может быть описана схемой
Zn 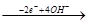 [Zn(OH)4]2–
[Zn(OH)4]2– 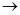 Zn(OH)2
Zn(OH)2 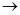 ZnO (10.1)
ZnO (10.1)
Анодное растворение цинка в щелочных электролитах сопровождается образованием цинкатных растворов повышенной против равновесной концентрации цинката. Так, в 10 М растворе КОН химически растворяется 88 г/л цинка, электрохимически — 250 г/л. Образование пересыщенных цинкатных растворов в условиях ограниченного объема электролита приводит к разложению цинкатного комплекса. Выпадающий в осадок оксид цинка характеризуется рыхлой структурой, благодаря чему пассивация электродной поверхности не наступает, хотя и создаются предпосылки для концентрационной поляризации.
Суммарная скорость анодного растворения цинка в щелочи определяется скоростью собственно электрохимического процесса. Максимальный ток в области активного растворения зависит от концентрации щелочи, температуры и конструкции электрода. Цинковые электроды с достаточно развитой поверхностью могут обеспечивать работу при плотностях тока до 3 кА/м2. Процесс анодного растворения цинка прекращается в результате его пассивации. Конечная причина пассивации в условиях ограниченного объема электролита — образование на поверхности электрода уплотненного слоя оксида цинка.
Заряд отрицательного электрода протекает по жидкофазному механизму. Первичным является процесс восстановления тетрагидроцинкат-иона до металлического цинка. Из-за склонности цинка к дендритообразованию структура активной массы получается разветвленной и электрохимически активной. Для того чтобы этот процесс был локализован в порах и не выходил за пределы пластины, используют тесную сборку электродов с минимальным свободным объемом электролита. В противном случае дендриты цинка прорастают сквозь сепаратор и вызывают короткое замыкание электродов.
 2020-04-12
2020-04-12 200
200








