Разряд положительного электрода протекает по сложному механизму. На первой стадии процесса потенциалопределяющей является реакция
2AgO + H2O + 2e–  Ag2O +2OH– E0 = 0,604 В (10.2)
Ag2O +2OH– E0 = 0,604 В (10.2)
После того как поверхность зерен активного вещества покроется тонким слоем оксида серебра (I), потенциалопределяющей становится реакция
Ag2O + H2O + 2e–  2Ag + 2OН– E0 = 0,345 В (10.3)
2Ag + 2OН– E0 = 0,345 В (10.3)
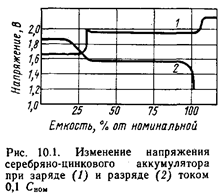
Ёмкость электрода по-прежнему определяется фазой оксида серебра (II). При этом потенциал электрода снижается примерно на 0,25 В. Ступенчатый характер катодной кривой определяет разрядную характеристику СЦ аккумулятора. На рис. 10.1 четко выделяются две ступени напряжения — при 1,85 и 1,55 В.
Заряд серебряного электрода протекает также двухступенчато. На начальном этапе серебро окисляется до оксида серебра (I):
2Ag + 2ОН–  Ag2O + H2O + 2е–
Ag2O + H2O + 2е–
Этой реакции отвечает нижняя площадка на зарядной кривой рис. 10.1. Однако Ag2O является полупроводником с удельной электрической проводимостью ~10–6 См/м, поэтому после образования оксидной пленки (ее толщина ~20 монослоев Ag2O) наступает пассивация электрода. Потенциал повышается примерно на 0,3 В до значения, отвечающего следующему анодному процессу — образованию оксида серебра (II) по суммарной реакции
Ag + 2ОН– 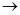 AgO + Н2О + 2е–.
AgO + Н2О + 2е–.
Этот процесс при заряде является преобладающим и соответствует ~70% сообщаемой электроду емкости, что следует из соотношения верхней и нижней площадок зарядной кривой рис. 10.1. К концу заряда в электроде остается до 4% металлического серебра, образующего токопроводящий каркас, а также некоторое количество Ag2O. Коэффициент использования активной массы серебряного электрода составляет от 80 до 60% в зависимости от режима разряда, а отдача по емкости близка 100%.
Окончание заряда четко фиксируется новым подъемом напряжения до площадки, отвечающей процессу электроокисления воды до кислорода.
Самопроизвольное растворение цинка в щелочи — одна из основных причин потери емкости серебряно-цинкового аккумулятора при его длительном хранении в заряженном состоянии. Выделение водорода, сопутствующее этому процессу, затрудняет конструирование герметичного источника тока.
Скорость саморазряда зависит главным образом от перенапряжения выделения водорода на цинковом электроде. При этом первостепенную роль играет степень чистоты цинка и электролита. Наиболее вредны примеси никеля, мышьяка, сурьмы и особенно железа, содержание которого не должно превышать 0,0005% в активной массе и 0,003 г/л в электролите. Введение в цинковый электрод металлической ртути методом амальгамации резко снижает скорость саморазряда. Оптимальное содержание ртути 2%.
 2020-04-12
2020-04-12 271
271








