Для аминов характерна изомерия положения аминогруппы (начиная с С3H9N).
| Например.Формуле С4Н11N соответствуют амины положения аминогруппы. |
| 1-Аминобутан (н -бутиламин) | 2-Аминобутан (втор -бутиламин) |

| 
|
Изомерия между типами аминов
| Например.Формуле С3Н9N соответствуют первичный, вторичный и третичный амины. |
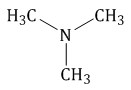
| Пропиламин (первичный амин) | Метилэтиламин (вторичный амин) | Триметиламин (третичный амин) |

| 
|
Физические свойства аминов
При обычной температуре низшие алифатические амины CH 3 NH 2, (CH 3 ) 2 NH и (CH 3 ) 3 N – газы (с запахом аммиака), средние гомологи – жидкости (с резким рыбным запахом), высшие – твердые вещества без запаха.
Ароматические амины – бесцветные жидкости с высокой температурой кипения или твердые вещества.
Первичные и вторичные амины образуют слабые межмолекулярные водородные связи:
Это объясняет относительно более высокую температуру кипения аминов по сравнению с алканами с близкой молекулярной массой.
Амины также способны к образованию водородных связей с водой:

Поэтому низшие амины хорошо растворимы в воде.
С увеличением числа и размеров углеводородных радикалов растворимость аминов в воде уменьшается. Ароматические амины в воде не растворяются.
Химические свойства аминов
| Амины имеют сходное с аммиаком строение и проявляют подобные ему свойства. Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов: |
| Аммиак:NH 3 | Первичный амин R–:NH 2 |

| 
|
| Поэтому амины и аммиак обладают свойствами оснований. |
Основные свойства аминов
| Алифатические амины являются более сильными основаниями, чем аммиак, а ароматические — более слабыми. |
Это объясняется тем, что радикалы СН 3 –, С 2 Н 5 – увеличивают электронную плотность на атоме азота:

Это приводит к усилению основных свойств.
| Основные свойства аминов возрастают в ряду: |

 2020-04-12
2020-04-12 235
235








