1. взаимодействие с активными металлами
2R–OH + 2Na → 2R–ONa + H2↑
алкоголет натрия
2.взаимодействие с кислотами
R–OH + HCl → R – Cl + H2O
галогенпроизводные
3. взаимодействие с другими спиртами
R1–OH + НО – R2 R1 – O–R2 + H2O
простой эфир
Общие способы получения спиртов.
1.гидратация этиленовых углеводородов
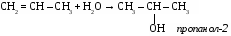
2. гидролиз галогенпроизводных
СН3Cl + NaOH → CH3OH + NaCl
Простые эфиры.
Простые эфиры - органические вещества, в молекулах которых два углеводородных радикала соединены через атом кислорода.
R1–O–R2 – общая формула простых эфиров
Простые эфиры образуются при взаимодействии молекул одного и того же спирта или различных спиртов при нагревании в присутствии серной кислоты.
Упражнение.
Составьте уравнения реакций получения всех простых эфиров, образовавшихся при нагревании смеси метанола и этанола в присутствии серной кислоты, назовите их.
Задача. При сгорании 3,45 г вещества образовалось 6,6 г СО2 и 4,05 г воды. Плотность паров этого вещества по воздуху равна 1,59. Определить молекулярную формулу вещества.
МНОГОАТОМНЫЕ СПИРТЫ.
1. Отдельные представители. Номенклатура

2. Физические свойства этиленгликоля и глицерина.
Этиленгликоль и глицерин бесцветные, прозрачные сиропообразные жидкости. Растворимы в воде, вкус сладкий. Этиленгликоль ядовит.
3. Химические свойства.
Многоатомными спиртам называют производные предельных углеводородов, в молекулах которых содержатся две или более гидроксильные группы.
Свойства многоатомных спиртов сходны со свойствами одноатомных. В реакцию может вступать одна или несколько гидроксильных групп.
Многоатомные спирты реагируют с щелочными металлами с выделением водорода, вступают в реакции замещения с галогеноводородами.

Многоатомные спирты могут образовывать сложные эфиры по всем гидроксильным группам.
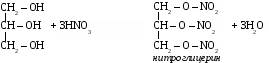
 2020-05-12
2020-05-12 167
167








