Основную роль в образовании третичной структуры играют нековалентные взаимодействия между радикалами аминокислот — водородные, ионные (электростатические), гидрофобные связи (Рис. 2). Аминокислоты, входящие в белки, различаются по физико-химическим свойствам радикалов. Между аминокислотами с неполярными (гидрофобными) радикалами возможны гидрофобные взаимодействия; между полярными радикалами возникают водородные связи, а между заряженными полярными радикалами — ионные. Все эти связи относятся к числу слабых: их энергия в водной среде не слишком сильно превышает энергию теплового движения молекул при комнатной температуре, и поэтому их образование и разрушение — легкообратимые процессы.

Рис. 2. Типы слабых взаимодействий при формировании третичной конформации.
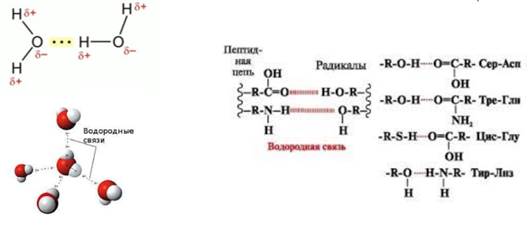
1. Слабые (нековалентные) взаимодействия: водородные связи- это взаимодействие между двумя электроотрицательными атомами полярных или заряженных функциональных групп различных молекул посредством атома водорода А–Н ··· В (где А и В-электроотрицательные атомы: – О, – S или – N).
Рис 3. Водородные связи (в левой части рисунка показаны водородные связи между молекулами воды: в правой части-между радикалами аминокислот).
Водородные связи обусловлены электростатическим притяжением атома водорода, возле которого присутствует локальный положительный заряд (σ+) к атому электроотрицательного элемента, имеющего отрицательный заряд (σ-).
Водородные связи образуются между полярными (гидрофильными) незаряженными группами радикалов АМК, имеющими подвижный атом водорода, и группами с электроотрицательным атомом.
 |
2. Слабые (нековалентные) взаимодействия: электростатические силы притяжения или ионные связи образуются при взаимодействии отрицательно заряженной карбоксильной группы (–СОО-) в составе радикалов Asp и Glu, и положительно заряженной амино (– NH3+) группой в составе основных аминокислот Arg b Lys, или иминогруппой Arg.
Рис. 4. Электростатические (ионные) связи, стабилизирующие третичную структуру белков:
 2020-05-12
2020-05-12 1131
1131
