1. Обозначение ядра. Ядро химического элемента  принято обозначать символом
принято обозначать символом  . Здесь
. Здесь  называют зарядовым числом – оно определяет заряд ядра (
называют зарядовым числом – оно определяет заряд ядра ( ) или порядковый номер элемента в Периодической системе элементов, или число электронов в электрически нейтральном атоме;
) или порядковый номер элемента в Периодической системе элементов, или число электронов в электрически нейтральном атоме;  – массовое число, оно равно суммарному числу протонов (
– массовое число, оно равно суммарному числу протонов (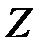 ) и нейтронов (
) и нейтронов (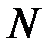 ) в ядре (т. е. числу нуклонов в ядре).
) в ядре (т. е. числу нуклонов в ядре).
2. Типы ядер:
- изотопы – это ядра, с одинаковыми зарядовыми, но разными массовыми числами (у них одинаковое количество протонов, но разное – нейтронов). Так, например, для водорода имеется три изотопа – протий  , дейтерий
, дейтерий  и тритий
и тритий  ;
;
- изобары – это ядра с одинаковыми массовыми, но разными зарядовыми числами (такие ядра могут получаться в ходе b-распада);
- изомеры – ядра с одинаковым числом нейтронов, но разным количеством протонов.
Наличие изотопов приводит к тому, что приводимое в периодической системе элементов Д.И. Менделеева массовое число каждого элемента не является целым. При расчете массового числа химического элемента, учитывается наличие и процентное всех его изотопов.
3. Размеры ядер. Было экспериментально доказано, что радиус ядра зависит от массового числа и эта зависимость имеет вид:
 (6.1)
(6.1)
Рассчитаем с помощью формулы (6.1) плотность ядерного вещества
 . (6.2)
. (6.2)
Из выражения (6.2) видно, что плотность ядерного вещества чрезвычайно велика и не зависит от массового числа (от номера элемента в таблице Менделеева).
 2020-05-21
2020-05-21 179
179








