Образование гормон-рецепторного комплекса при участии регуляторного G-белка активирует мембранную фосфолипазу С, вызывающую гидролиз фосфолипидов мембраны с образованием двух вторичных посредников: инозитол-3-фосфата и диацил глицерола. Инозитол-З-фосфат ведет к выходу Са2+ из внутриклеточных депо. Связывание ионизированного кальция со специализированным белком кальмодулином активирует протеинкиназы и вызывает фосфорилирование внутриклеточных структурных белков и ферментов. Диацилглицерол повышает сродство протеинкиназы С к Са2+, способствуя ее активации, что также завершается процессами фосфорилирования белков. Диацилглицерол одновременно реализует другой путь опосредования гормонального эффекта, активируя фосфолипазу А-2 и образование простаноидов.
ский эффект гормона. Через рассмотренную систему вторичных посредников реализуются эффекты адреналина (при связи с альфа-адренорецептором), вазопрессина (при связи с V-1-рецептором), ангиотензина-II, соматостатина, окситоцина.
4. Система кальций—кальмодулин. Ионизированный кальций поступает в клетку после образования гормон-рецепторного комплекса либо из внеклеточной среды за счет активирования медленных кальциевых каналов мембраны (как это происходит, например, в миокарде), либо из внутриклеточных депо под влиянием инозитол-3-фосфата. В цитоплазме немышечных клеток кальций связывается со специальным белком-кальмодули- ном, а в мышечных клетках роль кальмодулина выполняет тропонин С. Связанный с кальцием кальмодулин изменяет свою пространственную организацию и активирует многочисленные протеинкиназы, обеспечивающие фосфорилирование, а следовательно изменение структуры и свойств белков. Кроме того комплекс кальций—кальмодулин активирует фосфодиэстеразу цАМФ, что подавляет эффект циклического соединения как вторичного посредника. Вызываемое гормональным стимулом кратковременное увеличение в клетке кальция и его связывание с кальмодулином является пусковым стимулом для многочисленных физиологических процессов — сокращения мышц, секреции гормонов и выделения медиаторов, синтеза ДНК, изменения подвижности клеток, транспорта веществ через мембраны, изменения активности ферментов.
6.1.1.2. Взаимосвязи вторичных посредников
В клетках организма присутствуют или могут образовываться одновременно несколько вторичных посредников. В связи с этим между вторичными посредниками устанавливаются различные взаимоотношения: 1) равнозначное участие, когда разные посредники необходимы для полноценного гормонального эффекта; 2) один из посредников является основным, а другой лишь способствует реализации эффектов первого; 3) посредники действуют последовательно (например, инозитол-3-фосфат обеспечивает освобождение кальция, диацилглицерол облегчает взаимодействие кальция с протеинкиназой С); 4) посредники дублируют друг друга для обеспечения избыточности с целью надежности регуляции; 5) посредники являются антагонистами, т. е. один из них включает реакцию, а другой — тормозит (например, в гладких мышцах сосудов инозитол-3-фосфат и кальций реализуют их сокращение, а цАМФ — расслабление).
6.1.2. Механизм действия стероидных гормонов
Стероидные гормоны (рис. 6.3) обладают двумя путями действия на клетки: 1) классическим геномным или медленным и 2) быстрым негеномным.
6.1.2.1. Геномный механизм действия
Геномный механизм действия на клетки-мишени начинается трансмембранным переносом молекул стероидных гормонов в клетку (благодаря их растворимости в липидном бислое клеточной мембраны), с последующим связыванием гормона с цитоплазменным белком-рецептором. Эта связь с рецепторным белком необходима для поступления стероидного гормона в ядро, где происходит его взаимодействие с ядерным рецептором. Последующее взаимодействие комплекса гормон—ядерный рецептор с хроматиновым акцептором, специфическим кислым белком и ДНК влечет за собой: активацию транскрипции специфических мРНК, синтез транспортных и рибосомных РНК, процессинг первичных РНК-транскриптов и транспорт мРНК в цитоплазму, трансляцию мРНК при достаточном уровне транспортных РНК с синтезом белков и ферментов в рибосомах. Все эти явления требуют длительного (часы, сутки) присутствия гормон-рецеп- торного комплекса в ядре.
6.1.2.2. Негеномный механизм действия
Эффекты стероидных гормонов проявляются не только спустя несколько часов, что требуется для ядерного влияния, часть из них проявляется очень
быстро, в течение нескольких минут. Это такие эффекты, как повышение проницаемости мембран, усиление транспорта глюкозы и аминокислот, освобождение лизосомальных ферментов, сдвиги энергетики митохондрий. К числу быстрых негеномных эффектов стероидных гормонов относятся, например, увеличение в течение 5 мин после введения человеку альдостерона общего периферического сосудистого сопротивления и артериального давления, изменение транспорта натрия через мембрану эритроцитов (вообще лишенных ядра) под влиянием альдостерона в опытах in vitro, быстрый вход Са2+ в клетки эндометрия под влиянием эстрогенов и др. Механизм негеномного действия стероидных гормонов заключается в связывании на плазматической мембране клетки со специфическими рецепторами и активации каскадных реакций систем вторичных посредников, например фосфолипазы С, инозитол-3-фосфата, ионизированного Са2+, протеинкиназы С. Под влиянием стероидных гормонов в клетке может увеличиваться содержание цАМФ и цГМФ. Негеномный эффект стероидных гормонов
 |

 |
1 — классический геномный путь действия (гормон проникает через клеточную мембрану и цитоплазму в ядро, где после взаимодействия с ядерным рецептором воздействует на гены-ми- шени, активируя их). 2а и 2б — негеномные пути действия через мембранные рецепторы: 2а — пути, связанные с мембранным ферментом и образованием вторичного посредника, ведущего к активации протеинкиназ. Последние через фосфорилирование в ядре белка-коактиватора (БКА) активируют гены-мишени; 26 — пути, связанные с ионными каналами клеточной мембраны, в результате чего гормон-рецепторный комплекс активирует ионные каналы, меняя возбудимость клетки. 3 — альтернативный негеномный путь действия (молекула гормона, проникая через мембрану в цитоплазму, взаимодействует с цитозольным рецептором, что приводит к активации цитозольных киназ.
может быть реализован и после их связывания с цитоплазматическими рецепторами. Часть негеномных эффектов стероидных гормонов осуществляется благодаря их взаимодействию с рецепторами, связанными с воротным механизмом ионных каналов мембран нервных клеток, являясь тем самым модуляторами, например, глицин-, серотонин- или гамма-аминобу- тиратергических нейронов. Наконец, растворяясь в липидном бислое мембраны, стероидные гормоны могут менять физические свойства мембраны, такие как ее текучесть или проницаемость для гидрофильных молекул, что также является негеномным эффектом.
Таким образом, механизмы действия гормонов разной химической структуры имеют не только различия, но и общие черты. Как и стероиды, пептидные гормоны обладают способностью избирательно влиять на транскрипцию генов в ядре клетки. Этот эффект пептидных гормонов может быть реализован не только с поверхности клетки при образовании вторичных посредников, но и путем поступления пептидных гормонов внутрь клетки за счет интернализации гормон-рецепторного комплекса.
6.L3. Саморегуляция чувствительности эффектора к гормональному сигналу
Изменение характера и интенсивности регуляторных сигналов, поступающих к клетке, ведет к адаптивной перестройке ее рецепторных структур за счет специальных механизмов саморегуляции, изменяющих чувствительность клетки к этому сигналу. Так, при избыточности внеклеточного гуморального сигнала формируется десенситизация соответствующего рецептора, т. е. уменьшение его чувствительности к гуморальному регулятору из-за ослабления сродства рецептора к молекуле лиганда или числа рецепторных молекул. Механизм десенситизации рецепторов, реализующих регуляторный эффект через системы вторичных посредников, представлен на рис. 6.4. При наличии во внеклеточной среде избыточного гуморального сигнала и/или увеличении времени связывания лиганда с рецептором активируемая лиганд-рецепторным взаимодействием протеинкиназа плазматической мембраны фосфорилирует рецептор, в результате его аффинность к лиганду уменьшается в 2—5 раз, что предотвращает чрезмерность регуляторного эффекта. Если этого снижения чувствительности рецептора недостаточно, рецептор фосфорилируется другой протеинкиназой, активируемой соответствующим вторичным посредником. Следствием такого фосфорилирования является нарушение сопряжения рецепторов с G-белками и нарушение эффектов G-белков (активирующих или ингибирующих) на системы вторичных посредников и ионные каналы. Наконец, в случаях недостаточной эффективности двух указанных механизмов десенситизации гормон-рецепторные комплексы интернализуются внутрь клетки с образованием рецепторосомы (вакуоль с рецептором). В последующем, если уровень гуморального регулятора во внеклеточной микросреде снизится в течение 2—3 ч, интернализированный рецептор может вновь встроиться в мембрану, а если повышенная концентрация регулятора сохраняется — рецепторосомы сливаются с лизосомами и рецепторы разрушаются. Десенситизация рецепторов может быть гомологической, проявляющейся в снижении чувствительности только к тому гуморальному регулятору, избыток которого ее вызвал, и гетерологической, заключающейся в снижении чувствительности и к другим гуморальным факторам регуляции, но также реализующим эффект через связанные с G-белком рецепторы и те же вторичные посредники.
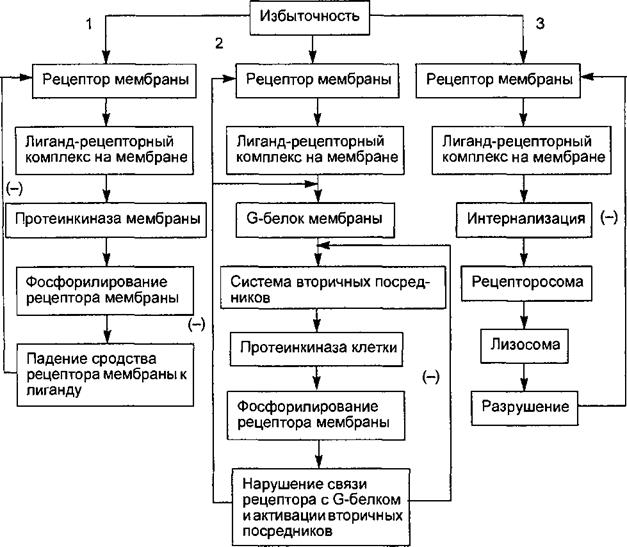
Рис. 6.4. Схема трех путей десенситизации клетки к избыточному внешнему регуляторному сигналу.
1. Снижение сродства рецептора к лиганду из-за фосфорилирования рецептора мембранной протеинкиназой. 2. Нарушение связи молекулы рецептора с G-белком при фосфорилировании рецептора цитоплазматическими протеинкиназами. 3. Интернализация лиганд-рецептор- ного комплекса и разрушение рецептора ферментами лизосом. Стрелками со знаком (—) обозначено подавление процесса взаимодействия.
Чувствительность клеток к внешним регуляторным сигналам зависит также и от числа так называемых свободных, или резервных, рецепторов, т. е. доступных для лиганда. Увеличивая синтез этих мембранных структур или их «всплывание» на поверхность мембраны, клетка способна повышать чувствительность к регуляторному сигналу (сенситизация), например в случаях недостаточного количества молекул гуморального регулятора во внеклеточной микросреде. Повышение чувствительности к регуляторному сигналу является также следствием возросшего сопряжения рецепторов с G-белком и системой вторичных посредников.
Клетки организма, как правило, используют не один, а несколько путей реализации одного гуморального регуляторного сигнала, в связи с чем для каждого лиганда (например, молекул одного гормона) на мембранах существуют несколько типов рецепторов. Так, для ацетилхолина, гистамина, катехоламинов, опиоидных пептидов, серотонина, вазопрессина иденти
фицировано два (вазопрессин), три (опиоиды), четыре (мускариновые для ацетилхолина) и более (катехоламины, серотонин) мембранных рецепторов. Соответственно, меняя за счет саморегуляции чувствительность рецепторов одного типа, клетка изменяет характер функционирования и способна компенсировать неадекватные сдвиги в регуляторных влияниях.
Одним из регуляторных эффектов, реализуемых внутри клетки с помощью систем вторичных посредников мембранного лиганд-рецепторного взаимодействия, является изменение функционального состояния генома клетки и биосинтеза белка. Но и ядро клетки способно менять состояние плазматической мембраны, ее чувствительность к сдвигам внеклеточной среды, в том числе и изменению в ней количества и характера регуляторных сигналов. В клетках под контролем генома происходит синтез специальных белков — инверторов, оказывающих различное влияние на функциональное состояние мембраны в зависимости от адаптивно-компенсаторных потребностей клетки — изменение активности рецепторов, состояния ионных каналов и насосов. Эти белки могут вести к гиперполяризации клеточной мембраны, ослаблению функциональной активности клетки, с одновременным повышением синтеза белка и процессов регенерации внутриклеточных структур.
 2020-05-25
2020-05-25 340
340








