1. Общие сведения о влиянии внешних факторов на скорость коррозии.
2. Влияние скорости движения жидкости и ее состава на скорость коррозии.
3. Влияние концентрации электролита на скорость коррозии.
4. Влияние давления на скорость коррозии
6. Графики зависимости скорости от каждого внешнего фактора.
6. Анализ полученных данных и выводы по работе.
Лабораторная работа №5 Изучение влияния внешних примесей и времени эксплуатации на параметры коррозионных процессов стали.
Цель работы: проанализироватьзависимости влияния химического состава стали и длительность эксплуатации на скорость коррозии
Теоретическая часть
а. Общиесведения
Большое влияние на коррозионную стойкость оказывает способ её производства вследствие различия в химическом составе, обусловленном особенностями этих способов и назначается получаемой стали.
Состав железоуглеродистых сплавов может по–разному сказывается на их коррозионной стойкости.
Из трёх основных структурных составляющих железоуглеродистых сплавов (феррита, цементита и графита); феррит обладает наименьшей коррозионной стойкостью, а графит – наибольшей. Цементит и графит обычно имеют в электролитах более положительные потенциалы, чем феррит, и является по отношению к нему катодами.
В процессе выплавки в железоуглеродистые сплавы попадают сера, фосфор, кремний, марганец, а иногда медь, хром и никель.
Повышение содержания в железоуглеродистых сплавов катодного компонента – углерода, увеличивает скорость их коррозии в непассивирующих растворах кислот за счёт снижения перенапряжения водорода меньше влияет на скорости коррозии в неподвижных нейтральных средах и уменьшает скорость коррозии, способствуя пассивированию сплавов в определённых условиях (преобладание анодного контроля).
Сера заметно снижает коррозионную стойкость железоуглеродистых сплавов в кислотах и атмосфере: участки защитной плёнки около сернистых включений FeS и MnS защищает сплав хуже, чем нормальная окисленная плёнка. Кроме того, сульфиды, разрушаясь в электролите, образуют сероводород, который заметно повышает скорость коррозии.
Фосфор несколько повышает стойкость железоуглеродистых сплавов против атмосферной коррозии, особенно при наличии в них меди и хрома.
Кремний при наличии его в стали в количестве 0.1… 0.1% и в чугунных 1…2% не оказывает влияния на коррозионную стойкость, а при содержании свыше 1% в стали и 3% в чугуне несколько понижает стойкость в связи с ухудшением по отношении к щелочам защитных свойств плёнки, содержащей окись кремния.
Коррозионная стойкость железоуглеродистых сплавов повышается только при высоком содержании кремния (порядка 14%), что соответствует второй границе устойчивости твёрдых растворов, т. е. 2/8 атомной доли.
Марганец практически мало влияет на коррозионную стойкость.
Медь заметно повышает коррозионную стойкость в атмосфере и в воде, не содержащую депассивирующих ионов (например, Сl), даже при незначительном её содержании (рис.8)
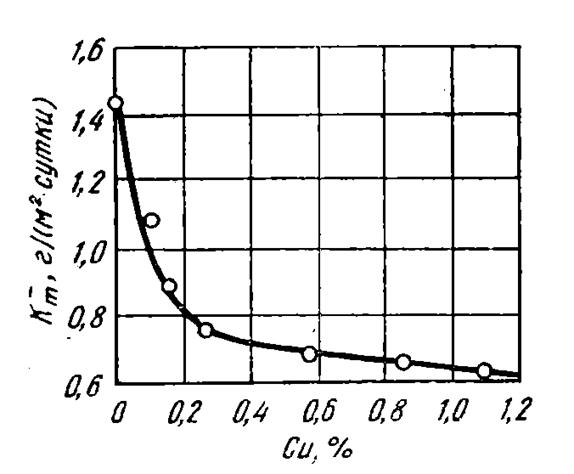
Рисунок 8- Влияние содержания меди на скорость атмосферной коррозии стали.
Хром как элемент легкопассивирующийся несколько увеличивает коррозионную стойкость, а при одновременном легировании их медью этот эффект ещё значительнее. С повышением содержания хрома коррозионная стойкость сплавов в различных средах растёт. При достаточно высоком легировании хромом (>13%), получают коррозионностойкие стали.
Никель в небольшом количестве почти не влияет на коррозионную стойкость. С увеличением содержания никеля возрастает стойкость сплавов в щелочных средах.
Термообработка железоуглеродистых сплавов почти не влияет на их коррозионную стойкость в атмосферных условиях, заметно изменяет её в нейтральных водных растворах (коррозия с кислородной деполяризацией) и очень сильно – в кислых растворах (коррозия с водородной деполяризацией) (рисунок 0)
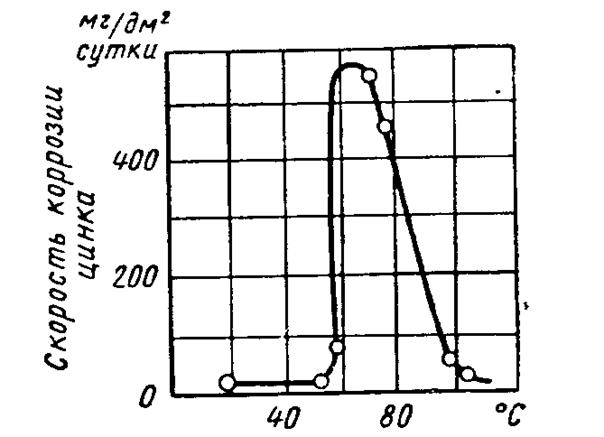
Рисунок 9- Влияние термообработки на коррозионную стойкость металла (цинк).
Изотермическая обработка повышает коррозионную стойкость железоуглеродистых сталей в кислых растворах по сравнению с обычной закалкой и последующим отпуском, что связано с образованием пластинчатых или игольчатых структур (перлит, бейнит), соответствующих коррозионную стойкость, близкую к таковой у сплавов, закалённых на мартене.(таблица 10)
| Вид термообработки | Потери массы за 1100г, г/м2 | |
| Сталь Ст2 | Сталь 15ХСНД | |
| Отжим при 680 0С на зернистый перлит. Закалка в воду с 640 0С Закалка в воду с 1100 0С | 58.6 25.2 26.3 | 27.7 - 12.4 |
Т а б л и ц а 10 Коррозионная стойкость сталей
Хорошие результаты достигаются при одновременном легировании углеродистой стали медью и хромом, а также медью, хромом и никелем.
Небольшие добавки к стали 15 ХСНД титана (0.02 – 0.05%) повышают её прочность и свариваемость, а присадка фосфора (0.13 – 0.15%) заметно увеличивает её коррозионную стойкость.
В связи с малой коррозионной стойкостью железоуглеродистых сплавов их сравнительно редко применяют незащищёнными в растворах кислот и щелочей.
Выполнение работы
Суть работы в том, что на основании литературных опытных данных строят зависимости влияния химического состава стали и длительность эксплуатации на скорость коррозии.
1. Установить содержания углерода на скорость коррозии железоуглеродистых сплавов:
Т а б л и ц а 11 Данные к работе
| Материал | % С | Vкор. г/м2 • ч |
| Железо Сталь 20 Сталь 45 Сталь 98 Серый чугун | 0.024 0.20 0.47 0.87 3.2 | 0.46 0.68 1.41 2.82 43.7 |
1.1. Постройте график зависимости скорости коррозии от содержания углерода в сплаве.
1.2. Объясните характер изменений скорости коррозии, увязав его со структурными составляющими и положительным потенциалом фаз (феррит, цементит, графит)
1.3. Сделайте практические выводы и рекомендации.
2. Установить влияние основных примесей (S, P, Si) на скорость коррозии углеродистой стали.
Т а б л и ц а 12 Данные к работе
| % S | Vк, г/ь2 сут. | % P | Vк, г/м2 сут. | % Si | Vк, г/м2 сут. |
| 0.05 0.1 0.12 0.15 | 600 900 1000 1250 | 0.05 0.08 0.1 | 300 500 550 | 0.05 0.1 0.15 | 50 50 50 |
2.1. Построите общий график зависимости скорости коррозии от содержания в S,P и Si в сплаве.
2.2. Объясните силу влияния каждой примеси на коррозионную стойкость сплава и характер хода кривых.
2.3. Сделайте практические выводы и рекомендации.
3. Установить влияние химического состава стали и длительности эксплуатации на скорость коррозии.
3. Данные к работе (таблица 13):
I – низколегированная сталь
II – 3.2 % Ni; 0.02% Р
III – 0.2 % Cu; 0.11% Р
IV – 0.2 % Cu 0.006% Р
Т а б л и ц а 13 Данные к работе
| Годы | Потери массы кг/м2 год | |||
| I | II | III | IV | |
| 1 | 0,25 | 0,3 | 0,5 | 0,55 |
| 2 | 0,32 | 0,38 | 0,6 | 0,7 |
| 3 | 0,35 | 0,4 | 0,63 | 0,8 |
| 4 | 0,37 | 0,42 | 0,65 | 0,83 |
| 5 | 0,38 | 0,45 | 0,7 | 0,9 |
| 6 | 0,40 | 0,5 | 0,75 | 0,92 |
| 7 | 0,42 | 0,52 | 0,77 | 1,0 |
| 8 | 0,43 | 0,55 | 0,79 | 1,05 |
3.1 Построите обобщённый график зависимости скорости коррозии от времени эксплуатации для каждой стали (I, II, III и IV)
3.2 Объясните характер хода кривых на графике, обратив внимание на возрастание скорости коррозии в начальный период эксплуатации и её замедление в последующий период. Связать это явление с характером и свойствами окисленных плёнок.
3.3. Сделайте практические выводы и рекомендации.
 2020-06-12
2020-06-12 196
196








