Программа
Закон сохранения и превращения энергии. Калорические параметры. Внутренняя энергия. Энтальпия и энтропия как функции состояния тела. Теплота и работа как функции процесса. Выражение теплоты и работы через термодинамические параметры состояния. Рабочая (p - v) и тепловая (T - s) диаграммы. Графическое изображение работы и теплоты.
Первый закон термодинамики, его содержание и формулировки. Две формы аналитического выражения первого закона термодинамики.
Методические указания. Калорические параметры характеризуют тепловым (энергетическим) состоянием тела или системы. Внутренняя энергия u – это энергия хаотического движения молекул тела. Энтальпия i (h) включает в себя энергию движения молекул и работу, которую совершает газ объемом v при внесении его в среду с давлением р (i = u + p×v). Энтропия s характеризует степень теплового взаимодействия тела с окружающей средой. Она изменяется только тогда, когда происходит теплообмен.
При изучении данной темы студент должен понять, что, несмотря на то, что работа и теплота - два различных способа передачи энергии, общее их свойство - передача энергии, оно может происходить только во время процесса - при чередовании параметров состояния рабочего тела. При этом должно быть условие протекания процесса (движущая сила) и его результат - изменение характерной для этого процесса свойства.Так, чтобы происходил теплообмен, нужны тела с разной температурой, то есть температура (Т) является потенциалом, движущей силой теплообмена; чтобы совершалось работа, нужно силовое воздействие, возникающее при разнице давления, то есть давление (р) является потенциалом, движущей силой механического воздействия - работы.
В результате силового взаимодействия происходит изменение объема тела, и оно выполняет работу l = ò p´ d v.
В результате теплового взаимодействия происходит изменение энтропии тела - передается теплота q = ò T ´ d s (см.рис.1).
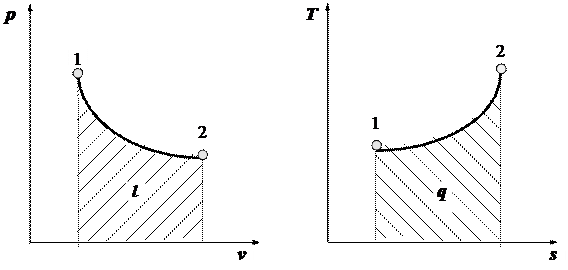
а) б)
Рисунок 1 – Графическое определение работы в рабочей (а) и теплоты в тепловой (б) диаграммахпри произвольном термодинамическом процессе 1-2
Площадь, ограниченная линией процесса 1-2, осью v и координатами, проведенными на нее из точек 1 и 2, является графическим изображением работы в координатах p - v. Площадь, ограниченная линией процесса 1-2, осью s и координатами, проведенными на нее из точек 1 и 2, является графическим изображением теплоты в координатах T - s. Согласно этому, диаграмма p - v получила название рабочей, а диаграмма T - s – тепловой.
Две формы аналитического выражения первого закона термодинамики:
d q = d u + p × d v, d q = d i - v× d p.
 2020-06-08
2020-06-08 104
104








