К истинным растворам относят многокомпонентные системы, не имеющие поверхностей раздела фаз. В них одни вещества распределены в среде других на молекулярном или ионном уровне (что не исключает существования в растворах ассоциатов молекул и ионов). Растворами называют однофазные системы, состоящие из двух и более компонентов, состав которых можно изменять в некоторых пределах без выделения новой фазы.
Истинные растворы образуются самопроизвольно за счет сил межмолекулярного взаимодействия между растворителем и растворяемым соединением. Процесс растворения невозможно отнести к чисто физическому смешиванию различных компонентов. Он сопровождается тепловым эффектом, а объем раствора не равен сумме объемов смешиваемых компонентов. Исследования показали, что в составе растворов часто присутствуют сольваты (для водных растворов – гидраты)определенного состава, например, в растворах серной кислоты H2SO4.H2O, H2SO4.2H2O. Эти признаки характерны для протекания химических реакций. Таким образом, истинные растворы занимают по своей природе промежуточное положение между механическими смесями и продуктами химической реакции.
Если при растворении нет теплового эффекта, а объем раствора равен сумме объемов компонентов, то такой раствор называют идеальным. Идеальные растворы рассматривают для теоретического вывода законов о поведении растворов.
Для выражения состава растворов применяют следующие формулы.
Массовая доля:
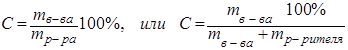 . (8.1)
. (8.1)
Молярная концентрация:
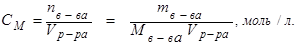 (8.2)
(8.2)
Эквивалентная концентрация:
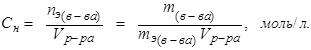 (8.3)
(8.3)
Моляльная концентрация:
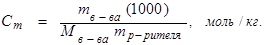 (8.4)
(8.4)
Мольная доля:
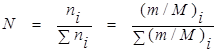 . (8.5)
. (8.5)
Титр раствора, широко применяемый в аналитической химии:
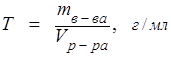 . (8.6)
. (8.6)
 2020-06-08
2020-06-08 124
124








