Na2S2O3 + H2SO4 = Na2SO4 + H2O + SO2 + S↓
Часть 1. Исследование зависимости скорости реакции от концентрации тиосульфата натрия при постоянных температуре и концентрации серной кислоты. Определение порядка реакции по тиосульфату натрия:
v = kC c xC к y; C к – const.
Т а б л и ц а 2
Зависимость скорости реакции от температуры.
Результаты измерений и расчетов
| С с | V c | V в | V к | τ | v | v ·10–2 |
| моль/л | мл | мл | мл | с | с–1 | с–1 |
| 0,1 | 5 | 15 | 5 | 82 | 0,0122 | 1,22 |
| 0,2 | 10 | 10 | 5 | 42 | 0,0238 | 2,38 |
| 0,3 | 15 | 5 | 5 | 28 | 0,0357 | 3,57 |
| 0,4 | 20 | 0 | 5 | 21 | 0,0476 | 4,76 |
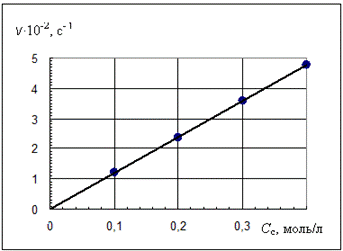
Рис. 1. Зависимость скорости реакции от концентрации соли
Вывод: (о влиянии концентрации соли на скорость реакции).
Часть 2. Исследование зависимости скорости реакции от температуры при постоянных концентрациях реагентов. Определение энергии активации реакции Ea и температурного коэффициента γ.
C c = ___ моль/л; V с = ___ мл; V воды = ___ мл; V к = ___ мл.
Т а б л и ц а 2
Зависимость скорости реакции от температуры.
Результаты измерений и расчетов
| t | T | 1/ T | (1/ T)·10–3 | τ | v | v ·10–2 | ln v |
| ºC | K | K–1 | K–1 | c | c–1 | c–1 | – |
| 12 | 285 | 0,00351 | 3,51 | 134 | 0,00746 | 0,75 | –4,89784 |
| 21 | 294 | 0,00340 | 3,40 | 82 | 0,0122 | 1,22 | –4,40672 |
| 40 | 313 | 0,00319 | 3,19 | 33 | 0,0303 | 3,03 | –3,49651 |
| 60 | 333 | 0,00300 | 3,00 | 14 | 0,0714 | 7,14 | –2,63906 |
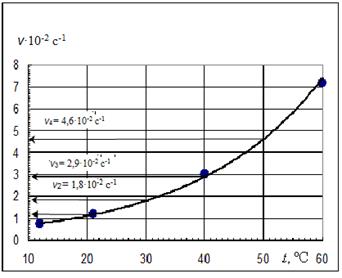
Рис. 2. Зависимость скорости реакции от температуры
v 1 = 1,2·10–2 с–1, v 2 = 1,8·10–2 с–1, v 2 = 2,9·10–2 с–1, v 2 = 4,6·10–2 с–1
γ1 = v 2/ v 1 = 1,50
γ2 = v 3/ v 2 = 1,61
γ3 = v 4/ v 3 = 1,58
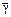 =1,59
=1,59
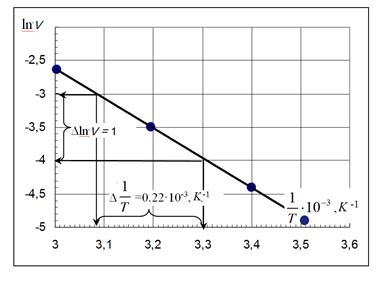
Рис. 3. Зависимость логарифма скорости от обратной температуры
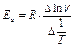 =
= 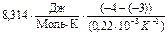 = 37790 Дж/моль = 37,8 кДж/моль
= 37790 Дж/моль = 37,8 кДж/моль
Выводы: (о влиянии температуры на скорость реакции)
С О Д Е Р Ж А Н И Е
Правила техники безопасности................................................................................. 3
Краткие сведения из теории....................................................................................... 3
Лабораторная работа.................................................................................................. 6
Шаблон отчета............................................................................................................ 12
Пример заполнения отчета......................................................................................... 16
Киселев Алексей Петрович, Лебедев Виктор Николаевич,
Фатина Александра Анатольевна
Кинетика химических реакций
Редактор Г.М. Звягина
Корректор Л.А. Петрова
Компьютерная верстка: Н.А. Андреева
Подписано в печать 15.04.2016. Формат 60×84/16. Бумага документная.
Печать трафаретная. Усл. печ. л 1,2. Тираж 200 экз. Заказ № 74
Балтийский государственный технический университет
Типография БГТУ
190005, С.-Петербург, 1-я Красноармейская ул., д. 1
 2020-06-10
2020-06-10 98
98







