Задание 1
Из чего можно получить больше этилового спирта: из 1 кг глюкозы или 1 кг крахмала? Ответ обоснуйте, не прибегая к расчетам.
Ответ: из 1 кг крахмала, т.к. при его гидролизе образуется больше спирта, чем 1 кг глюкозы. Крахмал- полимер, мономерами которого являются молекулы глюкозы.
Задание 2
В среднем сладкоежки кладут 2 чайные ложки сахара на стакан чая. Зная, что в такой ложке помещается 7 г сахара, а объем стакана 200 мл, рассчитайте массовую долю сахарозы в растворе (плотность чая считать равной 1 г/мл).
Решение:
m (двух чайных ложек сахара) = 7+7= 14г;
m (чая) = ρ. V = 1г/мл ٠ 200мл = 200г;
m (раствора чая) = m (чая) + m (двух чайных ложек сахара) = 200г + 14г = 214г;
ω (сахарозы) = m (двух чайных ложек сахара). 100% / m (раствора чая) = 14г ٠100% / 214г = 6,5%.
Ответ: ω (сахарозы) = 6,5%.
Задание 3
С помощью каких реакций можно осуществить следующие превращения:
Сахароза 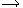 глюкоза
глюкоза 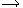 глюконовая кислота?
глюконовая кислота?
сахароза 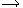 глюкоза:
глюкоза:
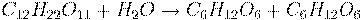
глюкоза 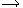 глюконовая кислота
глюконовая кислота
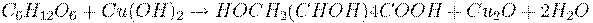
(реакцию проводить при нагревании!)
Резервное задание:
демонстрация опыта
В органическом анализе есть одна замечательная качественная реакция на углеводы. В нее вступают любые сахара: моно-, олиго-и полисахариды, растворимые и нерастворимые в воде, альдозы и кетозы, восстанавливающие и невосстанавливающие. Эта реакция называется пробой Молиша. Если в распоряжении учителя есть спиртовой раствор какого-либо из перечисленных ароматических гидрокси-соединений (резорцин, тимол, а-нафтол), он сумеет показать детям эту красивую реакцию.
В чисто вымытую пробирку наливают 1 мл воды и добавляют несколько крупинок сахарозы, или кристалликов глюкозы, или кусочек фильтровальной бумаги (целлюлоза). В раствор добавляют 2-3 капли раствора резорцина.
Пробирку закрепляют в штативе наклонно и по стенке осторожно наливают 1-2 мл концентрированной серной кислоты.
Пробирку поворачивают в вертикальное положение. В месте соприкосновения серной кислоты с водным раствором появляется красивое ярко-красное кольцо, свидетельствующее о наличие в исследуемой пробе углевода.
Итог:
Мы рассмотрели классификацию углеводов, физические и химические свойства глюкозы, ее реакции окисления (с гидроксидом меди (II), аммиачным раствором нитрата серебра), восстановления (водородом), особое свойство глюкозы – реакции брожения.
Домашнее задание:
1. Решить задачу: Даже великие химики нередко ошибались. Одним из первых определил элементный состав сахарозы А. Л. Лавуазье и получил следующие результаты: углерод — 28%, водород — 8%, кислород — 64%. Вычислите действительное содержание этих элементов в сахарозе, зная ее молекулярную формулу С12Н22О11.
2. Как распознать при помощи одного реактива глицерин, уксусный альдегид, уксусную кислоту, глюкозу? Напишите уравнения реакций
Литература:
1. Габриелян О. Химия 10кл.: Учебник для общеобразовательных учреждений. -М.:Дрофа,2009.-304с.
2. Габриелян, О. С., Остроумов, И. Г. Настольная книга учителя химии. 10 класс. - М.: Дрофа, 2001.-536с.
3. Кузьменко Н. Е., Еремин В. В. Начала химии. Современный курс для поступающих в ВУЗы.- М.: «Экзамен», 2001.-720с.
 2020-06-10
2020-06-10 311
311







