Практически все соединения щелочных металлов растворимы, поэтому для их качественного определения используют метод окраски пламени. При внесении металла или его соединений в пламя горелки, пламя окрашивается в определённый цвет (рисунок 1). На рисунке приведены цвета пламени для важнейших щелочных и щелочноземельных металлов, которые необходимо знать по школьной программе.

Рисунок 1 – Окраска пламени в присутствии щелочных и щелочноземельных металлов*
Применение соединений натрия и калия
NaCl – в пищевой промышленности (cоль пищевая, консервант); в медицине (приготовление физиологического раствора).
NaNO2 – в пищевой промышленности (улучшитель окраски и консервант в изделиях из мяса и рыбы).
KNO3, KCl и другие соединения калия – используют в сельском хозяйстве в качестве удобрения. Калий является одним из трех базовых элементов, которые необходимы для роста растений, наряду с азотом и фосфором.
Na2CO3, К2CO3, Na2SO4 – используют в производстве стекла, эмалей и глазурей. Получение обычного стекла сводится к уравнению:
| Na2CO3 + | СаCO3 + | 6 SiO2 = | Na2O × СаO × 6 SiO2 + 2CO2 |
| кальц. сода | мел | кварцевый песок |
В случае использования более дешевого сульфата натрия, к исходным веществам добавляют уголь:
Na2SO4 + СаCO3 + 6 SiO2 + С = Na2O × СаO × 6 SiO2 + CO2 + СО + SO2
Щелочноземельные металлы
Все элементы этой подгруппы – активные металлы, сильные восстановители. Раньше Be и Mg не относили к щёлочноземельным металлам, в настоящее время, согласно определению ИЮПАК, все металлы II группы главной подгруппы называются щелочноземельными. К числу наиболее распространенных элементов относятся кальций и магний.
Получение II группы главной подгруппы
Из-за высокой активности металлы II группы главной подгруппы получают электролизом расплавов их солей, реже – металлотермией:
CaCl2 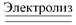 Ca + Cl2
Ca + Cl2
катод анод
3BaO + 2Al = 3Ba + Al2O3
BeF2 + Mg = Be + MgF2
 2020-06-29
2020-06-29 250
250