Шкала перевода первичного балла за выполнении контрольной работы в отметку по 5-ной шкале
| Отметка по 5-ной шкале | 2 | 3 | 4 | 5 |
| Первичный балл | 0-10 | 11-15 | 16-21 | 22-24 |
Инструкция по выполнению работы.
На выполнение итоговой работы по биологии дается 40 минут. Работа состоит из 10 заданий.
При выполнении заданий 1-5 запишите ответ так, как указано в тексте задания.
При выполнении заданий 6-10 запишите сначала номер задания, а затем ответ к нему.
Советуем выполнять задания в том порядке, в котором они даны. Баллы, полученные Вами за выполненные задания, суммируются. Постарайтесь выполнить как можно больше заданий и набрать наибольшее количество баллов.
Итоговая контрольная работа по химии для обучающихся 9 класса
Вариант 1.
При выполнении заданий 1-2 выберите правильные ответы и запишите выбранные цифры в порядке возрастания.
1. В ряду элементов кремний —> алюминий —> магний
1) увеличивается число электронных слоёв в атоме
2) уменьшается число электронов во внешнем слое атома
3) уменьшается степень окисления в высших оксидах
4) ослабевают металлические свойства
5) уменьшается радиус атома
2. Азот- простое вещество:
1) является газом
2) относится к металлам
3) растворяется в воде
4) в обычных условиях химически инертен
5) составная часть оболочек растительных клеток
В заданиях 3-5 установите соответствие и запишите в таблицу цифры выбранных вами ответов. Цифры в ответе могут повторяться.
Установите соответствие между схемой превращения и изменением степени окисления восстановителя в ней.

Установите соответствие между веществом и реагентами, с которыми оно может вступать в реакцию.

Установите соответствие между формулами нитратов и продуктами их разложения.
формулы солейпродукты разложения
А) KNO3 1) Ag, NO2, O2
Б) Cu(NO3)22) Cu, NO2, O2
В) AgNO3 3) CuO, NO2, O2
KNO2, O2
Ag2O, NO2, O2
В заданиях 6-10 запишите сначала номер задания, а затем решение и ответ к нему.
Дана схема превращений:Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения.Для второй реакции составьте сокращенное ионное уравнение.
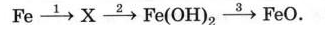
7. Мрамор – является одним из самых популярных природных камней, известных во всём мире. Люди любуются и восхищаются фантастической красотой изделий из мрамора на протяжении многих веков. Ценность определяется его необычной структурой, богатым многообразием цветовой гаммы и неповторимостью рисунка, это делает его уникальным. Мрамор славится своей долговечностью, прочностью, стойкостью к перепадам температур и влажности. Мрамор состоит из кальцита с примесями других минералов, а также органических соединений. Примеси различно влияют на качество мрамора, снижая или повышая его декоративность. Окраска, также зависит от примесей. Большинство цветных мраморов имеет пёструю или полосчатую окраску. Оксид железа окрашивает его в красный цвет, высокодисперсный сульфид железа — в сине-чёрный, железосодержащие силикаты— в зелёный, лимонит (гидроксиды железа) и карбонаты железа и марганца — в жёлтые и бурые тона. Серые, голубоватые и чёрные цвета могут быть обусловлены также примесями битумов или графита. Напишите химическую формулу мрамора и рассчитайте массовую долю углерода.
8. Вычислите массу осадка, образующегося при сливании 200 г 20% -го раствора гидроксида натрия с раствором, содержащим избыток сульфата меди (II).
9. На занятиях химического кружка учащиеся исследовали бесцветный прозрачный раствор. Раствор разделили на две порции. К первой порции исследуемого раствора добавили раствор карбоната натрия, при этом выделился газ без цвета и запаха, в котором горящая лучинка гаснет. При добавлении нитрата бария ко второй порции исследуемого раствора образовался осадок белого цвета, нерастворимый в кислотах.
Определите состав вещества, образующего исследуемый раствор, и запишите его название. Составьте два уравнения реакций, которые были проведены учащимися в процессе его распознавания.
10. Составьте уравнения реакций, соответствующие следующим схемам и определите тип каждой реакции. В окислительно- восстановительной реакции определите окислитель и восстановитель, процессы окисление и восстановление.:
a) HCl®H2®Cu
1)___________________________ - реакция ___________________________;
2) ___________________________ - реакция ___________________________.
б) H2O®H2®HCl®MgCl2
1)__________________________ - реакция ___________________________;
2) __________________________ - реакция ___________________________;
3) __________________________ - реакция ____________________________.
Вариант 2.
При выполнении заданий 1-2 выберите правильные ответы и запишите выбранные цифры в порядке возрастания.
1. В ряду элементов литий —>берилий —> бор
1) увеличивается число электронных слоёв в атоме
2) уменьшается число электронов во внешнем слое атома
3) уменьшается электроотрицательность
4) ослабевают металлические свойства
5) уменьшается радиус атома
2. Выберите верные суждения:
1) Молоко является чистым веществом
2) Хлор- ядовитый газ
3) Кислород и озон являются аллотропными формами
4) Методом вытеснения воздуха в открытый стакан нельзя собрать углекислый газ
5) Отходы, образующиеся при использовании металлического натрия, уничтожают водой
 2020-07-01
2020-07-01 1177
1177