В стаканы емкостью 50 мл внесли соответственно 0,5;1;1,5; 2 и 2,5 мл стандартного раствора CaSO4 добавили дистиллированной воды до 25 мл. Подкислили соляной кислотой до pH = 3 по pH - метру. Добавили 2 мл защитного коллоида. Прилили 5 мл раствора BaCl2 из пипетки при непрерывном движении ее кончика по спирали внутри раствора. Раствор перенесли в мерную колбу емкостью 50 мл, довели дистиллированной водой до метки и перемешали.
Измерили оптическую плотность раствора при ранее выбранном светофильтре. По результатам измерений построили градуировочный график зависимости А от С (SO42-), мг/мл.
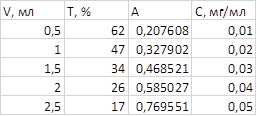
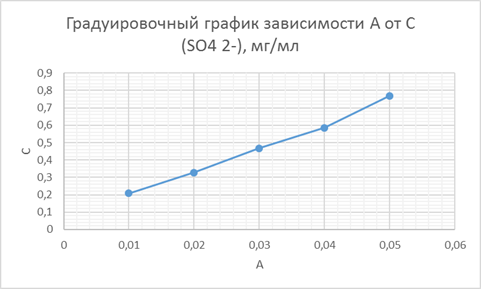
Определение сульфат — иона в водопроводной воде
В стакан емкостью 50 мл внесли 10 мл водопроводной воды. Подкислили соляной кислотой до pH = 3 по pH – метру. Добавили 2 мл защитного коллоида. Прилили 5 мл раствора BaCl2 из пипетки при непрерывном движении ее кончика по спирали внутри раствора. Раствор перенесли в мерную колбу емкостью 50 мл, довели дистиллированной водой до метки и перемешали. Измерили оптическую плотность раствора при ранее выбранном светофильтре. Повторили опыт не менее 3-х раз.
Определили содержание сульфат — иона по градуировочному графику. Дали интервальную оценку сульфат — иона в массовых и мольных концентрациях.
Статистическая обработка для массовой концентрации сульфат-ионов в воде:
С1 = 0.0163 мг/мл
С2 = 0.017 мг/мл
С3 = 0.0163 мг/мл
Сср = 0.0165 мг/мл
S = 0.0003
ΔС = 0.0007 мг/мл
С±ΔC = (0.0165±0.0007) мг/мл
Концентрация сульфат-ионов по формуле:
С [моль/л] = С [мг/мл] / М [г/моль] (SO42-)
Статистическая обработка для молярной концентрации сульфат-ионов в воде:
С1 = 0.00017 моль/л
С2 = 0.00018 моль/л
С3 = 0.00017 моль/л
Сср = 0.000173 моль/л
S = 0.000003
ΔС = 0.000007 моль/л
С = (0.000175±0.000007) моль/л
Концентрация сульфат-ионов:
С [моль/л] = С [мг/мл] / М [г/моль] (SO42-)
Статистическая обработка для молярной концентрации сульфат-ионов в воде:
С1 = 0.00017 моль/л
С2 = 0.00018 моль/л
С3 = 0.00017 моль/л
Сср = 0.000173 моль/л
S = 0.000003
ΔС = 0.000007 моль/л
С±ΔC = (0.000175±0.000007) моль/л
Выводы
1. Изучено: турбидиметрический анализ. Оптическая плотность раствора на фотоколориметре КФК. λmax = 315нм.
2. Размер частиц золя сульфата бария измеренные графическими и математическим способами:
Графически: r = 160
Математически: r = 160
С(ср)±ΔC = (0,026±0,001) мг/мл,
С(ср)±ΔC = (0.00027±0,00001) моль/л.
3. По ГОСТу 4389-72 содержание сульфатов в воде не должно быть выше 5 мг/мл. На основании полученных данных сделали вывод, что наша вода пригодна к использованию.
 2020-07-12
2020-07-12 553
553







