1.Окисление или окислительное дегидрирование спиртов
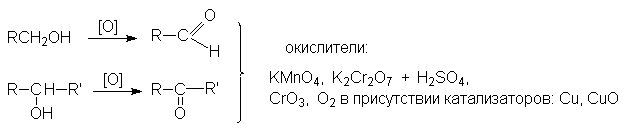
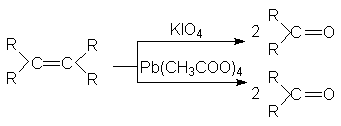
2Окисление алкенов Pb(OOCCH3)4 и KIO4
3.Гидратация алкинов
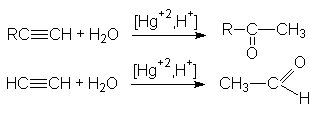
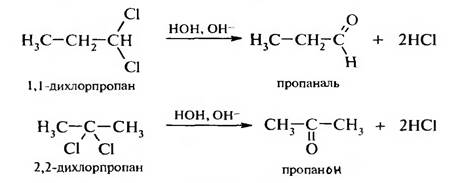
4.Гидролиз геминальных (1,1) дигалогеналканов
5. Ацилирование ароматических углеводородов:
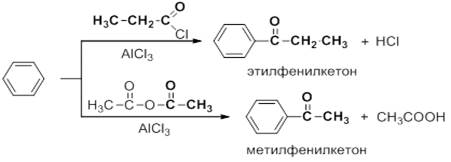
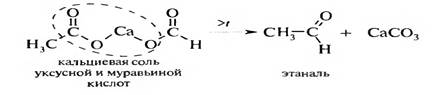
8.Пиролиз солей двухваапентных металлов и карбоновых кислот, образуются оксосоединения и карбонат металла. Из смешанной соли муравьиной и другой карбоновой кислоты при термическом разложении (пиролизе) получают альдегиды, а в остальных случаях образуются кетоны:
Физические свойства
Первый представитель - формальдегид – газ с острым раздражающим запахом. Насыщенные альдегиды и кетоны являются бесцветными жидкостями со своеобразным запахом. Высшие альдегиды имеют цветочный запах. Температуры кипения ниже, чем у соответствующих алканолов, т.к. не способны образовывать водородные связи. Низшие альдегиды и кетоны смешиваются в воде во всех отношениях, высшие в воде не растворимы.
Химические свойства альдегидов и кетонов
В молекуле оксосоединений имеется двойная связь, следовательно присущи реакции присоединения. Но двойная связь в карбонильной группе сильно поляризована и переходит в простую связь при действии полярных агентов. Полярная свзь C=O атакуется нуклеофилами, характерны реакции нуклеофильного присоединения.
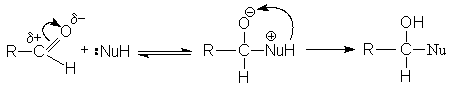
Во-вторых, электроноакцепторный характер карбонильной группы за счет –I и –M–эффектов обусловливает кислотность водородных атомов при соседних с ней углеродных атомов. Подвижность атомов водорода при a –углеродном атоме позволяет проводить a –галогенирования и конденсации.
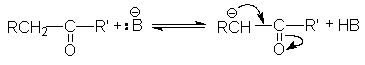
В-третьих, промежуточная степень окисления карбонильных групп (+1 в альдегидах и +2 в кетонах) обусловливает их способность к реакциям окисления и восстановления.
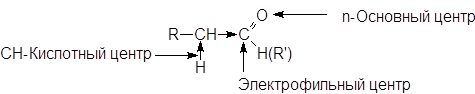
 2020-07-12
2020-07-12 145
145








