Многоклеточные организмы, состоящие из огромного числа различных типов тканей и органов, нуждаются в регуляции взаимодействия между ними для нормального функционирования в нестационарных условиях. В основе этой регуляции всегда лежат молекулярные механизмы. Превращения субстратов регулируются ферментами как за счет концентрационных факторов по закону действующих масс, так и с участием регуляторных ферментов, изменяющих каталитическую активность под действием эффекторов (ингибиторов или активаторов), а это уже регуляция по принципу обратной связи. Однако только такими простыми взаимосвязями нельзя обеспечить даже простое существование сформировавшегося многоклеточного организма в постоянно изменяющихся условиях и уж тем более его развитие с дифференциацией эмбриональных клеток в различные органы и ткани.
Более сложная регуляция, которая также основана на обратной связи, осуществляется нервной системой с участием специальных веществ, поскольку иннервация каждой отдельной клетки организма несколькими типами нервных окончаний просто невозможна. В общем случае эти регуляторные молекулы по их функциям можно классифицировать на три группы:
- гормоны;
- факторы роста и цитокины;
- нейромедиаторы.
Более всего известны классические регуляторные молекулы – гормоны. Многие из них содержатся в организме в сравнительно больших количествах, и поэтому они были выделены и стали известны уже давно. У животных гормоны образуются в специальных клетках, собранных в железы внутренней секреции (эндокринные железы), которые выделяют их прямо в кровь (у насекомых в гемолимфу). Этим железы внутренней секреции отличаются от других железистых органов, выделяющих свои секреты в протоки, которые так или иначе связаны с внешней средой (поджелудочная железа имеет экзокринную и эндокринную функцию). Разносимые кровью по всему организму гормоны находят свои клетки мишени на значительном удалении от секретирующей их железы.
Факторы роста – это регуляторные молекулы (у животных белковой природы). Они отличаются от гормонов тем, что их выделяют не специализированные клетки желез, а клетки тканей или отдельные самостоятельные клетки (тромбоциты, лейкоциты). Большинство факторов роста паракринны, то есть они предназначены для передачи сигнала на коротком расстоянии в пределах одного органа, но есть и аутокринные факторы роста, которые стимулируют сами выделяющие их клетки. В рамках такой классификации к факторам роста следует, очевидно, относить и фитогормоны, то есть вещества, управляющие ростом и дифференциацией клеток растений. В качестве примера таких регуляторных молекул у теплокровных можно назвать фактор роста из тромбоцитов, который выделяется и из многих других клеток, эпидермальный фактор роста, колонийстимулирующие факторы роста (стимулируют рост колоний некоторых лейкоцитов, поэтому их называют также интерлейкинами). Термин «цитокины» относится к факторам роста, участвующим в иммунных ответах.
Регуляция высвобождения факторов роста протекает по разным механизмам. Они участвуют в процессе развития, репарации поврежденных клеток, в их дифференциации, но точные данные обо всех взаимодействиях на этом уровне пока не получены.
Нейромедиаторы участвуют в работе клеток нервной ткани – нейронов, они передают сигнал от нервного окончания на конце отходящего от нейрона отростка (аксона) на иннервируемую клетку.
Регуляторная система организма находится под иерархическим контролем, где основная роль принадлежит нервной системе, которая таким образом через нервные окончания (с участием нейромедиаторов) и поступающие в жидкие среды организма (по лат. humor – жидкость) гормоны управляет всеми функциями организма (отсюда термин «нейрогуморальная регуляция»).
Рецепторные клетки кожи, слизистых оболочек, органов чувств, хеморецепторы внутри организма постоянно сообщают в центральную нервную систему об изменениях в окружающей среде, в составе крови, в работе органов. ЦНС анализирует поступающую информацию обычно на бессознательном уровне и выдает адекватные команды через нейроны или с помощью регуляторных молекул. В начале гормональной регуляции лежит специализированный отдел головного мозга, называемый гипоталамусом. Это одна из первичных и наиболее жизненно важных частей мозга. Гипоталамус (подбугорье) с помощью регуляторных молекул, называемых либеринами или рилизинг-факторами, по принципу обратной связи управляет работой гипофиза – дирижера работы всей эндокринной системы организма. Гипофиз человека весит 0,5–0,6 г. Он связан с гипоталамусом короткой ножкой и состоит из трех гистологически различных частей – передней доли, промежуточной и задней доли. Передняя доля состоит из железистых клеток, работой которых управляют либерины, поступающие по кратчайшему пути из гипоталамуса по кровеносным сосудам в ножке. Задняя доля гипофиза состоит из нервных клеток, гормоны гипоталамуса поступают сюда по отросткам нейронов – аксонам.
Гормоны передней доли гипофиза, стимулирующие работу желез внутренней секреции, называются тропинами или тропными гормонами. Принцип обратной связи состоит в том, что выделяемые железами внутренней секреции гормоны тормозят выделение как либеринов, так и тропинов. Правда, здесь нет такой четкой иерархии и не все железы внутренней секреции находятся под контролем гипоталамуса с участием либеринов. Так, например, активность задней доли гипофиза, секретирующей окситоцин и вазопрессин, регулируется по другим механизмам, а передняя доля гипофиза секретирует самостоятельный гормон – соматотропин (его секреция тормозится соматостатином – гормоном из гипоталамуса). В поджелудочной железе секреция инсулина (b-клетки) и глюкагона (a-клетки) напрямую зависит от уровня сахара в крови, но это не значит, что в регуляции уровня глюкозы в крови не участвует ЦНС. Кроме инсулина и глюкагона образование и расходование глюкозы контролируют некоторые другие гормоны. Под прямым контролем со стороны ЦНС находятся клетки мозгового вещества надпочечников, содержащие везикулы (пузырьки) с адреналином и норадреналином (около 20%) и АТФ (около 4%). По команде, поступающей из ЦНС, в течение нескольких секунд происходит выброс адреналина в результате экзоцитоза и его концентрация в крови возрастает на три порядка (от 10–10 до 10–7 моль/л). Обычная концентрация гормонов в крови составляет от 10–12 до 10–9 моль/л.
В качестве примера классической регуляции по схеме
Гипоталамус ® Гипофиз ® Железа внутренней секреции
можно привести цепочку
Тиролиберин ® Тиреотропин ® Тироксин.
Тиролиберин представляет собой трипептид – пироглутамил–гистидинил–пролинамид:
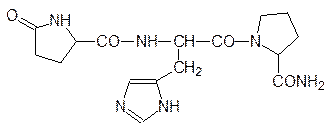
Гормональная активность этого вещества поразительна. Его концентрация в гипоталамусе очень мала: для установления его строения из 4 т гипоталамуса животных был выделен всего лишь 1 мг этого вещества. При введении его в организм в микрограммовых дозах секреция тиротропина, который представляет собой гликопротеин с молекулярной массой около 28 кДа, возрастает уже через несколько минут. Метилирование тиролиберина в положение 1 имидазольного кольца или замена амидной группы в пролиновом фрагменте на карбоксильную снижает активность тиролиберина в несколько тысяч раз, а метилирование имидазольного кольца в положение 3 повышает активность. Интересно, что этот необычный трипептид сравнительно устойчив к действию протеаз пищеварительной системы, поскольку он сохраняет активность и при приеме через рот.
В ответ на секрецию тиротропина гипофизом щитовидная железа выделяет в кровь тироксин и трииодтиронин, образующиеся из тирозиновых фрагментов в специально предназначенной для этого белковой молекуле:

По химической природе гормоны, продуцируемые железами внутренней секреции, относятся к трем типам соединений. Они могут быть пептидами, производными тирозина или стероидами. Растворимые в воде пептиды и гормоны на основе тирозина не проходят через клеточные мембраны. Их действие опосредовано рецепторными белками на внешней стороне клеток. Они, как в случае инсулина, могут работать в комплексе с транспортными белками или же действовать через специальные внутриклеточные белки (G-белки) на фермент, синтезирующий внутриклеточный регулятор (его называют мессенджером). Гормоном, действующим через G-белки, является, например, адреналин. Связываясь с адренорецептором, он запускает механизм образования активного комплекса из ГТФ и G‑белка, и уже этот комплекс включает работу аденилатциклазы, катализирующей образование цАМФ (это и есть мессенджер) из АТФ. Действие активированного G‑белка ограничено по времени, так как он обладает гидролазной активностью. Вследствие этого связанный с G-белком ГТФ разлагается на ГДФ и фосфат, а комплекс G-белка с ГДФ неактивен.
В отличие от пептидов и производных тирозина стероиды достаточно легко проходят через клеточные мембраны. Их рецепторы представлены растворенными в цитоплазме белками, которые связаны с белками теплового шока (Hsp). Обычно белки Hsp управляют организацией пространственной структуры синтезируемого на рибосоме белка (за это их называют также шаперонами, от франц. сhaperonne – сопровождающий). Гормон, проникший через мембрану в клетку, связывается с рецепторным белком, который вместе с белком теплового шока или уже без него проникает в ядро и связывается с соответствующим участком ДНК, активируя его. Однако для активации ДНК обязательно надо, чтобы белок теплового шока отошел от комплекса рецептора и гормона. Активация ДНК включает транскрипцию с образованием мРНК, мРНК выходит из ядра и поступает в рибосомы, где начинается синтез белка (трансляция), образование которого и должен был запустить гормон.
Из этого следует, что действие растворимых в воде гормонов проявляется в очень короткие сроки (до нескольких секунд, как у адреналина), тогда как стероидные гормоны проявляют свое действие через достаточно медленно текущие процессы. Нерастворимые в воде гормоны чаще всего регулируют синтез белков (ферментов, транспортных белков, структурных белков), поэтому их эффект может проявиться и через несколько дней.
Из пептидных гормонов хорошо изучены вазопрессин, окситоцин, соматотропин, ангиотензин, но более других, конечно, инсулин.
Недостаток инсулина или ослабленная реакция на инсулин со стороны клеток являются причиной сахарного диабета (в США каждый двадцатый имеет нарушения в обмене глюкозы; диабет является третьей по частоте причиной смерти после сердечно-сосудистых заболеваний и рака). При диабете происходит серьезное отклонение от нормы составляющих мочи и крови. Для усиления транспорта глюкозы в клетки у организма остается одна единственная возможность – повышение ее концентрации в крови, но почки не рассчитаны природой на этот вариант, и «лишняя» глюкоза попадает в мочу. Кроме повышенной концентрации глюкозы (в сутки с мочой может уходить до 100 г глюкозы), в моче диабетиков повышена концентрация так называемых кетоновых тел (ацетоацетата, ацетона и b‑гидроксибутирата), мочевины, ионов аммония (это все побочные продукты образования глюкозы из аминокислот), натрия (рН мочи у диабетиков понижен). Выделяющийся с выдыхаемым воздухом ацетон имеет характерный органический запах похожий на запах перегара. Диабетики пьют много воды, поскольку для выведения всего набора необычных отходов их жизнедеятельности ее расход увеличивается.
Антагонистом инсулина является глюкагон – полипептидный гормон, секретируемый поджелудочной железой, но клетками α-типа. Его эффект аналогичен действию адреналина, однако в отличие от него глюкагон не влияет на частоту сердечных сокращений и на давление крови.
Выделяемый передней долей гипофиза гормон соматотропин – белок с молекулярной массой около 21 кДа – регулирует вес и рост тела. Кроме того, соматотропин сложным образом регулирует секрецию инсулина и глюкагона, поэтому его используют для лечения некоторых форм сахарного диабета. Недостаток соматотропина приводит к остановке роста тела (лилипуты), а избыток – к гигантизму. Если усиленное выделение соматотропина происходит во взрослом возрасте – то это вызывает акромегалию, слоновую болезнь.
Вазопрессин повышает кровяное давление, его недостаток вызывает так называемый «несахарный диабет», это нонапептид формулы
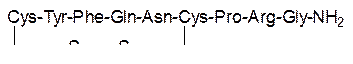
или
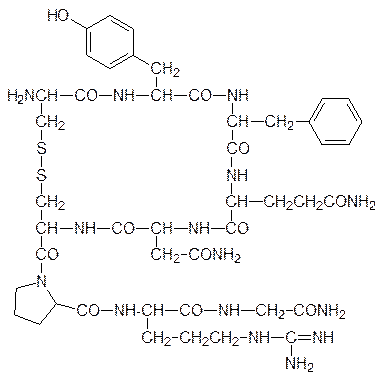
Вазопрессин регулирует работу почек, он управляет обратным всасыванием воды в почках (вместе с необходимыми организму веществами). При недостатке этого гормона почки выделяют до 10 л в день сильно разбавленной мочи.
Окситоцин вызывает сокращение гладкой мускулатуры, и его применяют для стимуляции родов, по строению он похож на вазопрессин:

или
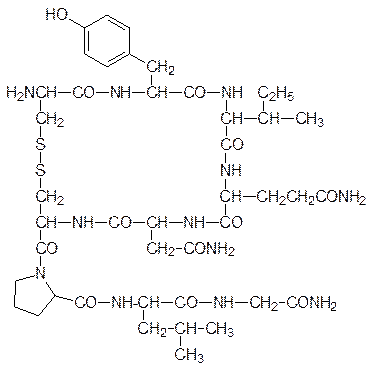
Тонус кровеносных сосудов регулируется ангиотензином. Этот гормон также участвует в регуляции работы почек. Аминокислотная последовательность неактивного ангиотензина I и активного ангиотензина II входит в состав белка ангиотензиногена (см. стр. 200). При повышенном давлении (гипертонии) можно получить терапевтический эффект путем снижением уровня активности этого гормона. Во всех клетках содержатся гидролазы, расщепляющие его, но их активация с целью снижения уровня ангиотензина II проблематична. В лекарственных целях блокируют превращение ангиотензина I в ангиотензин II. Для этого используют ингибирующие фермент соединения, похожие по строению на пептиды (пептидомиметики), первым соединением этой группы стал каптоприл – ацилированный меркаптоизомасляной кислотой пролин:
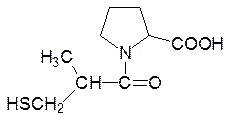
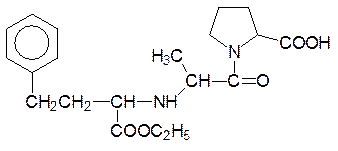
Вторая формула представляет одно из современных лекарстенных средств, блокирующих ангиотензинконвертирующий фермент – эналаприл (энап).
Ангиотензин II действует также на надпочечники, стимулируя выделение альдостерона, что приводит к задержке в организме ионов натрия.
Гипоталамус с участием кортиколиберина через адренокортикотропный гормон гипофиза (АКТГ, пептид из 39 аминокислот, период его полупревращения в организме составляет около 10 минут) регулирует работу внешнего (коркового) слоя клеток еще одной важной парной железы – надпочечников. Клетки внутренней (мозговой) части надпочечников секретируют адреналин, а клетки внешнего (коркового) слоя секретируют гормоны стероидной природы, которые участвуют в регуляции углеводного обмена и водно-солевого баланса – глюкокортикоиды и минералокортикоиды:


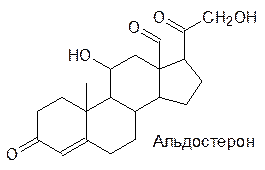
Здесь приведены три типичных представителя кортикостероидов, всего их известно около 30. Все эти гормоны обладают как глюкокортикоидной, так и минералокортикоидной активностью, но у кортизола более выражена глюкокортикоидная активность, у альдостерона – минералокортикоидная, а кортикостерон в равной мере обладает обеими видами активности. Кортизол стимулирует образование глюкозы из аминокислот (глюконеогенез) и обладает противовоспалительной и противоаллергической активностью. Избыток кортизола в организме приводит к потере мышечной массы, быстрой утомляемости; при общей худобе лицо у человека становится пухлым, круглым (болезнь Кушинга). Минералокортикоиды вызывают задержку ионов натрия в организме и потерю ионов калия с мочой. Недостаточная секреция гормонов коры надпочечников приводит к аддисоновой болезни, характеризующейся слабостью, подверженностью к стрессам и к инфекциям, кожа приобретает характерный смуглый оттенок (бронзовая болезнь).
Лекарственное применение самих кортикостероидов осложнено нарушением гормонального баланса организма из-за реализации принципа обратной связи (их длительное введение в виде лекарства может привести к атрофии надпочечников). Сейчас в основном стараются использовать эти соединения в виде средств местного действия и для этого уменьшают их растворимость и сродство к транспортным белкам введением атомов фтора и гидрофобизацией:

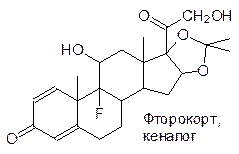
Еще одна группа стероидных гормонов представлена мужскими (андрогены) и женскими (эстрогены и гестагены) половыми гормонами:

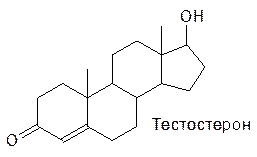

Кора надпочечников, семенники и яичники имеют общее эмбриональное происхождение, поэтому в разных количествах мужские и женские половые гормоны выделяются всеми этими типами тканей, то есть их действие зависит от соотношения между ними.
Уровень половых гормонов также контролируется гипоталамусом и гипофизом через лютеинизирующий гормон (в женском организме) и гонадотропины.
Половые гормоны определяют внешние половые признаки – мужские или, соответственно, женские. Они регулируют процессы роста, поддерживают функционирование репродуктивной системы. Андрогены стимулируют рост скелетных мышц, и поэтому их часто называют анаболическими гормонами. Эти свойства привлекают внимание фармакологов, поскольку разделение анаболической и андрогенной активности перспективно не только с целью получения анаболических допингов для спортсменов, но и с фармакологической точки зрения для лечения некоторых видов мышечных слабостей (астенические синдромы).
Эффективным анаболиком оказался, например, 19-нортестостерон, который в виде его эфира с фенилпропионовой кислотой используется на практике под названием феноболин (использование его спортсменами запрещено):
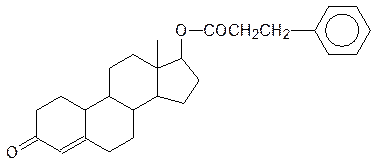
Эффективный стероидный анаболик 20-гидроксиэкдизон содержится в некоторых растениях (левзея сафлоровидная):
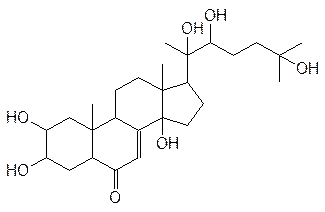
Тестостерон и, особенно, метилтестостерон задерживают развитие рака молочных желез, но побочный андрогенный эффект этих гормонов не позволяет использовать их для лечения этого заболевания.
Точно также женский половой гормон эстрадиол был бы неплохим средством для лечения атеросклероза, но связанное с ним появление женских вторичных половых признаков исключает возможность применения его для этих целей. Тем не менее, женские половые гормоны используются в медицинской практике для восполнения их недостатка после удаления яичников или в менопаузе. Однако наиболее широкое применение нашли они в качестве пероральных противозачаточных средств (контрацептивов). В этом случае экзогенные гормоны не вызывают интенсивной перестройки гормональной системы или атрофии генерирующих их тканей (как это было отмечено в случае кортикостероидов), так как периодические колебания их концентрации в крови характерны для женского организма. Наиболее эффективны сочетания эстрогенов и гестагенов (гормонов желтого тела); в поиске оптимальных структур аналогов и их дозировки были приложены колоссальные усилия. В качестве эстрогена в составе этих средств чаще всего используется этинилэстрадиол, а в качестве гестагена – прегнин:
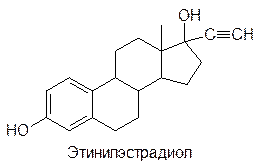
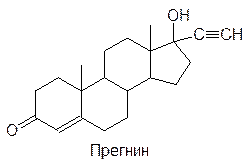
Принцип действия этих противозачаточных средств основан на создании гормональной среды, характерной для состояния беременности, когда овуляция прекращается. Гормональные противозачаточные средства принимаются при врачебном контроле, а современные препараты вообще состоят из двух или трех различных таблеток – эстрогена, гестагена и, желательно, гормонов гипофиза и гипоталамуса. Причем их дозы подбираются наблюдающим врачом с учетом гормонального статуса принимающей их женщины.
В общем случае надо понимать, что нормальный предусмотренный природой жизненный цикл женского организма представляет собой чередование периода беременности и кормления ребенка грудью без «простоев». Иначе говоря, как раз менструация – это ненормальность (недаром она так болезненна). Регулирующий лактацию и, как это всегда бывает у гормонов, многие другие функции, включая проявление материнского инстинкта, гипофизарный гормон белоковой природы пролактин в период беременности и активного кормления грудью (его концентрация при этом возрастает от 5–10 до 200 нг/мл) препятствует овуляции. Именно поэтому раньше длительное, до двух–трех лет, кормление ребенка грудью было лучшим естественным противозачаточным средством. Однако применение пролактина в качестве лекарственного средства вряд ли возможно из-за проблем, связанных с необходимостью равномерного введения высокомолекулярного белка (23–24 кДа) и с активизацией им процесса лактации.
Гормоны регулируют также рост и развитие насекомых. Лучше всего у этих представителей животного мира изучены гормоны линьки. Рост насекомого с его жестким экзоскелетом (кутикулой) возможен только после освобождения от ставшей тесной старой кутикулы с формированием новой, более просторной. Сам процесс линьки запускается гормоном стероидной природы – экдизоном:
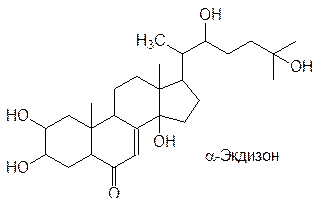
Высшие насекомые, проходящие несколько фаз развития (яйцо, личинка, куколка, имаго), претерпевают так называемый метаморфоз – переход из одной фазы развития в другую. А это уже регулируется ювенильными гормонами: при их присутствии в гемолимфе личинки ее линька не сопровождается метаморфозом. Ниже приведена структура одного из ювенильных гормонов ЮГ-III:
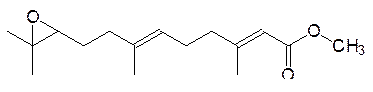
Ювенильные гормоны выделяются специальной железой, которая после прохождения личинкой нескольких линек атрофируется, и тогда в следующей линьке личинка претерпевает метаморфоз. Атрофия клеток железы может быть ускорена веществами, легко образующими реакционноспособные эпоксиды. В этом случае число линек сокращается и личинки превращаются в карликовые формы имаго. Такой эффект проявляют, например, прекоцены (от лат. рrecoce – преждевременно), содержащиеся в некоторых растениях. Показано, что ферментные системы насекомых окисляют их с образованием эпоксидов, например:

которые, очевидно, и вызывают преждевременную деградацию клеток железы, генерирующей ювенильные гормоны.
Образование ювенильных гормонов блокируется, например, лактоном фтормевалоновой кислоты (их биоситез, как и других изопреноидов, идет через мевалоновую кислоту, см. стр. 191):
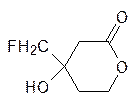
Агонистами ювенильных гормонов (их называют ювеноидами) являются очень многие вещества, например метопрен:
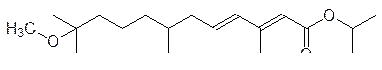
При действии фтормевалоната личинка, как и при действии прекоценов, преждевременно претерпевает метаморфоз и превращается в неполноценную карликовую форму взрослого насекомого, которое не может дать потомства, а действие метопрена приводит к тому, что личинка не превращается в имаго и также не может дать потомства. С точки зрения производителя сельскохозяйственной продукции преждевременный метаморфоз активно питающейся личинки, конечно, предпочтительнее, но фтормевалонат малоактивен, а получить антагонист ювенильных гормонов так и не удалось.
Особого разговора заслуживают фитогормоны – вещества, регулирующие рост и развитие растений, однако в приведенной в начале раздела классификации веществ, участвующих в гуморальной регуляции, растительные гормоны скорее всего надо относить к факторам роста, поскольку их образование идет не в специализированных клетках (клетках желез), а в клетках меристемы (это растительный аналог эмбриональной ткани), в клетках корней, листьев, то есть в обычных тканях растений. Более всего известны стимулирующие рост и клеточное деление ауксины, цитокинины и гиббереллины:

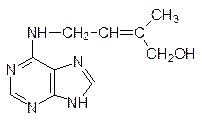
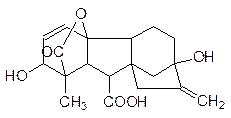
К фитогормонам, регулирующих состояние покоя, относятся этилен и абсцизовая кислота:

В регуляции роста и развития растений очень важную роль играет сочетание различных концентраций гормонов и их взаимное влияние. Так, например, повышенная концентрация стимулятора роста ауксина (индолилуксусная кислота) приводит к образованию ингибитора роста этилена.
Образующийся в меристемной ткани ауксин стимулирует рост корневой системы, а цитокинин (производное аденина), образующийся в корнях, стимулирует клеточное деление. Разные концентрации двух этих гормонов роста – ауксина и цитокинина – определяют рост и дифференциацию клеток меристемной ткани.
 2020-10-10
2020-10-10 148
148








