Масс-спектрометрия - это метод измерения отношения массы заряженных частиц к их заряду (m/z).
Для проведения масс-спектрометрического анализа образец переводят в ионизированную форму. После этого тем или иным способом производится разделение ионов по отношению их массы к зарядам и регистрация этих ионов, которые могут быть как положительными, так и отрицательными.
Масс-спектрометрический анализ дает важную информацию для определения молекулярной массы, молекулярной формулы или элементного состава и структуры молекул.
Масс-спектрометрию используют для определения относительной молекулярной массы Мг соединения, которую выражают в атомных единицах массы (а.е.м.) или дальтонах, Да, (1 Да = 1 а.е.м.=1,660541-10-27 кг, что равно 1/12 массы изотопа углерода с массовым числом 12). Масса основного изотопа углерода 12С выражается целым числом и равна 12,000000 Да. Массы всех изотопов любых других элементов будут выражаться нецелыми числами.
В масс-спектре пики или линии с определенным отношением m/z, соответствуют молекулярным фрагментам и также обозначаются целым числом, полученным при округлении точного значения m/z.
В масс-спектрометрии существует три различных понятия массы. Средняя молекулярная масса вычисляется на основании элементного состава и средних атомных масс. Средняя молекулярная масса важна при изучении больших молекул. Номинальная молекулярная масса вычисляется с учетом элементного состава и номинальных атомных масс наиболее распространенных в природе изотопов. Точная молекулярная масса вычисляется из значений точных масс наиболее распространенных изотопов.
С помощью масс-спектрометрии возможны: анализ органических соединений, неорганический анализ, исследования по выяснению механизмов реакций в органической химии и анализ поверхности.
С помощью масс-спектрометрии как аналитического метода решают громадное число качественных и количественных задач. Качественные исследования заключаются в определении структуры неизвестного соединения, в частности, природных веществ, метаболитов лекарственных препаратов и других ксенобиотиков, синтетических соединений. Для количественного анализа масс-спектрометрию используют при разработке арбитражных методов и методов сравнения. Масс-спектрометрия сегодня развивается очень быстро, охватывая все более широкие области применения. Объединение масс-спектрометрии с хроматографией значительно увеличило возможности метода и расширило круг изучаемых объектов.
5.12. Электрогравиметрия
В электрогравиметрическом анализе определяемое вещество количественно выделяют из раствора электролизом и по массе выделившегося металла или его оксида на электроде рассчитывают содержание определяемого элемента в пробе.
Электролизом называют химическое разложение вещества под действием электрического тока. На катоде происходит восстановление:
Cu2+ + 2e → Cu0
а на аноде – окисление:
2Cl- - 2e → Cl2 (г) и 2OH- - 2e → 1\2O2 + H2O
Под действием приложенного напряжения заряженные частицы (ионы) перемещаются к электродам. Однако их разряд, т. е. электролиз, начинается при достижении определенной величины напряжения, называемой напряжением разложения
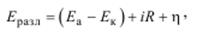 (5.2)
(5.2)
где Eа, Eк – ЭДС гальванического элемента;
iR – омическое падение напряжения;
η – перенапряжение анода и катода при выделении продуктов электролиза.
Схема установки для проведения электролиза приведена на рис. 5.14.
Электролиз чаще всего проводят при постоянном токе. Для получения постоянного тока обычно используют выпрямитель переменного тока или батарею аккумуляторов 1. Скользящий контакт 2 позволяет регулировать подаваемое напряжение, которое измеряют вольтметром V. Сила тока контролируется амперметром А. При выделении металлов катод 5 обычно используют в виде платиновой сетки, анод 4 – в виде платиновой спирали или пластинки. При выделении оксидов знаки электродов меняются: платиновая сетка становится анодом, а спираль – катодом. Раствор перемешивается механической или магнитной мешалкой 3.
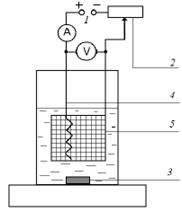
Рис. 5.14. Схема установки для проведения электролиза: 1 – источник постоянного тока; 2 – переменное сопротивление (реостат); 3 – магнитная мешалка;
4 – анод; 5 – катод
В электрогравиметрических методах анализа кроме потенциала, силы тока важно контролировать ряд экспериментальных условий.
5.13. Кулонометрия
В кулонометрических методах определяют количество электричества, которое расходуется в ходе электрохимической реакции. Различают прямую кулонометрию и кулонометрическое титрование.
В методах прямой кулонометрии анализируемое вещество непосредственно подвергается электрохимическому превращению в кулонометрической ячейке (процесс проводят при постоянном контролируемом потенциале) (Рис. 5.15.).

Рис. 5.15. Схема установки для прямой кулономeтрии при постоянном E:
1 - электролизер; 2 - источник постоянного токa с регулируемым напряжением: 3 - прибор для определения количества злектричества: 4 - рабочий электрод; 5 - вспомогательный электрод; 6 - электрод сравнения, относительно которого контролируют потенциал рабочего электрода: 7 - устройство, измеряющее разность потенциалов.
В методе кулонометрического титрования определяемое вещество реагирует с титрантом, который производится в кулонометрической ячейке посредством электролиза специально подобранного раствора.
Кулонометрическое титрование проводят при постоянном токе.
Кулонометрические методы основаны на законах Фарадея. Необходимым условием количественного определения является 100%-й выход по току. Выход по току определяется отношением количества вещества, выделившегося в процессе электролиза, к теоретическому количеству, вычисленному на основании закона Фарадея. Не 100%-й выход по току может быть обусловлен затратами тока на побочные процессы:
1) разложение воды на водород и кислород;
2) восстановление или окисление примесей, например, растворенного в воде кислорода;
3) реакция с участием продуктов электролиза;
4) реакция с участием материала электрода (окисление ртути и др).
При проведении кулонометрических определений нужно предусмотреть все условия, обеспечивающие 100%-й выход по току, контроль рН, выбор электродов, разделение катодного и анодного пространства.
5.14. Кондуктометрия
Кондуктометрический метод анализа основан на измерении удельной электропроводности анализируемого раствора.
Электропроводностью называют величину, обратную электрическому сопротивлению R. Единицей измерения электропроводности является сименс (См) или Ом-1. Растворы электролитов, являясь проводниками II рода, подчиняются закону Ома. По аналогии с сопротивлением проводников I рода сопротивление раствора прямо пропорционально расстоянию между электродами d и обратно пропорционально площади их поверхности A:
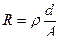 (5.3)
(5.3)
где р - удельное сопротивление, Ом · см.
При d =1 см и А =1 см 2имеем R = р, следовательно, удельное сопротивление равно сопротивлению 1 см3 раствора.
Величину, обратную удельному сопротивлению, называют удельной электропроводностью:
æ = 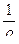 (5.4)
(5.4)
Удельная электропроводность (См ∙ см-1) численно равна току (А), проходящему через слой раствора с поперечным сечением, равным единице, под действием градиента потенциала 1 В на единицу длины.
Электропроводность разбавленных растворов электролитов зависит от числа ионов в растворе (т. е. от концентрации), числа элементарных зарядов, переносимых каждым ионом (т. е. от заряда иона), и от скорости движения одинаково заряженных ионов к катоду или аноду под действием электрического поля (Рис. 5.16.). С учетом всех этих факторов электропроводящие свойства ионов характеризуют эквивалентной ионной электропроводностью (подвижностью).
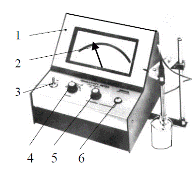
Рис. 5.16. Кондуктометр ОК 102/1: 1 – корпус прибора; 2 – измерительная
шкала; 3 – тумблер «Сеть»; 4 - переключатель пределов измерения «Range»; 5 – ручка калибровки потенциометра «Calibration»; 6 – кнопка калибровки «Calibration».
Различают прямую и косвенную кондуктометрию, или кондуктометр ическое титрование.
Прямая кондуктометрия мало применяется в аналитической химии. Причина этого в том, что электропроводность является величиной аддитивной и определяется присутствием всех ионов в растворе. Прямые кондуктометрические измерения используют для контроля качества воды, применяемой в химической лаборатории, и современные установки для перегонки или деминерализации воды снабжаются кондуктометрическими датчиками - кондуктометрами для измерения удельной электропроводности растворов. Детекторы по электропроводности применяются в ионной хроматографии.
К достоинствам метода кондуктометрического титрования относится возможность высокоточных измерений даже в очень разбавленных растворах.
Для кондуктометрического титрования пригодны кислотно-основные или осадительные реакции, сопровождающиеся заметным изменением электропроводности вследствие образования малодиссоциирующих или малорастворимых соединений.
5.15. Титриметрия
Титриметрический анализ (титрование) — метод количественного/массового анализа, который часто используется в аналитической химии, основанный на измерении объёма раствора реактива точно известной концентрации, расходуемого для реакции с определяемым веществом (Рис. 5.17.).

 2020-10-10
2020-10-10 252
252








