# Определение температуры кипения
Основные правила по технике безопасности для данной работы
Работу проводят в вытяжном шкафу, не следует наклоняться внутрь его, так как пары и мелкие частицы реактивов потоком воздуха уносятся вверх и могут попасть вам в лицо, дыхательные пути и глаза.
Нагревание легколетучих веществ проводят на водяной бане, не допуская контакта их паров с открытым пламенем, электропроводкой, электроприборами и другими возможными источниками возгорания.
Цель работы
Определить температуру кипения перегоняемой жидкости, сравнить со справочными данными, определить степень чистоты исследуемого вещества.
Основные теоретические положения
В результате нагревания жидкости и ее испарения устанавливается равновесие между жидкостью и паром, а следовательно, и определенное давление пара. Величина этого давления зависит от природы жидкости и ее температуры. С повышением температуры давление пара над жидкостью возрастает. Когда давление пара становится равным внешнему давлению, жидкость начинает кипеть. Как правило, при этих условиях температура жидкости больше не повышается. Температуру, при которой давление пара становится равным внешнему давлению, называют температурой кипения.
Температуру кипения можно определить в ходе простой перегонки этой жидкости. Перегонкой называют процесс, в ходе которого вещество нагревают в соответствующей аппаратуре до кипения и образовавшийся пар отводят и конденсируют.

Установка для простой перегонки жидкости.
| 1 - круглодонная колба | 4 – холодильник Либиха | 6 – приемник |
| 2 - насадка Вюрца 3- термометр | 5 - алонж | 7 – водяная баня |
В круглодонную колбу помещают 20 мл исследуемой жидкости, для равномерного кипения бросают «кипелки» (кусочки пористого материала размером со спичечную головку: кирпича, неглазурованного фарфора, пемзы) для предотвращения перегрева и связанных с ним задержки кипения. У поверхности этих материалов начинается образование пузырьков пара, и кипение будет происходить равномерно при соответствующей температуре. «Кипелки» можно использовать только один раз, если перегонка прерывается и содержимое колбы охлаждается поры «кипелок» заполняются жидкостью и они становятся неактивными, поэтому должны быть заменены новыми. Если в начале перегонки забыли бросить в колбу «кипелки», то ошибку можно исправить только после того, как жидкость охладится не менее чем на 10°С ниже температуры кипения перегоняемого вещества. При добавлении «кипелок» в горячую жидкость может произойти бурное вскипание, которое, как правило, сопровождается выбросом жидкости из колбы.
Собирают установку согласно рисунку, круглодонную колбу закрывают пробкой со вставленным в нее термометром, который размещают так, чтобы верхний край шарика ртути находился на 0,5 см ниже бокового отвода насадки Вюрца и полностью омывался парами. Включают водяное охлаждение холодильника и начинают нагревать содержимое колбы.
При этом следят за равномерностью кипения, за показаниями термометра и за поступлением отгона в приемник (в течение секунды в приемник должно поступить 1 – 2 капли дистиллята). После того, как установится постоянная температура кипения, записывают показания термометра. Указанная температура и будет температурой кипения перегоняемого вещества. Перегонку прекращают, когда остаток в колбе составит 3 – 4 мл.
| Название исследуемого вещества | Температура падения первой капли, 0С | Установившаяся, постоянная температура кипения, 0С | Температура кипения данного чистого вещества, 0С (справочные данные) |
Анализ результатов лабораторной работы
Сделайте вывод о влиянии примесей, имеющихся в исследуемой жидкости на её температуру кипения.
Контрольные вопросы
1. Какой процесс называют простой перегонкой?
2. Типы колб: какие используются в данной лабораторной работе?
3. Почему круглодонную колбу при перегонке при атмосферном давлении наполняют не более чем на 2/3 от её объема?
4. От чего зависит характер кипения жидкости? Что такое «кипелки» и для чего их используют?
# Определение температуры плавления
Основные правила по технике безопасности для данной работы
При работе со спиртовкой нужно помнить:
· зажигать её можно только спичкой, а не от другой спиртовки;
- диск должен плотно прилегать к горлышку и фитиль находиться в расправленном виде;
- нельзя переносить зажжённую спиртовку;
- тушить фитиль спиртовки только колпачком.
Цель работы
Определить температуру плавления исследуемого вещества и при сравнении её со справочными данными сделать вывод о степени чистоты изучаемого образца.
Основные теоретические положения
Температура плавления вещества - это температура, при которой вещество из твердого (кристаллического) состояния переходит в жидкое. Началом плавления считается момент размягчения вещества и образование первой капли, а концом - образование прозрачной жидкости.
Если вещество химически чистое, то его температура плавления колеблется в интервале 0,5-1,0°С. Четкая температура плавления вещества является признаком его чистоты, примеси обычно понижают эту температуру или увеличивают интервал, в котором плавится данное соединение.
Порядок выполнения работы
Температуру плавления органического кристаллического вещества определяют в стеклянном капилляре. Для этого вещество, тщательно измельченное в фарфоровой ступке, помещают в запаянный с одного конца стеклянный капилляр, диаметром 0,8 – 1 мм. Для того чтобы переместить вещество на дно капилляра и плотно его утрамбовать, капилляр с веществом бросают несколько раз запаянным концом вниз через стеклянную трубку длиной 40 - 50 см, поставленную вертикально на стол. Высота столбика вещества в капилляре, тщательно уплотненного должна быть 3 – 5 мм.
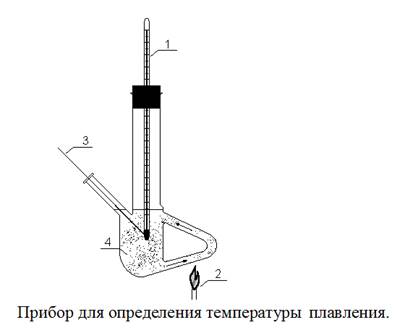
1- термометр,
2- спиртовка,
3- капилляр,
4- глицерин (дибутилфталат или силиконовое масло)
Капилляр с веществом помещают в боковой отвод прибора, так чтобы он касался шарика термометра.
Сначала нагревание ведут со скоростью 4 – 6 0С в минуту, а при температуре, близкой к температуре плавления (справочной) – со скоростью 1 – 2 0С в минуту.
Отмечают температуру, при которой появляется жидкая фаза (начало плавления) и температуру, при которой исчезают
последние кристаллы вещества (конец плавления). Результаты представляют в виде интервала, например 135 -135,5°C. Данные заносят в таблицу.
| Название исследуемого вещества | Температура начала плавления, 0С | Температура конца плавления, 0С | Температура плавления чистого вещества, 0С (справочные данные) |
Анализ результатов лабораторной работы
Сделайте вывод о степени чистоты исследуемого органического вещества.
Контрольные вопросы
1. Какие физические константы характерны для твердых органических веществ?
2. Что такое температура плавления?
3. В каком случае, температура плавления, полученная в результате эксперимента, может отличаться от справочных данных.
4. О чём можно судить по величине интервала: появление первой капли - образование прозрачной жидкости в капилляре.
5. Почему прибор для определения температуры плавления заполняют глицерином, а, например, не водой.
# Определение показателя преломления
Основные правила по технике безопасности для данной работы
Анализируемые вещества токсичны, поэтому определять их запах, нужно осторожно, не вдыхая полной грудью, не наклоняясь над сосудом, а направляя к себе пары или газ движением руки.
- Алканы С5 - С8 оказывают умеренное раздражающее действие на дыхательные пути, высшие члены ряда более опасны при воздействии на кожные покровы, чем при ингаляции паров;
- Ароматические углеводороды токсичны, при отравлении высокими концентрациями бензола слизистые оболочки становятся вишнево-красного цвета, лицо — бледно-розовое или землисто-синюшное; меньшие концентрации их приводят к возбуждению, напоминающему алкогольное опьянение, возможны галлюцинации, затем возникают сонливость, общая слабость, головокружение, головная боль, тошнота, рвота, диспепсические явления, метеоризм, может наступить потеря сознания.
Цель работы
Определить зависимость показателя преломления от температуры.
Основные теоретические положения
Показатель преломления широко используется для идентификации индивидуальных жидких веществ и проверки их чистоты (наличие примесей в исследуемой жидкости ведет к отклонению численного значения показателя преломления от справочных данных), а также для определения состава бинарных углеводородных смесей. Показатель преломления позволяет судить о групповом углеводородном составе нефти и нефтяных дистиллятов (он уменьшается в последовательности: ароматические углеводороды > нафтены > алканы), а в сочетании с плотностью и молекулярной массой – рассчитать стуктурно-групповой состав нефтяных фракций.
При переходе светового луча А (рис.3) из воздуха на поверхность какого либо тела он частично отражается – луч Б, а частично проходит внутрь тела – луч В; при этом он изменяет свое направление, т.е. преломляется.
Отношение синуса угла падения к синусу угла преломления называется показателем преломления
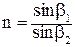
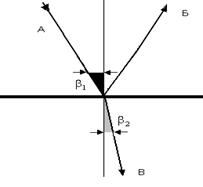
Рис.3. Переход светового луча из газа в жидкость
Экспериментальная часть работы
Работа на рефрактометре ИРФ-454 производится в следующем порядке: открывают верхнее полушарие измерительной головки и протирают ватой, смоченной спиртом, поверхности призм, дают спирту испариться. Затем на плоскость измерительной призмы наносят с помощью капельницы (не касаясь призмы) несколько капель изучаемого вещества. Осторожно закрывают верхнее полушарие измерительной головки. Осветительное зеркало устанавливают так, чтобы свет от источника освещения поступал к осветительной призме и равномерно освещал поле зрения, позволяя свету поступать в окошко, освещающее шкалу прибора. Глядя в зрительную трубу, фокусируют окуляр так, чтобы шкала прибора была отчетливо видна. Вращая маховичок I и наблюдая в окуляр зрительной трубы, находят границу раздела света и тени. Если она размыта и окрашена в желто – красный или сине – зеленый свет, надо при помощи маховичка I I добиться более четкого изображения этой границы.
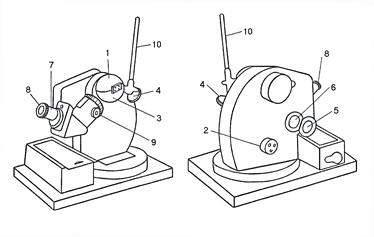
Рис.4. Рефрактометр типа ИРФ – 454.
| 1 – верхнее полушарие измерительной головки; |
| 2 – маховичок I; |
| 3 – нижнее полушарие измерительной головки; |
| 4 – зеркало для освещения призмы; |
| 5 – зеркало для освещения шкалы; |
| 6 – окошко, освещающее шкалу; |
| 7 – зрительная труба; |
| 8 – окуляр; |
| 9 – маховичок I I; |
| 10 – термометр. |
Границу раздела света и тени необходимо точно совместить с перекрестием сетки (рис.5) и снять отсчет по шкале показателей преломления. Показатель преломления измеряется с точностью до четвертого знака после запятой.
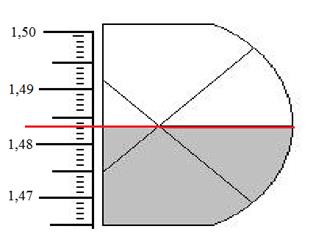
Рис.5. Значение показателя преломления на шкале.
Показатель преломления зависит от температуры (с повышением температуры показатель преломления понижается) и изменяется в зависимости от длины волны. Поэтому измерение показателя преломления проводят в монохроматическом свете при постоянной температуре и обозначают 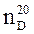 , (где 20 – температура в 0С, D – линии желтого натриевого пламени).
, (где 20 – температура в 0С, D – линии желтого натриевого пламени).
Зависимость показателя преломления от температуры выражается формулой
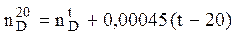
где
0,00045 – поправочный коэффициент (коэффициент α следует применять в пределах температуры от 15 до 35°С;
t – температура, при которой проводилось определение.
Полученные данные заносят в таблицу:
| Индивидуальное вещество | |
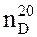
| |
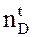
| |
| класс углеводородов |
Анализ результатов лабораторной работы
Сделайте вывод о:
- чистоте индивидуальных органических веществ;
- влиянии температуры на численное значение показателя преломления;
Контрольные вопросы
1. Влияние состава органических соединений на показатель преломления.
2. Влияние строения органических соединений на показатель преломления.
3. Что влияет на изменение численного значения показателя преломления данного углеводорода.
Тема «Способы разделения смеси органических соединений»
# Фракционная перегонка смеси
Цель работы
Определить соотношение компонентов в смеси и их химическую чистоту после разделения смеси.
Основные теоретические положения
Перегонка называется фракционной потому, что вся перегоняемая жидкость собирается в разные приемники отдельными порциями, которые называются фракциями. Первые фракции содержат преимущественно вещество с самой низкой температурой кипения, последние— с самой высокой.
При этом виде перегонки используется дефлегматор, в котором при неполном охлаждении пара кипящей жидкости происходит частичная конденсация пара более высоко кипящей жидкости, обогащенный высоко кипящим компонентом промежуточный дистиллят (флегма) возвращается в колбу, а пар обогащается более низкокипящим веществом. Фракционная перегонка позволяет эффективно разделять смеси веществ с небольшой разницей в температурах кипения (~10-20 °C).
Порядок выполнения работы
Для фракционной перегонки смеси 2-х жидкостей собирают прибор, изображенный на рисунке:
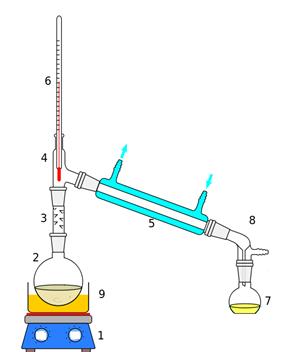
Прибор для фракционной перегонки жидкостей
| 1-плитка | 2- круглодонная колба | 3- дефлегматор. |
| 4 - насадка Вюрца | 5- холодильник Либиха | 6- термометр |
| 7- приемник. | 8- алонж | 9- нагревательная баня |
При выполнении данной работы студент получает 20мл бинарной смеси – «ацетон +толуол».
В круглодонную колбу помещают исследуемую жидкость, бросают “кипелки” и закрывают колбу дефлегматором со вставленным в него термометром. Включают водяное охлаждение и начинают нагревать содержимое колбы. Следят за равномерностью кипения, показаниями термометра и за поступлением отгона в приемник (в течение секунды в приемник должно поступать 1-2 капли дистиллята).
В ходе разгонки собирают 3 фракции:
1-я фракция с момента падения первой капли и до температуры кипения ацетона.
2-я фракция (промежуточная) собирается во время быстрого повышения температуры
3-я фракция – фракция кипения толуола.
После завершения перегонки определяют объем каждой фракции и определяют объемное соотношение компонентов в смеси.
Строят кривую разгонки в координатах: объем фракции - температура
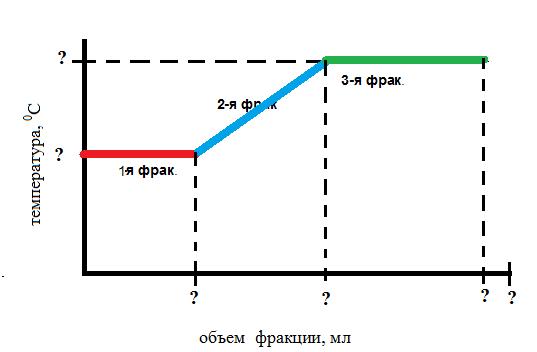
Кривая разгонки смеси ацетон/толуол
| № фракции |
вещество | содержание фракции |
t кип | ||
| название | объем, мл | % об. | экспериментальная | литературная | |
| 1. | ацетон | ||||
| 2. | промежуточная фракция | Х | Х | ||
| 3. | толуол | ||||
| 4. | остаток | Х | Х | ||
Анализ результатов лабораторной работы
Сделайте вывод о соотношении компонентов в смеси, о их химической чистоте после разделения смеси и о эффективности данного метода разделения смеси двух жидкостей..
Контрольные вопросы
- Почему нагрев первой фракции ведут на водяной бане, какие еще виды нагревательных бань Вы знаете, их назначение?
- О чём свидетельствуют не параллельные участки кривой разгонки для первой и третьей фракции, какими они должны быть в идеале.
# Экстракция
Цель работы
Определить соотношение компонентов в смеси и их химическую чистоту после разделения смеси.
Основные теоретические положения
Экстракция (от лат. extraho — извлекаю) — извлечения вещества, растворенного в одном растворителе, другим растворителем, который не смешивается с первым и лучше растворяет извлекаемое вещество.
При подборе растворителя для экстракции учитывают несколько факторов:
· растворитель не должен растворяться в воде;
· растворимость извлекаемого вещества в экстрагенте должна быть значительно выше, чем в исходном растворе;
· плотность извлекаемого вещества и экстрагента должна существенно отличаться;
· растворитель должен иметь невысокую температуру кипения;
· невысокая летучесть и низкая токсичность.
Порядок выполнения работы
Чаще всего экстрагирование проводят в делительной воронке, в которую наливают раствор, подлежащий экстракции, и экстрагирующую жидкость. При этом воронка должна быть заполнена не более чем на 2/3. Обычно объем экстрагирующей жидкости составляет от 1/5 до 1/3 объема экстрагируемого раствора. Верхний тубус делительной воронки закрывают пробкой и осторожно встряхивают воронку, придерживая пробку и кран руками.
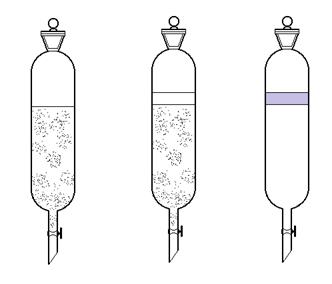
Экстракция жидкости в делительной воронке.
Затем необходимо ненадолго открыть кран для выравнивания избыточного давления, возникающего вследствие испарения органического растворителя (при этой операции воронка наклоняется так, чтобы кран был выше отверстия закрытого пробкой). По окончании взбалтывания делительную воронку укрепляют вертикально на штативе, подставив под кран воронки колбу. После полного расслаивания нижний (водный) слой сливают через кран, а верхний (органический) выливают в колбу через верхнее отверстие воронки. Экстракцию водного слоя проводят три раза, используя каждый раз новую порцию органического растворителя.
Полученные экстракты объединяют и сушат подходящим осушителем в течение 20-30 минут, затем, отделив от осушителя, проводят фракционную разгонку органического растворителя и экстрагируемого вещества
Анализ результатов лабораторной работы
Сделайте вывод о соотношении компонентов в смеси, о их химической чистоте после разделения смеси и о эффективности данного метода разделения смеси двух жидкостей.
Контрольные вопросы
- В чем сущность процессов экстракции в системе «жидкость – жидкость»?
- Какие компоненты учувствуют в процессе экстракции?
# Перекристаллизация
Цель работы
Очистить от примесей твердое органическое вещество, определить степень его чистоты после разделения смеси.
Основные теоретические положения
Кристаллизация является важным методом очистки твердых органических соединений. Вещество, которое нужно перекристаллизовать, растворяют при нагревании в подходящем растворителе. Решающее значение для успешного проведения кристаллизации имеет правильный выбор растворителя. Одно из основных требований к растворителю заключается в том, чтобы при нагревании он растворял кристаллизуемое вещество значительно лучше, чем на холоду. Растворитель не должен растворять примеси (тогда их можно будет отфильтровать).
Если растворитель – органическое соединение, то растворение ведут при кипячении в колбе с обратным холодильником.
Порядок выполнения работы
Основные этапы процесса перекристаллизации:
· Приготовление горячего раствора, насыщенного кристаллизуемым веществом
Взвешивают вещество, подлежащее перекристаллизации и помещают его в коническую колбу. Растворитель (дистиллированная вода нагретая до кипения) добавляют понемногу в колбу с взвешенным веществом. Растворитель следует брать в количестве, достаточном для полного растворения вещества при нагревании (нерастворимые примеси во внимание не принимаются),
·
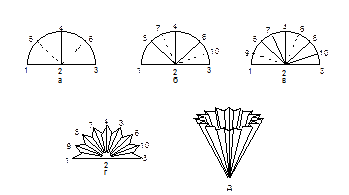 |
Отфильтровывание этого раствора от не растворивщихся примесей на складчатом фильтре.
При продолжающемся несильном кипении раствор фильтруют через складчатый фильтр(3), лежащий на химической воронке(2).
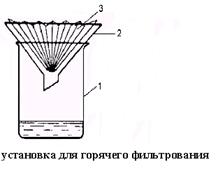
· Охлаждение фильтрата (в бане с ледяной водой).
Кристаллизацию проводят до прекращения увеличения количества кристаллов.
· Отфильтровывание выпавшего осадка на нутч – фильтре.
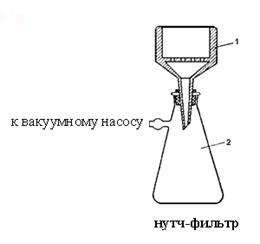 Кристаллы переносят на фильтр, помещенный на воронку Бюхнера (1), вставленную в коническую колбу Бунзена (2). Маточный раствор отсасывают с помощью вакуумного насоса.
Кристаллы переносят на фильтр, помещенный на воронку Бюхнера (1), вставленную в коническую колбу Бунзена (2). Маточный раствор отсасывают с помощью вакуумного насоса.
· Высушивание отфильтрованного осадка на воздухе
· Изучение формы кристаллов
Анализ результатов лабораторной работы
Сделайте вывод о химической чистоте перекисталлизованного вещества и о эффективности данного метода разделения смеси твердых веществ.
Контрольные вопросы
1. Какое количество растворителя необходимо добавить при приготовлении раствора перекристаллизуемого вещества.
2. Какие требования, предъявляют к растворителю для перекристаллизации.
3. Почему при горячем фильтровании используется складчатый фильтр.
4. Почему необходимо проводить горячее фильтрование при продолжающемся несильном кипении раствора через складчатый фильтр.
5. Какая операция предшествует фильтрованию на нутч-фильтре.
6. Как необходимо вести охлаждение фильтрата, чтобы получить крупные кристаллы перекристаллизованного вещества.
# Возгонка
Цель работы
Очистить от примесей твердое органическое вещество, определить степень его чистоты после разделения смеси.
Основные теоретические положения
Возгонка (сублимация) -это процесс, при котором твердое тело при помощи нагревания переводится в газообразное состояние, а потом при охлаждении обратно в твердое, минуя стадию жидкости.
Давление пара твердого вещества как и жидкости увеличивается с повышением температуры. Вещества, имеющие относительно высокое давление пара, при нагревании могут приобрести давление пара, равное атмосферному, при температуре ниже температуры плавления. Температура плавления при нагревании этих веществ не достигается, они непосредственно переходят в парообразное состояние, т.е. возгоняются. Температура, при которой давление пара над твердым веществом равно внешнему давлению, называется температурой возгонки.
Для очистки органических соединений возгонка удобна в том случае, когда возгоняется лишь основной продукт, а примеси не испаряются.
Даже однократная возгонка, как правило, приводит к получению вполне чистого продукта, но это весьма длительный процесс, поэтому его обычно используют для очистки небольших количеств веществ.
Порядок выполнения работы
Возгонка состоит из двух стадий:
· испарение твердого вещества,
· конденсация образовавшихся паров в твердое вещество.
Поскольку скорость испарения пропорциональна общей площади поверхности испарения, подвергаемое возгонке вещество необходимо как можно тоньше измельчать.
Не следует также допускать плавления вещества при возгонке:
· в этом случае испарение будет происходить уже из жидкой фазы, т.е. фактически вещество будет перегоняться с превращением конденсата непосредственно в твердое вещество,
· это ведет к падению скорости процесса вследствие резкого уменьшения поверхности вещества,
· при этом кристаллы растрескиваются, осколки их долетают до возгнанного вещества и загрязняют его.
Охлажденная поверхность должна находиться вблизи от пространства, в котором происходит возгонка - это увеличивает скорость возгонки.
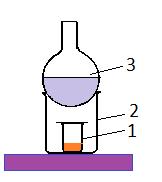
Установка для возгонки
1-кристаллическое вещество
2-стакан
3-круглодонная колба, заполненная холодной водой
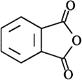
ФТАЛЕВЫЙ АНГИДРИД - бесцветные кристаллы, t пл 130,8°C (с возгонкой). Сырьё в производстве алкидных смол, пластификаторов (эфиров фталевой кислоты), красителей.
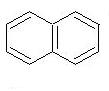 НАФТАЛИН- бесцветные кристаллы с характерным запахом; т. пл. 80,29 °С (с возгонкой), т. кип. 218oС.
НАФТАЛИН- бесцветные кристаллы с характерным запахом; т. пл. 80,29 °С (с возгонкой), т. кип. 218oС.
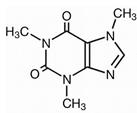
КОФЕИН- бесцветные горькие кристаллы, t пл. 238C, сублимируется при 178C
Кофеин содержится в растениях, таких как кофейное дерево, чай, мате, гуарана, кола, и некоторых других.
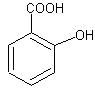
САЛИЦИЛОВАЯ КИСЛОТА - бесцветный кристаллический порошок слабогорького вкуса, t пл. - 159,5°С, е. В природе салициловая кислота встречается в свободном состоянии в листьях и цветах некоторых растений (ромашка, таволга)
Анализ результатов лабораторной работы
Сделайте вывод о химической чистоте органического вещества после возгонки и об эффективности данного метода разделения смеси твердых веществ.
Контрольные вопросы
1. Что называют возгонкой?
2. Что выражает понятие «температура возгонки»?
3. Почему возгонку следует проводить при температуре, лежащей несколько ниже температуры возгонки?
 2020-10-12
2020-10-12 593
593








