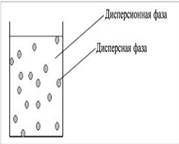
Дисперсные системы – это системы, в которых мелкие частицы вещества, или дисперсная фаза, распределены в однородной среде (жидкость, газ, кристалл), или дисперсионной фазе
Размер частиц дисперсной фазы характеризуется дисперсностью. В зависимости от неё дисперсные системы можно разделить на высокодисперсные, или собственно коллоидные, и низкодисперсные (грубодисперсные).
Размер частиц низкодисперсных систем составляет 10–3
мм. и больше. Размер частиц высокодисперсных систем лежит в интервале 10–6–10–4 мм (от 1 до 100 нм), что, как минимум, на порядок больше размера частиц в истинных растворах (10–7 мм).
Химия дисперсных систем изучает поведение вещества в сильно раздробленном, высокодисперсном состоянии, характеризующемся очень высоким отношением общей площади поверхности всех частиц к их общему объему или массе (степень дисперсности).
Важнейшая особенность дисперсного состояния вещества состоит в том, что энергия системы главным образом сосредоточена на поверхности раздела фаз. При диспергировании, или измельчении, вещества происходит значительное увеличение площади поверхности частиц (при постоянном суммарном их объеме).
Поэтому область химии дисперсных систем (и коллоидных растворов) считают химией поверхностных явлений.
Свойства вещества в раздробленном, или дисперсном, состоянии значительно отличаются от свойств того же вещества, находящегося в недисперсном состоянии, т.е. в виде куска твердого тела или некоторого объема жидкости. Классификация дисперсных систем
Таблица №3
| Дисперсная | Дисперсионная среда | Название системы | Примеры | ||||
| фаза | |||||||
| Газ | Газ | (Дисперсная Система не образуется) |
|
| |||
| - | |||||||
|
| |||||||
| Жидкость | Пена | Пена газированной воды, пузырьки газа в жидкости, мыльная пена | |||||
| Твердое тело | Твердая пена | Пенопласт, Микропористая резина, пемза, хлеб, сыр | |||||
| Жидкость | Газ | Аэрозоль |
| Туман, облака, струя из аэрозольного баллона | |||
|
| |||||||
| Жидкость | Эмульсия |
| Молоко, сливочное масло, майонез, крем, мазь | ||||
|
| |||||||
| Твердое тело | Твердая |
| Жемчуг, опал | ||||
| эмульсия |
| ||||||
| Твердое тело
| Газ | Аэрозоль, порошок | Пыль, дым, мука, цемент | ||||
| Жидкость | Суспензия, золь (коллоидный раствор) | Глина, паста, ил,жидкиесмазочные масла с добавкой графита или MoS | |||||
| Твердое тело | Твердый золь | Сплавы, цветные стекла, минералы | |||||
Конус Тиндаля тем ярче, чем выше концентрация и больше размер частиц. Интенсивность светорассеяния усиливается при коротковолновом излучении и при значительном отличии показателей преломления дисперсной и дисперсионной фаз. С уменьшением диаметра частиц максимум поглощения смещается в коротковолновую часть спектра, и высокодисперсные системы рассеивают более короткие световые волны и поэтому имеют голубоватую окраску.
На спектрах рассеяния света основаны методы определения размера и формы
 частиц.
частиц.
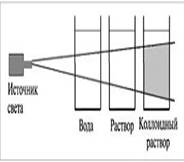
Методы исследования дисперсных систем (определение размера, формы и заряда частиц) основаны на изучении их особых свойств, обусловленных гетерогенностью и дисперсностью, в частности оптических. Коллоидные растворы обладают оптическими свойствами, отличающими их от настоящих растворов, – они поглощают и рассеивают проходящий через них свет. При боковом рассматривании дисперсной системы, через которую проходит узкий световой луч, внутри раствора на темном фоне виден светящийся голубоватый так называемый конус Тиндаля.
Суспензия иначе взвесь (англ. suspension) — дисперсная система, в которой твердые частицы дисперсной фазы находятся во взвешенном состоянии в жидкой дисперсионной среде.
Суспензии подразделяют на грубодисперсные (размер частиц — от 1 мкм до долей миллиметра) и мелкодисперсные (от 100 до 1000 нм). Первые неустойчивы и склонны к коагуляции. Суспензии, в которых частицы двигаются свободно, называют золями; если же частицы дисперсной фазы связаны в пространственную структуру, суспензию называют гелем. Суспензии получают методом диспергирования (измельчение твердых тел в жидкости) или конденсации (выделение твердой фазы из пересыщенных растворов). Суспензии имеют ряд общих свойств с порошками, они подобны по дисперсности. Если порошок поместить в жидкость и перемешать, то получится суспензия, а при высушивании суспензия снова превращается в порошок. Поэтому способы получения суспензий и порошков одинаковы, лишь при получении суспензий появляется дополнительная технологическая стадия – смешивание порошка с дисперсионной средой. Концентрированные суспензии (пасты) могут быть получены как в результате оседания более разбавленных суспензий, так и непосредственно растиранием порошков или массивных твердых тел с жидкостями.
Коагуляция иначе агрегация; флокуляция (англ. coagulation) — слипание коллоидных частиц друг с другом и образование из них более сложных агрегатов.
Коагуляция представляет собой процесс укрупнения частиц, а седиментация является конечным результатом этого процесса, однако термин «коагуляция» часто используют для обозначения данного явления в целом.
Золь иначе лиозоль; аэрозоль; коллоидный раствор (англ. sol) — высокодисперсная коллоидная система (коллоидный раствор) с жидкой (лиозоль) или газообразной (аэрозоль) дисперсионной средой, в объеме которой распределена другая (дисперсная) фаза в виде мелких твердых частиц, капелек жидкости или пузырьков газа.
Примером аэрозоля на основе жидкости является туман — взвесь капель воды в воздухе; находящийся в воздухе дым или пыль — пример твердотельного аэрозоля.
Гель (англ. gel) — (от лат. gelo - застываю или gelatus - замороженный, неподвижный): Гель представляет собой студенистое тело, способное сохранять форму и обладающее упругостью и эластичностью. Примеры веществ, образующих гели: аморфный (гелеобразный) гидроксид алюминия переменного состава Al2O3·nH2O, гидрогели кремниевых кислот (nSiO2·mH2O). При их высушивании получают, соответственно, алюмогель и силикагель — пористые вещества, используемые в качестве сорбентов и носителей для катализаторов.
Эму́льсия (новолат. emulsio, от лат. emulgeo — дою, выдаиваю) — дисперсная система, состоящая из микроскопических капель жидкости (дисперсной фазы), распределенных в другой жидкости (дисперсионной среде).
Эмульсии могут быть образованы двумя любыми несмешивающимися жидкостями; в большинстве случаев одной из фаз эмульсий является вода, а другой - вещество, состоящее из слабополярных молекул (жидкие углеводороды, жиры). Например, молоко — одна из первых изученных эмульсий: в нём капли молочного жира распределены в водной среде.
Эмульсии относятся обычно к грубодисперсным системам, поскольку капельки дисперсной фазы имеют размеры от 1 до 50 мкм. Эмульсии низкой концентрации —неструктурированные жидкости. Высококонцентрированные эмульсии — структурированные системы.
Тип эмульсии зависит от состава и соотношения ее жидких фаз, от количества и химической природы эмульгатора, от способа эмульгирования и некоторых других факторов.
Прямые, с каплями неполярной жидкости в полярной среде (типа «масло в
воде»)
Для эмульсих типа м/в хорошими эмульгаторами могут служить растворимые в воде мыла (натриевые и калиевые соли жирных кислот).
Обратные, или инвертные (типа «вода в масле»). Для эмульсии типа в/м хорошими эмульгаторами могут быть нерастворимые в воде мыла (кальциевые, магниевые и алюминиевые соли жирных кислот).
Так же эмульсии разделяются на лиофильные и лиофобные:
Лиофильные эмульсии образуются самопроизвольно и термодинамически устойчивы.
Лиофобные эмульсии возникают при механическом, акустическом или
электрическом эмульгировании (диспергировании), а также вследствие конденсационного образования капель дисперсной фазы в пересыщенных растворах или расплавах. Они термодинамически неустойчивы и длительно существуют лишь вприсутствии эмульгаторов — веществ, облегчающих диспергирование и препятствующих коалесценции (слипанию).
Гранулометрический состав полимерных материалов характеризуется наличием частиц разных размеров, т.е. дисперсностью и степенью дисперсности. Величину частиц гранулированных и порошкообразных материалов измеряют в миллиметрах или микронах.
Степень дисперсности (в %) показывает наличие частиц определенного размера в данном количестве порошка. Однородность порошка (по крупности частиц) характеризуется разницей размеров отдельных частиц.
Чем меньше разница, тем однороднее материал и наиболее пригоден для переработки его в изделия. От степени дисперсности и однородности полимерного материала зависят удельный объем, сыпучесть и физико-механические показатели. Степень дисперсности определяют обычно ситовым анализом.
Величину частиц можно определить микрометрическим методом.
Ситовый анализ заключается в разделении пробы материала по фракциям путем просева через набор сит с различными ячейками и определении остатка на каждом сите. Стандартные сита имеют поддон для приема материала, прошедшего через сито, и крышку, предохраняющую от потерь тонких фракций материала.
 2020-10-10
2020-10-10 461
461








