O2: FeO Fe2O3 FeO3 Fe3O4
CoO Co2O3 CoO2 Co3O4
NiO Ni2O3 NiO2 Ni3O
Fe3O4=Fe2O3+FeO.Чтобы получить гидроксид брать соль+щелочь
Fe(2) FeSO4+2NaOH→Fe(OH)2↓+Na2SO4
Fe(OH)2+2H+=Fe2++2H2O,Fe(OH)2+OН -→(—)-осн.св-ва Fe(OH)2
Fe(OH)2 неустойчив,легко окисл O2 воздуха:Fe(OH)2+O2+H2O→Fe(OH)3(бурый)
Fe Cl3+3KOH=Fe(OH)3+3KCl
Fe(OH)3 амфотерен с преобл.осн.св-в
Fe(OH)3+OH- практически не идет
Согласно совр.предст. Fe(OH)3 в вод.растворах сущ-ет в виде FeOOH оксида гидроксида (3)Ферриты сильно гидролизуют и в результате гидролиза:
NaFeO2+H2O→←FeOOH+NaOН
NaFeO2+2H2O→←Fe(OH)3+NaOH
Гидроксида Fe+6 не существует.
Co(2):2CoSO4+2NaOН→Co(OH)2SO4+Na2SO4(Синий осадок)
CoSO4+2NaOH→Co(OH)2(розовый)+Na2SО4
α-Со(ОН)2(синий)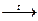 β – Co(OH)2(розовый)
β – Co(OH)2(розовый)
Co(OH)2 имеет преимущ.осн.св-ва
Со(ОН)2+ОН-→(—)
Со(ОН)2+2Н+=Co2++2H2O
Со(ОН)2+H2O+O2→Co(OH)3 — Реакция идет медленно. Чтобы ускорить, нужно взять более сильный ок-ль.
Со(ОН)2+H2O2+NaOH→Co(OH)3+…
H2O2+2e=2OH-
Co(OH)3 имеет так же только осн. св-ва.
Co(OH)3+HCl→Co2++Cl2+…|ОВР
Когда подливаем HCl падает степень ок-я
Ni(II):NiSO4+2NiOH→Ni(OH)2↓+Na2SO4
Ni(OH)2+O2(H2O2)+NaOH→(—)
Ni(OH)2+Cl2+NaOH→Ni(OH)3(чётный)+Cl-
Ni(III): Ni(OH)3+HCl→Ni2++Cl2++…|ОВР
Соли:
Fe(II): FeSO4+KMnO4+H2SO4→Fe3++Mn2+…
Fe(III): FeCl3+KI+H2SO4→Fe2++I2+ …
Co2+, Ni2+ - не участвуют
Fe+KN+5O3+KOH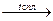 K2Fe+6O4(феррат) +KN+3O3
K2Fe+6O4(феррат) +KN+3O3
K2FeO4+H2O→Fe(OH)3↓+O2 H2FeO4
Fe2+, Fe3+, Co2+,Co(III), Ni2+—хорошие КО
Fe(II): FeSO4+2KCN=Fe(CN)2↓+K2SO4
Fe(CN)2+4KCN=K4[Fe(CN)6] – жёлтая кровяная соль, реактив на Fe3+
Fe3++K++[Fe(CN)6]4-= KFe3+[Fe2+(CN)6]↓ - берлинская лазурь
K4[Fe2+(CN)6]+J2→KJ+K4[Fe3+(CN)6] – красная кровяная соль, реактив на Fe2+
Fe2++K++[Fe(CN)6]3-= KFe2+[Fe3+(CN)6]↓ - турнбулева синь
Со временем KFe2+[Fe3+(CN)6] меняется на KFe3+[Fe2+(CN)6] и наоборот
FeCl3+3KSCN=Fe(SCN)3+3KCL
Fe(SCN) +3KSCN=K3[Fe(SCN)6]
Co(II)
CoCl2(синяя)+6H2O=[Co(H2O)6]Cl2(розовый) —индикатор влажности
K2[Ni(CN)6] — соль для блестящего никелирования
 2014-02-04
2014-02-04 1218
1218







