ОНКОГЕНЫ
Вирусные онкогены (V-onc), обычно известные как раковые гены являются генами, которые кодируют белки, вызывающие трансформацию нрмальных клеток в раковые. Онкогены не существенны для репликации вируса, и мутанты, испытывающие их недостаток, реплицируются нормально, не являясь онкогенными.
Гены, похожие на вирусные онкогены найдены как в нормальных, так и в раковых клетках. Онкогены, выделенные из раковых клеток называются клеточными онкогенами (C-onc). Подобные гены, обнаруженные в нормальных клетках называются протоонкогенами. Они не имеют вирусного происхождения. Напротив, вирусные онкогены оказались клеточного происхождения. Клеточные онкогены содержат интроны, характерные для эукариотичных генов, тогда как вирусные онкогены - нет. Очевидно, вирусные онкогены, произошли в прошлом от протоонкогенов путем рекомбинации между ретровирусными и клеточными генами.
Протоонкогены широко распространены среди позвоночных и многоклеточных - от людей до мух. Они хорошо сохраняются в их геномах; предполагают что они выполняют некоторые существенные функции в нормальных клетках. Было обнаружено, что они кодируют белки, участвующие в регулировании роста клетки и ее дифференцировании. Предполагаемые функции многих онкогенов были идентифицированы. Например, онкоген src связан с тирозин-специфическими протеинкиназами, sis - с фактором роста, продуцируемым тромбоцитами, myc - с ДНК-связанными белками, все они связаны с регулированием нормального роста клетки.
Ценный метод для изучения онкогенов - трансфекция. Определенные линии фибробластов мыши, такие как NIH 3T3, могут воспринимать чужую ДНК, включать ее в геном и проявлять ее. Этот метод передачи гена называется «трансфекция». Этим методом ДНК, извлеченная из человеческих опухолевых клеток, преобразовывала 3T3 клетки, и такие гены преобразования оказались идентичными с клеточными онкогенами.
Анти-онкогены. В нормальных клетках человека была идентифицирована категория генов, функцией которых оказалось подавление злокачественной трансформации. Они были названы анти-онкогены, ингибиторы опухоли или гены-супрессоры роста. Их прототип – ген ретинобластомы, потеря которого связана с развитием ретинобластомы у детей. Специфические хромосомальные делеции, связанные с определенными типами опухолей человека могут отражать потерю генов-супрессоров опухоли.
Русский ученый академик Л.А.Зильбер предложил вирусо - генетическую теорию онкогенеза, которая в настоящее время получает все большее подтверждение и дальнейшее развитие.
Основные постулаты теории ЗилЬбера:
1.Все известные естественно развивающиеся опухоли животных вызываются вирусами. Поэтому можно предположить, что опухоли человека также имеют вирусную природу.
2. Для вирусного онкогенеза необходима интеграция генома онкогенного вируса в клеточный геном, и это приводит к нарушению регулции размножения клеток и опухолевому росту.
3. Онкогенные виурсы являются пусковым фактором в развитии опухоли. В дальнейшем росте опухоли вирус участия не принимает, может вообще исчезнуть из клетки, или присутствовать в ней в качестве «пассажира". По выражению Л.Зильбера - " Мавр сделал свое дело, мавр может и уйти».
Теория предложена в конце 1950-х. С того времени теория обогатилась новыми фактами, подтверждающими ее основные положения.
В случае онкогенных ДНК-содержащих вирусов вирусная ДНК (или ее часть) интегрирована с геномом клетки-хозяина. РНК-содержащие вирусы, ретровирусы интегрируют свой геном в форме провируса. Вирусная ДНК, будучи неполной или «дефектной», неспособна обеспечить воспроизводство инфекционных вирусов. Однако под ее влиянием клетка-хозяин подвергается злокачественной трансформации. Трансформированная вирусом раковая клетка во многом аналогична бактерии, пораженной дефектным фагом. В обоих случаях клетка не разрушается, и вирусы не продуцируются. Приобретение новых характеристик трансформированной клеткой походит на лизогенную конверсию у бактерий. Вообще, ретровирусы вызывают развитие опухолей двумя путями - или путем внедрения в клеточный геном нового трансформирующего гена (онкогена) или, стимулируя или изменяя экспрессию существующего клеточного гена.
Несколько молекулярных механизмов были предложены для объяснения преобразования доброкачественных протоонкогенов в гены рака. Гены могут сверхэкспрессироваться, и их продукт может вызывать ненормальный рост. Рекомбинация между ретровирусными и клеточными генами, вставка промотора, хромосомная транслокация, амплификация гена и мутация - вот некоторые из генетических процессов, связанных с этим.
РЕКОМЕНДОВАННАЯ ЛИТЕРАТУРА
1. Пяткін К. Д., Кривошеїн Ю.С. Мікробіологія. - К: Высшая школа, 1992. - 432 с.
Тимаков В.Д., Левашев В.С., Борисов Л.Б. Микробиология. - М: Медицина, 1983. - 312 с.
2. Борисов Л.Б., Козьмин-Соколов Б.Н., Фрейдлин И.С. Руководство к лабораторным занятиям по медицинской микробиологии, вирусологии и иммунологии / под ред. Борисова Л.Б. – Г.: Медицина, 1993. – 232 с.
3. Медицинская микробиология, вирусология и иммунология: Учебник под ред. А.А.Воробьева. – М.: Медицинское информационное агентство, 2004. - 691 с.
4. Медицинская микробиология, вирусология, иммунология /ред. Л.Б.Борисов, А.М.Смирнова. - М: Медицина, 1994. - 528 c.
5. Букринская А.Г. Вирусология. – М.:Медицина, 1986. – 336 с.
Лекция 25. ВИРУС ИММУНОДЕФИЦИТА ЧЕЛОВЕКА
Первые указания на новое заболевание – Синдром Приобретенного Иммунодефицита (СПИДе) появились летом 1979 года, когда поступили сообщения из крупных городов США (Нью-Йорка, Лос-Анджелеса, Сан-Франциско) о внезапном увеличении распространенности у молодых людей, которые были гомосексуалистами или употребляли героин и другие инъекционные наркотики, двух очень редких болезней - саркомы Капоши (ранее регистрировавшейся лишь у пожилых африканцев) и пневмонии, вызванной Pneumocystis carinii (ранее описанной в виде эпидемий в закрытых детских учреждениях). Заболевания проявлялись в потере иммунокомпетентности, что приводило к незащищенности как против трудно поддающихся лечению и фатальных инфекций, вызванных относительно маловирулентными микроорганизмами, так и против злокачественных новообразований в лимфоидной и других системах.
О выделении возбудителя вначале сообщили в 1983 г. Люк Монтанье с сотрудниками из Института Пастера. Они изолировали ретровирус от больного из Западной Африки с персистирующей генерализованной лимфаденопатией, которая является проявлением СПИДА, и назвалаи его Lymphadenopathy Associated Virus (LAV ).
В 1984 г. Роберт Галло и сотрудники из Национального Институтов Здоровья, США, сообщили о выделении от больных СПИДом ретровируса и назвали его «Человеческий T –лимфотропный вирус-III», илиHTLV-III. Ретровирусы HLTV-I и II ранее ранее были описаны в связи с T-клеточной лейкемией человека. HTLV-III можно было культивировать в перевиваемой культуре клеток T-клеточной лейкемии, получая в достаточном количестве антиген для серологических тестов.
Серологический анализ и молекулярное клонирование позволили установить общее происхождение этих вирусов, несмотря на различной степени антигенные отличия между этими изолятами, которым дали раньше разные названия. Для разрешения этого номенклатурного недоразумения Международный комитет по номенклатуре вирусов в 1986 г. остановился для этих вирусов на родовом названии Human Immunodeficiency Virus (HIV), или Вирус Иммунодефицита Человека (ВИЧ).
В 1984 г. стали доступными первые серологические тесты для обнаружения анти-ВИЧ антител. Это сделало возможным более реальную оценку распространенности ВИЧ инфекции. До этого инфекция могла быть диагностирована только тогда, когда у больных развивались характерные клинические проявления типа оппортунистических инфекций или злокачественных новообразований. Эти случаи заключительных стадий представляли только верхушку айсберга. Серологический скрининг групп высокого риска, доноров и др. показал очень большой и расширяющийся резервуар ВИЧ-инфекции у больных и носителей в различных регионах мира. Было установлено, что в мире каждую минуту инфицируется ВИЧ более трех человек. Прогнозируется, что к 2000 году число ВИЧ-инфицированных людей в мире составит 40 миллионов, а больных СПИДом - 15 миллионов.
ВИРУС ИММУНОДЕФИЦИТА человека (ВИЧ)
ВИЧ, возбудитель СПИДА, относится к подсемейству Lentivirinae семейства Retroviridae. Подсемейство Lentivirinae (от L. lentus = медленно) включает возбудителей медленных вирусных инфекций висна/мэди овец и др. Помимо ВИЧ в эту группу включены также вирусы иммунодефицита животных.
Структура. ВИЧ – оболочечный вирус сферической формы размером 90 -120 нм (рис. 1).
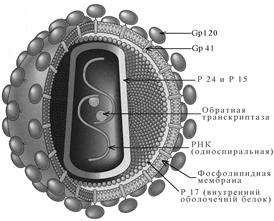 Рис. 1. Вирион ВИЧ
Рис. 1. Вирион ВИЧ
Нуклеокапсид имеет наружную оболочку икосаэдрической формы и внутреннее конусообразное ядро, окружающее рибонуклеопротеид. Геном - диплоидный, состоящий из двух одинаковых спиралей плюс-нитей РНК. В ассоциации с вирусной РНК находится фермент обратная транскриптаза, которая является характерной особенностью ретровирусов. Когда вирус инфицирует клетку, вирусная РНК транскрибируется ферментом сначала в односпиральную ДНК, а затем в двухспиральную ДНК (провирус), которая интегрируется в хромосому клетки - хозяина. Провирус может оставаться в скрытом состоянии в течение длительного времени, хотя это и влияет на функции клетки - хозяина. Время от времени, в ответ на действие факторов, активирующих вирус, провирус индуцирует репликацию вируса путем управления синтезом вирусной РНК и других компонентов вируса.
Во время репликации вируса, когда лишенные оболочки отпочковующиеся вирусы проходят через оболочку клетки, они приобретают липопротеидную оболочку, состоящую из липидов оболочки клетки-хозяина и гликопротеидов, кодируемых вирусом. Большинство кодируемых вирусом протеинов в проекции имеют вид поверхностно расположенных кнопкообразных шипов с закрепляющими их трансмембранными ножками. Шипы, являются основным поверхностным компонентом вируса, который связывается с CD4 рецепторами на восприимчивых клетках.
Вирусные гены и антигены. Геном ВИЧ содержит три структурных гена (gag, pol и env) характерные для всех ретровирусов, также как и другие неструктурные и регуляторные гены, специфичные для вирусов. Продукты этих генов, структурных и неструктурных, являются антигенами. Сыворотки инфицированных людей содержат антитела к ним. Обнаружение этих антигенов и антител имеет большое значение для диагностики и прогноза ВИЧ-инфекции.
A. Кодирующие гены для структурных белков:
1. Ген gag определяет сердцевину и оболочку вируса. Его продуктов является белок-предшественник p55. (Белки и гликопротеиды обозначаются по их молекулярной массе, выраженной в килодальтонах.). Этот белок- предшественник расщепляется на три белка, pl5, pl8 и p24, которые составляют сердцевину вируса и оболочку. Главный сердцевинный антиген - p24 может быть обнаружен в сыворотке в ранней стадии ВИЧ инфекции, прежде, чем появляются антитела. Позднее в течение инфекции исчезновение из кровотока свободных anti-p24 антител указывает на отягощение болезни и служит показанием для активного антивирусного лечения.
2. Ген env определяет синтез гликопротеида оболочки gp l60, который расщепляется на два компонента оболочки - gp l20, который образует поверхностные шипы, и gp 41, являющийся трансмембранным прикрепляющим белком. Гликопротеид шипов gp l20 - главный антиген оболочки, и антитела к gpl20 появляются первыми после инфицирования.
3. pol ген кодирует обратную транскриптазу и другие вирусных ферменты, типа протеазы и эндонуклеазы. Он экспрессируется как белок-предшественник, который расщепляется на белки p31, p51 и p66.
 2014-02-02
2014-02-02 7457
7457








