Классы (типы) катализаторов
Катализаторы можно разделить на два больших класса, каждый из которых представлен, в основном, соединениями переходных металлов или самими этими металлами.
1) Гетерогенные катализаторы
Гетерогенный катализатор – это любой катализатор, который нерастворим в реакционной смеси.
Наиболее употребляемые гетерогенные катализаторы:
– Никель (Ni) Ренея;
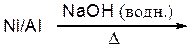
– Pd/C (палладий на угле), Pd/BaSO4;
– NaBH4 + восстановленный никель («борид» никеля);
– металлическая Pt или ее оксид PtO2 («чёрный диоксид», катализатор Адамса);

– родий Rh (Rh/C);
– рутений Ru;
– NaH-RONa-Ni(OAc)2;
– ZnO.
Наиболее эффективными катализаторами являются Ru и Rh, но большее распространение имеют Pt и Ni Ренея.

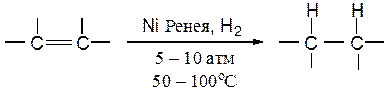

2) Гомогенные катализаторы
Гомогенный катализатор – это катализатор, который растворим в реакционной среде.
Наиболее употребляемые гомогенные катализаторы:
– катализатор Уилкинсона –– трис(трифенилфосфин)родий хлорид Rh(PPh3)3Cl (комплекс хлорида родия (I)), селективно гидрирует олефины (-COOR, -NO2, -CN, -C(O)R, -C(O)H – любой из этих заместителей может быть сохранен при гидрировании);
– хлоротрис(трифенилфосфин)гидридорутений (II) (Rh3P)3RuClH (степень окисления рутения равна двум); этот катализатор используется для специфического восстановления концевых (терминальных) двойных связей;
– пентацианокобальт-ион [Co(CN)5]3- – комплексный анион (используется для специфического восстановления двойных связей, сопряженных с С=О, С=С, Ar).
Как и в случае гетерогенно-каталитического гидрирования, при гомогенно-каталитическом гидрировании происходит син-присоединение водорода:

Преимущества гетерогенных катализаторов
Гетерогенные катализаторы легко отделяются от реакционной массы, и их возможно регенерировать или утилизировать.
Недостатки гетерогенных катализаторов
Гетерогенный катализ осуществляется, как правило, в более жестких условиях, чем гомогенный, и поэтому возможность селективного восстановления кратных связей С=С в случае присутствия в молекуле заместителей с кратными связями уменьшается по сравнению с гомогенным катализом. Кроме того, возможна изомеризация алкена в ходе восстановления и гидрогенолиз, т. е. расщепление одинарных связей С–С.
Преимущества гомогенных катализаторов
1) лучшая «воспроизводимость» катализатора;
2) высокая селективность;
3) меньшая чувствительность к действию каталитических ядов (к ним относятся, например, RSH, R2S, S);
4) возможность осуществления энантиоселективного гидрирования с высокой степенью оптической чистоты (> 90%).
Недостаток гомогенных катализаторов
Гомогенные катализаторы трудно выделить из реакционной массы.
Устойчивость к гидрированию обычно возрастает с увеличением числа заместителей, что, вероятно, обусловлено, стерическими факторами. Это позволяет селектинво восстанавливать моно- и дизамещенные двойные связи в присутствии в той же молекуле три- и тетразамещенных двойных связей:

Хотя каталитическое гидрирование представляет собой наиболее применяемый метод, для восстановления С=С можно использовать и другие реагенты:
– Na в EtOH (in situ);
– Na в смеси t-BuOH + ГМФТА (гексаметапол) (in situ, in statu nascendi);
– Cr2+;
– Zn в кислотах (in situ, in statu nascendi);
– NaTeH;
– H2O и осажденный Ni;
– гидразин (NH2-NH2) в присутствии небольшого количества окислителей (воздух, H2O2, Cu2+);
HN=NH (диимид)
– NH2OH + этилацетат и др.;
– гидриды щелочных металлов (LiAlH4 – алюмогидрид лития, NaBH4 – боргидрид натрия) – как правило, не восстанавливают двойную связь:
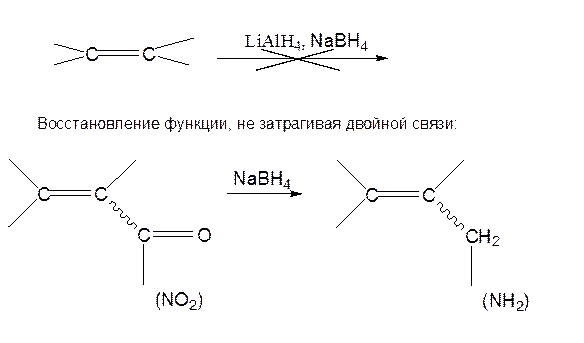
 2014-02-02
2014-02-02 1694
1694








