Преимущественно применяют двунатриевую соль ЭДТУ – ЭДТА, комплексон III, трилон Б:
Все комплексоны – это полидентатные лиганды, ЭДТА – гексадентатный лиганд, (4 атома кислорода, 2 атома азота).
Образующие с ионами металлов (кроме щелочных) устойчивые комплексы состава 1: 1, называем комплексонатами.
 Ме2+ + Na2H2Y
Ме2+ + Na2H2Y MeY2+ + 2Na+ + 2H+
MeY2+ + 2Na+ + 2H+
Ме3+ + Na2H2Y MeY– + 2Na2+ + 2H+
MeY– + 2Na2+ + 2H+
Ме3+ + Na2H2Y MeY + 2Na2+ + 2H+
MeY + 2Na2+ + 2H+

М(1/1Ме)
М(1/1ЭДТА)
Устойчивость комплексонатов (комплексов Ме с комплексонатами) различные и характеризуются константой устойчивости (нестойкости)
MeY2-  Me2+ + Y4-
Me2+ + Y4-
Kуст =  ; Кнест =
; Кнест = 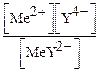 ;
;
lgКуст = рКнест
| Ион металла | lgКуст (рКн) | Ион металла | lgКуст (рКн) | Ион металла | lgКуст (рКн) |
| Fe3+ | 25,1 | Ni2+ | 18,6 | Al3+ | 16,1 |
| Th4+ | 23,2 | Pb2+ | 18,0 | Ca2+ | 10,7 |
| Cr3+ | 23,0 | Zn2+ | 16,5 | Mg2+ | 8,7 |
| Cu2+ | 18,8 | Co2+ | 16,3 | Ba2+ | 7,8 |
На практике правильно использовать условную константу устойчивости, учитывающую конкурирующие реакции комплексообразования β’ = Kн / α, мы будем принимать α = 1, т. е. создавать такие условия при титровании, при которых конкурирующей реакцией можно пренебречь.
Титриметрический анализ возможен в том случае, если рβ’ > 8, β’ – зависит от рН раствора, поэтому ионы металлов, образующие комплексонаты с достаточно большими Куст титруют в кислой среде; ионы металлов, образующие менее устойчивые комплексы следует титровать в щелочных растворах.
3. В качестве индикаторов в комплексонометрии обычно применяют органические соединения – красители, образующие с ионами металла комплексные соединения различной окраски. Такие индикаторы называются металлохромными индикаторами или металлиндикаторами.
Требования:
- комплекс металла с индикатором должен быть менее прочным, чем комплекс Ме с комплексоном;
- собственная окраска индикатора и окраска комплекса металла с индикатором должны быть различны.
Механизм изменения окраски
Н2Ind + Me2+ → MeInd + 2H+
синий б\ц красный
MeInd + H2Y2- → Me2+ + H2Ind
красный б\ц синий
Для четкого и правильного фиксирования конечной точки титрования рМе в т.э. должно находиться в области рМе, где комплекс MeInd разрушается.
Интервал перехода окраски индикатора
MeInd -  Me2+ +Ind2-
Me2+ +Ind2-
Kнест. = 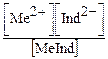
[Me2+] = Кнест.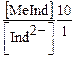 или
или 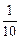
∆рМе = рКнест. ± 1
 2014-02-02
2014-02-02 2011
2011








