O O этиловый эфир уксусной кислоты





 R-C CH3-C этилацетат
R-C CH3-C этилацетат
OR’ OC2H5 этилэтаноат
Способы получения: 1) Реакция этирификации
2) Через ангидриды
3) Алкилирование солей карб.кислот галогеналканами
Химические свойства: ** Гидролиз
а) в кисл.среде (обратимый)
O H+ O
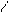
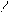
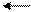
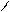
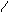 R-C + HOH R-C + R’OH
R-C + HOH R-C + R’OH
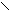
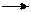
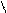 OR’ OH
OR’ OH
Механизм:
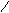
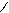
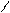
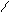 O: O+-H OH +НОН H
O: O+-H OH +НОН H
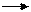
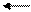

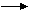
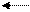
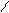

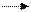
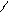
 R-C + H+ R-C R-C+ R-C-OR’
R-C + H+ R-C R-C+ R-C-OR’



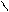
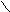
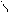 OR’ КАТ. OR’ OR’ O+
OR’ КАТ. OR’ OR’ O+
КарбокатионI H H
ОксониевыйионI
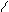
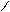
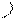
 H R’OH O-H O
H R’OH O-H O
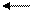





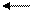
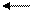
 R-C-OR R-C+ R-C + H+
R-C-OR R-C+ R-C + H+
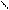
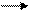 OH H O-H O-H возврат кат.
OH H O-H O-H возврат кат.
оксониевый ион II карбокатион II
б) в щелочной среде (необратимый)
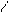
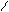
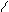
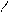 O O
O O
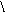
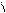 R-C + NaOH ®R-C + R’OH
R-C + NaOH ®R-C + R’OH
OR’ ONa
Механизм:
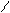
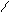
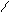

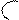
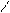
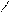 Oб O- O O
Oб O- O O
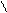
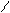
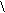

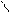 Rб+-C + OH- FR-C-OR’ ®R-C + R’O- ®R-C + R’OH
Rб+-C + OH- FR-C-OR’ ®R-C + R’O- ®R-C + R’OH
OR’ OH OH O- стабильный анион
Неустойчивый, они образуют
т.к. нет условий для более устойчивую
его стабилизации пару
Щелочной гидролиз называют омылением, т.к. при гидролизе жиров, яв-ся сл.эфирами трехатомного спирта и высших карб.кислот, образующих мыла.
** Взаимодействие с аммиаком, первич. и вторич. аминами (амманолиз и аминолиз)
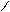
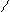
 O O
O O
 R-C + NH3®R-C + R‘OH
R-C + NH3®R-C + R‘OH
OR’ NH2
амид
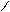 O O
O O

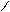
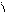
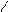
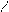 R-C + R”NH2 ® R-C + R’OH
R-C + R”NH2 ® R-C + R’OH
OR’ NHR”
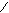
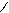
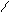
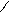 O H+ O
O H+ O
** R-C + R”OH F R-C + R’OH
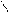
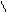 OR’ OR”
OR’ OR”
** Сложно-эфирная конденсация Кляйзена (идет при наличии Н у α- углеродного атома)
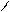
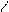
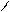
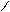 O O
O O
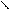
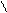 2 СH3-C C2H5ONa CH3-C-CH2-C
2 СH3-C C2H5ONa CH3-C-CH2-C


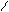
 OC2H5 O OC2H5
OC2H5 O OC2H5
Этиловыйэфирацетоуксуснойкислоты
Если взять 2 разных эфира, то образ. смесь 4-х разных продуктов.
** Восстановление
Чаще до первич. спиртов, реже в альдегиды и простые эфиры.
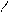
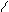 O
O
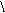 R-C + [H] ®R-CH2-OH-R’OH
R-C + [H] ®R-CH2-OH-R’OH
OR’
 2014-02-02
2014-02-02 637
637








