Механизм действия ферментов. Этапы ферментативного катализа.
После установления химической природы фермента было подтверждено представление Михаэлиса и Ментен о том, что при энзиматическом катализе фермент соединяется с субстратом (они подходят как ключ к замку), образуя нестойкий промежуточный фермент-субстратный комплекс, который в конце реакции распадается с освобождением фермента и продукта реакции.
Даниэль Кошланд предложил теорию «индуцированного» соответствия: т. е. что субстрат навязывает активному центру свою форму, а активный центр в свою очередь подгоняет форму субстрата под свою собственную.
Выдвинутая в 1913 году Л. Михаэлисом и М. Ментен общая теория ферментативного катализа постулировала, что фермент Е сначала обратимо и относительно быстро связывается с со своим субстратом S в реакции:
E + S == ES
Образовавшийся при этом фермент-субстратный комплекс ES, не имеющий аналогий в органической химии и химическом катализе, затем распадается в второй более медленной (лимитирующей) стадии реакции:
ES == Е + Р
1 этап: происходит сближение и ориентация субстрата относительно субстратного центра фермента и его постепенное «причаливание» к «якорной» площадке.
2 этап: напряжение и деформация: индуцированное соответствие - происходит присоединение субстрата, которое вызывает конформационные изменения в молекуле фермента приводящие к напряжению структуры активного центра и деформации связанного субстрата.
3 этап: непосредственный катализ.
Все химические реакции сопровождаются, как правило, разрывом или образованием ковалентных связей. По характеру разрыва ковалентных связей различают три типа реакций
1. Гетеролитический разрыв связи: ковалентная связь разрывается таким образом, что электронная пара остается с одним из атомов, образующим связь. Атом при этом приобретает отрицательный заряд, а у второго атома возникает положительный заряд. Такие реакции называют также ионными. Гетеролитически разрываются полярные или легкополяризующиеся ковалентные связи. Реакция катализируется кислотами или основаниями;
Гомолитический разрыв связи: при разрыве ковалентной связиэлектронная пара разделяется между атомами с образованием свободных радикалов. Свободные радикалы - это атомы или группы атомов с неспаренным валентным электроном.
одновременно без образования радикалов или ионов
2. Нуклеофильные реагенты: богатые электронами соединения: а) отрицательно заряженные ионы, б) нейтральные молекулы, имеющие свободную неподеленную пару электронов, в) реагенты, способные давать карбанионы в ходе реакций. Нуклеофилы реагируют с органическими субстратами по их положительному реакционному центру. Легко образуют ковалентные связи. Биологически важными нуклеофилами являются аминогруппы, гидроксильные группы, имидазольные группы и сульфгидрильные группы аминокислот. Нуклеофильные формы этих групп одновременно являются основаниями. Связываясь с Н+,- они основания, реагируя с другими электрондефицитными центрами – они нуклеофилы.
Электрофильные реагенты: Электрондефицитные соединения: а) положительно заряженные ионы; б) нейтральные молекулы с частично положительным зарядом на одном из атомов. Электрофилы реагируют с органическими субстратами по их отрицательному реакционному центру. Легко образуют ковалентные связи. Наиболее известными электрофилами в биохимических реакциях являются Н+, ионы металлов, углерод карбонильной группы.
Группы радикалов аминокислот – плохие электрофилы.
По числу молекул реакции можно разделить на мономолекулярные и бимолекулярные. В биологических системах реакции с большим числом участвующих молекул практически не встречаются.
По направлению реакций с учетом конечного результата можно выделить следующие типы реакций
1. Окислительно-восстановительные реакции включают потерю или присоединение электронов, в результате чего меняется степень окисления атомов, которые являются реакционными центрами. Многие окислительно- восстановительные реакции в клетке включают разрыв С-Н связи с отнятием у атома углерода двух электронов и переносе их на акцептор, роль которого могут выполнять коферменты. Конечный акцептор электронов у аэробных организмов кислород, представляющий бирадикал с двумя неспаренными электронами, Молекула кислорода поэтому может принимать только неспаренные электроны. Отнимаемые у субстрата пары электронов должны быть перенесены на кислород при помощи специальной электронпереносящей системы, включающей ряд переносчиков.
2. Реакции кислотно-основного взаимодействия. Взаимодействие между кислотами и основаниями с образованием солей
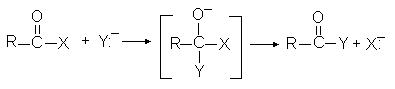
3. Реакции замещения. В ходе реакции происходит замена атомов или групп атомов на другие атомы или группы. Особое место среди реакций этой группы среди биохимических реакций занимают реакции переноса групп. Они включают перенос электрофильной группы от одного нуклеофила на другой. Такие реакции можно назвать реакциями нуклеофильного замещения. Наиболее часто переносимыми группами в биохимических реакциях являются ацильная, фосфатная и гликозильные группы. Примером такой реакции может быть гидролиз пептидной связи при помощи химотрипсина.
4. Реакции отщепления. Протекают одновременно по двум соседним атомам с отщеплением групп и образованием двойной связи. Отщепляемыми группами могут быть небольшие молекулы типа Н2О, NН3. Распад связи может проходить по одному из трех механизмов: а)согласованный механизм, б)постепенно с разрывом С-О связи и образованием карбокатиона, в) постепенно, с разрывом С-Н связи и образованием карбаниона. Ферменты катализируют отщепление воды двумя механизмами или протонированием ОН группы кислотой (кислотный катализ) или отщепление протона (основной катализ). Постепенное отщепление требует стабилизации образующихся заряженных групп противоположными по заряду группами (электростатический катализ). Одна из самых интересных реакций дихотомического процесса, катализируемая енолазой относится к этому типу реакций.
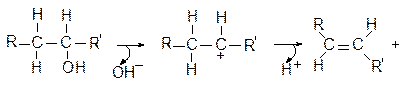
5. Реакции перегруппировки
- изменяют форму углеродного скелета молекул. Среди метаболических реакций такой тип реакций встречается довольно часто. Например, реакции изомеризации. В результате реакции происходит перераспределение электронной плотности и характера связей.
- Могут включать внутримолекулярный сдвиг водородного атома, таким образом, чтобы изменить расположение двойной связи. В таких реакциях протон отнимается у одного углеродного атома и переносится к другому. Наиболее распространенная реакция изомеризации - взаимное превращение альдоз в кетозы
Рацемизация - реакция изомеризации, в которой водородный атом изменяет свое стереохимическое положение в молекуле в хиральном центре. Эпимеризация то же самое, но молекула имеет несколько хиральных центров
6. Реакции, которые образуют или разрывают С-С связи. Это реакции, лежащие в основе и катаболизма и анаболизма. При превращении глюкозы в СО2 протекает 5 реакций разрыва С-С связей. Синтез глюкозы требует столько же реакций образования этих связей. Наиболее часто в этих реакциях принимает участие электрофильный карбонильный углеродный атом. Примерами могут быть реакции альдольной конденсации, катализируемые альдолазой, декарбоксилирование b-кетокислот (изоцитратдегидрогеназная реакция) и др.
2. Факторы, определяющие активность ферментов [E], [S], [P], Km. Влияние pH, [P], tº, ионной силы на активность ферментов.
У каждого фермента существует свой pH-оптимум. Существенное влияние на активность ферментов оказывает реакция среды. Для проявления их оптимального действия чаще всего существует узкий диапазон измерения pH среды (pH-оптимум). В некоторых случаях сдвиг pH на единицу снижает активность на 80%. Поэтому в экспериментальных условиях работы с ферментом очень важно поддерживать pH на постоянном уровне.
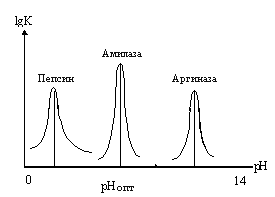 Слева приведены кривые зависимости активности фермента от изменения pH среды. Пепсин желудочного сока, который катализирует гидролиз белков, имеет pH-оптимум при pH=2. При pH=3 он теряет половину активности, а при pH=4 активность пепсина не измеряется. pH-оптимум амилазы, фермента, катализирующего расщепление крахмала, составляет 7,0. И в этом случае изменения pH на единицу приводит к снижению активности на 50%, а - на 2 единицы отмечается полная потеря активности. Относительно редко встречаются случаи, когда pH-оптимум активности ферментов находится в сильно кислой или щелочной среде. Это характерно для таких ферментов как пепсин и аргиназа (катализирует расщепление аргинина). Большинство белков при экстремальных значениях pH неустойчивы. рH-оптимум является важной характеристикой фермента, но ни как не исключительной, присущей только данному ферменту.
Слева приведены кривые зависимости активности фермента от изменения pH среды. Пепсин желудочного сока, который катализирует гидролиз белков, имеет pH-оптимум при pH=2. При pH=3 он теряет половину активности, а при pH=4 активность пепсина не измеряется. pH-оптимум амилазы, фермента, катализирующего расщепление крахмала, составляет 7,0. И в этом случае изменения pH на единицу приводит к снижению активности на 50%, а - на 2 единицы отмечается полная потеря активности. Относительно редко встречаются случаи, когда pH-оптимум активности ферментов находится в сильно кислой или щелочной среде. Это характерно для таких ферментов как пепсин и аргиназа (катализирует расщепление аргинина). Большинство белков при экстремальных значениях pH неустойчивы. рH-оптимум является важной характеристикой фермента, но ни как не исключительной, присущей только данному ферменту.
| Табл 2-2.Значения pH опт. некоторых ферментов | |
| Фермент | pH опт. |
| Липаза (подж.железа) | 8.0 |
| Липаза (желудок) | 4.0 - 5.0 |
| Липаза(касторовое масло) | 4.7 |
| Пепсин | 1.5 - 1.6 |
| Трипсин | 7.8 - 8.7 |
| Уреаза | 7.0 |
| Инвертаза | 4.5 |
| Мальтаза | 6.1 - 6.8 |
| Амилаза (подж.железа) | 6.7 - 7.0 |
| Амилаза (солод) | 4.6 - 5.2 |
| Каталаза | 7.0 |
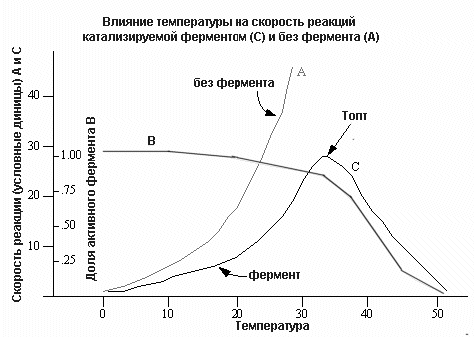
Влияние температуры на активность фермента
Дело в том, что многие ферменты имеют схожие значения pH-оптимумов. Механизм влияния pH среды на активность ферментов заключается в том, что изменение этого показателя приводит к изменению степени ионизации амино- (NH3) и карбосильных (СОО-) групп в молекуле фермента. В результате белковая молекула фермента подвергается конформационным перестройкам, что сказывается на взаимоотношения между ферментом и субстратом.
 2014-02-02
2014-02-02 679
679







